ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ЗАНЯТИЯ_Леч. Теоретический материал занятия
 Скачать 413 Kb. Скачать 413 Kb.
|
|
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ЗАНЯТИЯ Основные методы исследования ЦНС у человека 1. Стереотаксический метод. Современный стереотаксис - это нейрохирургический метод, обеспечивающий малотравматичный доступ к глубоко расположенным структурам головного мозга или патологическим образованиям и обеспечивающий возможность локального воздействия на них (стереотаксис от греч. "стереос" - пространство и "таксис" - расположение, порядок). Применение метода. Возникновение многих тяжелых заболеваний обусловлено возникновением небольшого по объему патологического очага в глубине мозговых структур, либо нарушением нормального функционирования тех или иных структур. Когда терапевтические методы лечения не дают эффекта, а обычные нейрохирургические вмешательства невозможны из-за риска повреждения здоровых участков мозга, следует прибегнуть к стереотаксическому вмешательству. Подобные ситуации возникают при органических поражениях головного мозга: опухоли, гематомы, кисты, которые трудно или просто невозможно удалить другим способом, также при паркинсонизме, эпилепсии, неукротимых болях и некоторых видах психических расстройств. Выполнение операции стереотаксическим методом может позволить взять фрагмент опухоли на исследование, разрушить опухоль путем ее замораживания или вживления радиоактивного источника, эвакуировать кровь из гематомы и опорожнить кисту и др. Современный стереотаксис можно рассматривать как одно из главных достижений нейрохирургии в этом направлении. Этапы стереотаксического вмешательства. Сначала выполняется томография головного мозга – компьютерная, рентгеновская, магнитно-резонансная или позитронно-эмиссионная (томография - это метод получения послойных изображений внутренних органов, в том числе мозга). После компьютерной обработки полученных данных на изображениях слоев мозга определяют координаты тех патологических очагов, которые и составляют основу болезни. Следующий этап проводится в операционной, в стерильных условиях - под местной анестезией практически безболезненно к голове пациента крепится стереотаксический аппарат (рис.1), который наводится на патологический очаг. После обезболивания делается разрез кожи длиной 2-3 см и в черепе сверлится небольшое отверстие диаметром около 1 см, через которое затем, точно в расчетную точку, вводится стереотаксический инструмент. В мозге нет болевых рецепторов, поэтому эта манипуляция совершенно безболезненна и не ощущается больным, и не требует наркоза. Погружению стереотаксического инструмента в мозг обязательно предшествует проведение расчетного интраскопического исследования. В его задачу входит получение диагностических сведений об анатомических особенностях строения мозга пациента, включая распознавание мишеней, и получение информации, необходимой для последующих стереотаксических расчетов и наведения стереотаксического инструмента на найденные целевые точки.  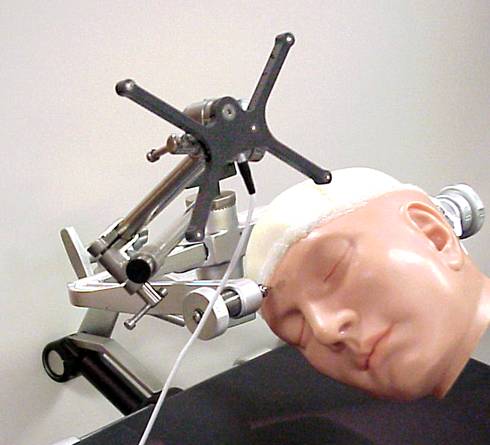 Рис.1: универсальный стереотаксический прибор для работы на головном мозге человека. 2. ЭЭГ человека. Электроэнцефалография (ЭЭГ) - метод исследования головного мозга, основанный на регистрации его суммарных электрических потенциалов. С помощью этого метода можно определять локализацию органических поражений мозга, а также, что более существенно, оценивать его функциональную активность. В стволе мозга и в передних отделах лимбической системы имеются ядра, активация которых приводит к изменению уровня функциональной активности практически всего мозга (рис.2). Эти образования подразделяются на восходящие активирующие системы, расположенные на уровне ретикулярной формации среднего мозга и в преоптических ядрах переднего мозга, и подавляющие, тормозящие, сомногенные системы, расположенные главным образом в продолговатом мозге, нижних отделах моста и неспецифических таламических ядрах. Активирующие ретикулокортикальные и лимбикокортикальные системы вызывают повышение уровня функциональной активности мозга, при активации сомногенных ретикулокортикальных и таламокортикальных систем уровень бодрствования снижается вплоть до засыпания. Возбуждение активирующих ретикулокортикальных систем приводит к возникновению на ЭЭГ десинхронизации, выражающейся появлением высокочастотной, нерегулярной, низкоамплитудной активности. При снижении активности мозга сокращается афферентный приток. Отдельные нейроны функционально объединяются при этом в огромные популяции с синхронизированной активностью, которая отражается на ЭЭГ медленными, регулярными, высокоамплитудными колебаниями. Распространение возбуждения в мозге, изменение потенциалов на мембранах нейронов создают неоднородное в пространстве и изменяющееся во времени электрическое поле. В связи с этим, между двумя точками мозга, а также между мозгом и удаленными от него тканями организма возникает разность потенциалов, которая и регистрируется с помощью метода электроэнцефалографии. При экспериментах на животных регистрируется электроэнцефалограмма коры и подкорковых структур. В клинических исследованиях ЭЭГ отводится, с помощью электродов, расположенных на интактных покровах головы человека и в некоторых экстракраниальных точках. 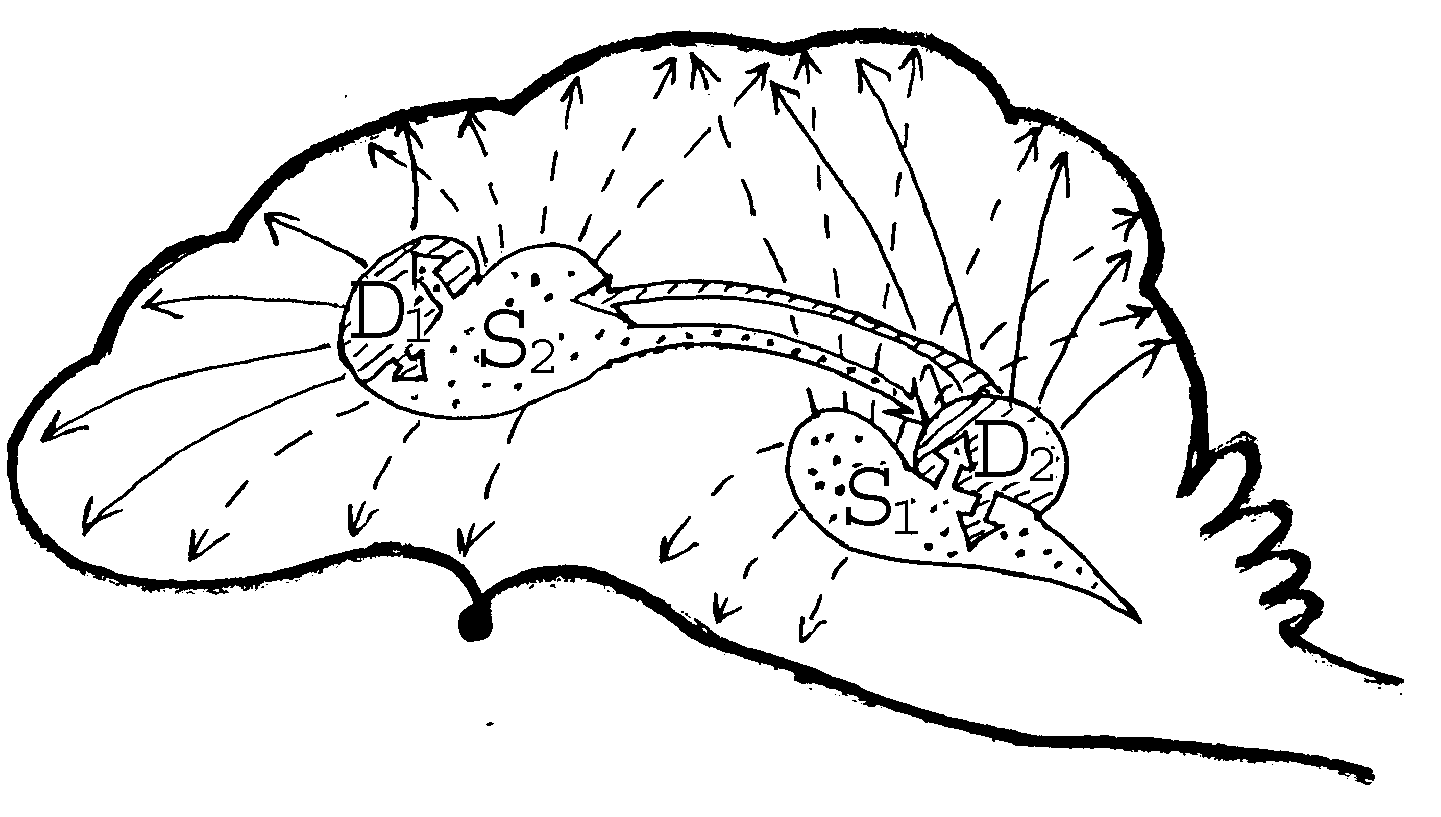 Рис. 2: схема восходящих систем регуляции уровня активности мозга. D1 и D2 -десинхронизирующие активирующие системы переднего мозга и среднего мозга, S1 и S2 - синхронизирующие тормозящие системы продолговатого мозга и моста и неспецифических ядер промежуточного мозга. В цифровых электроэнцефалографах ЭЭГ записывается на магнитном носителе или лазерном компакт-диске с одновременным выводом на экран. При записи ЭЭГ используют два основных метода: биполярный и монополярный. В первом случае оба электрода помещаются в электрически активные точки скальпа, во втором один из электродов располагается в точке, которая условно считается электрически нейтральной (мочка уха, переносица). При биполярной записи регистрируется ЭЭГ, представляющая результат взаимодействия двух электрически активных точек (например, лобного и затылочного отведений), при монополярной записи — активность какого-то одного отведения относительно электрически нейтральной точки (например, лобного или затылочного отведения относительно мочки уха). Выбор того или иного варианта записи зависит от целей исследования. В исследовательской практике шире используется монополярный вариант регистрации, поскольку он позволяет изучать изолированный вклад той или иной зоны мозга в изучаемый процесс. Международная федерация обществ электроэнцефалографии приняла так называемую систему "10-20", позволяющую точно указывать расположение электродов (рис.3). В соответствии с этой системой у каждого испытуемого точно измеряют расстояние между серединой переносицы (назионом) и твердым костным бугорком на затылке (инионом), а также между левой и правой ушными ямками. Возможные точки расположения электродов разделены интервалами, составляющими 10% или 20% этих расстояний на черепе. При этом для удобства регистрации весь череп разбит на области, обозначенные буквами и цифрами (четные – правое полушарие, нечетные – левое). Количество электродов, задействованных в эксперименте, может варьироваться в каждом конкретном случае. 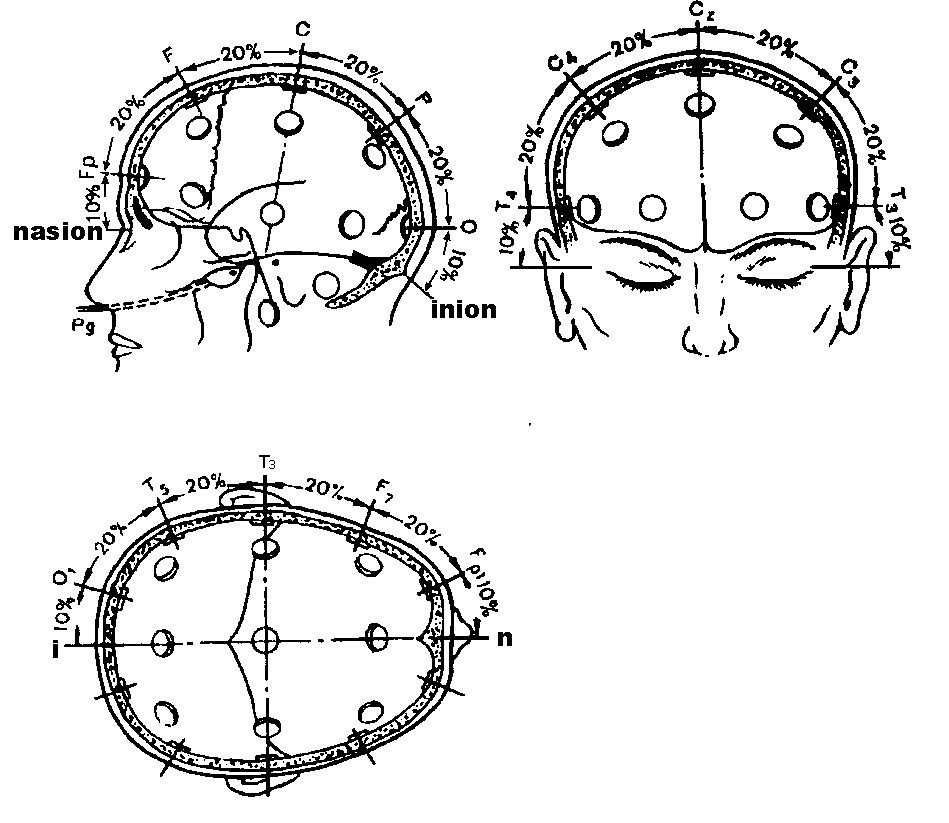 Буквенные индексы означают: О - затылочное отведение; Р - теменное отведение, С - центральное отведение; F - лобное отведение; Т - височное отведение; Та - переднее височное отведение; Тр -заднее височное отведение; d - правое полушарие мозга; s - левое полушарие. Рис. 3: международная схема расположения электродов 10-20. Каждый электрод подключен к усилителю. Для записи ЭЭГ может использоваться или бумажная лента или сигнал может преобразовываться с помощью АЦП и записываться в файл на компьютере. Наиболее распространена запись с частотой дискретизации 250 Гц. Основными характеристиками ЭЭГ являются частота и амплитуда: Частота определяется количеством колебаний в секунду и выражается в герцах (Гц). Амплитуда измеряется от пика предшествующей волны до пика последующей волны в противоположной фазе и выражается в микровольтах (мкВ), (рис. 4). Для пересчёта используется калибровочный сигнал. В соответствии с международным стандартом отклонение пера на 7 мм соответствует 50 мкВ. 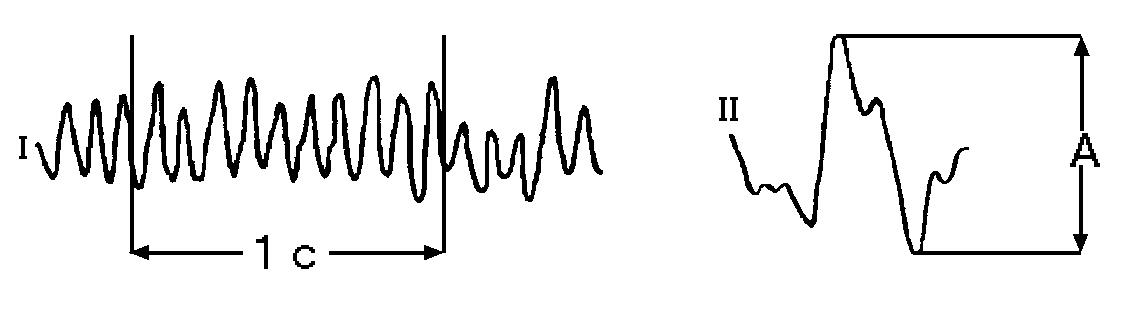 Рис. 4: измерение частоты (I) и амплитуды (II) на ЭЭГ. Определённый тип электрической активности, соответствующий тому или иному состоянию мозга, соответствует понятию «ритм». Для взрослого бодрствующего человека наиболее характерны α- (альфа) и β- (бета) ритмы. Основные ритмы ЭЭГ или классические диапазоны ЭЭГ (рис. 5). Альфа ритм Частота: 8-13 Гц Амплитуда: до 70 мкВ Генерация коркового альфа-ритма связана с ядрами таламуса и таламо-кортикальными связями. В настоящее наиболее распространена точка зрения, согласно которой в генерации альфа-ритма принимают участие как таламические, так и корковые пейсмекеры. Мощность диапазона альфа-ритма Мощность диапазона альфа-ритма возрастает, при: снижается при: 1.состоянии релаксации 1.состоянии депрессии 2.эмоциональном утомлении 2. деменции и паркинсонизме 3.состоянии голода 3. шизофрении Десинхронизация ритма – это резкое подавление альфа-ритма. Десинхронизацию вызывают: 1 напряженная умственная деятельность 2. уровень сложности когнитивной задачи 3. усиление внимания 4. движение глаз Бета – ритм Частота: 14-30 Гц Амплитуда: до 30 мкВ Выделяют бета-1, бета-2, бета-3 диапазоны. Мощность диапазона бета-ритма Мощность диапазона бета-ритма возрастает, при: снижается при: арифметических вычислений в уме при болезни Альцгеймера двигательной активности мысленном вращении фигур сенсорной стимуляции Тета– ритм Частота: 3-7 Гц Амплитуда: до 200 мкВ Ритм является одним из наименее изученных. Предположительно, берет свое начало от гиппокампа. Мощность диапазона тета-ритма возрастает, при: решение в уме трудных задач, процессы эпизодической памяти, ассоциативной и когнитивной деятельности, операторская деятельность, при управлении автомобилем, вербальная деятельность, релаксация, мозговая гипоксия, лишение сна, депрессия, в ряде патологий. Дельта – ритм Частота: 1-3 Гц Амплитуда: до 300 мкВ 1.Дельта-ритм находится в тесной взаимосвязи с разными стадиями сна, эффектами введения опиоидов и некоторыми патологическими состояниями мозга. 2. Наблюдается рост выраженности его компонентов с увеличением длительности лишения сна. 3. Также при когнитивной деятельности человека. 4 Дельта-ритм может быть связан с состоянием голода. 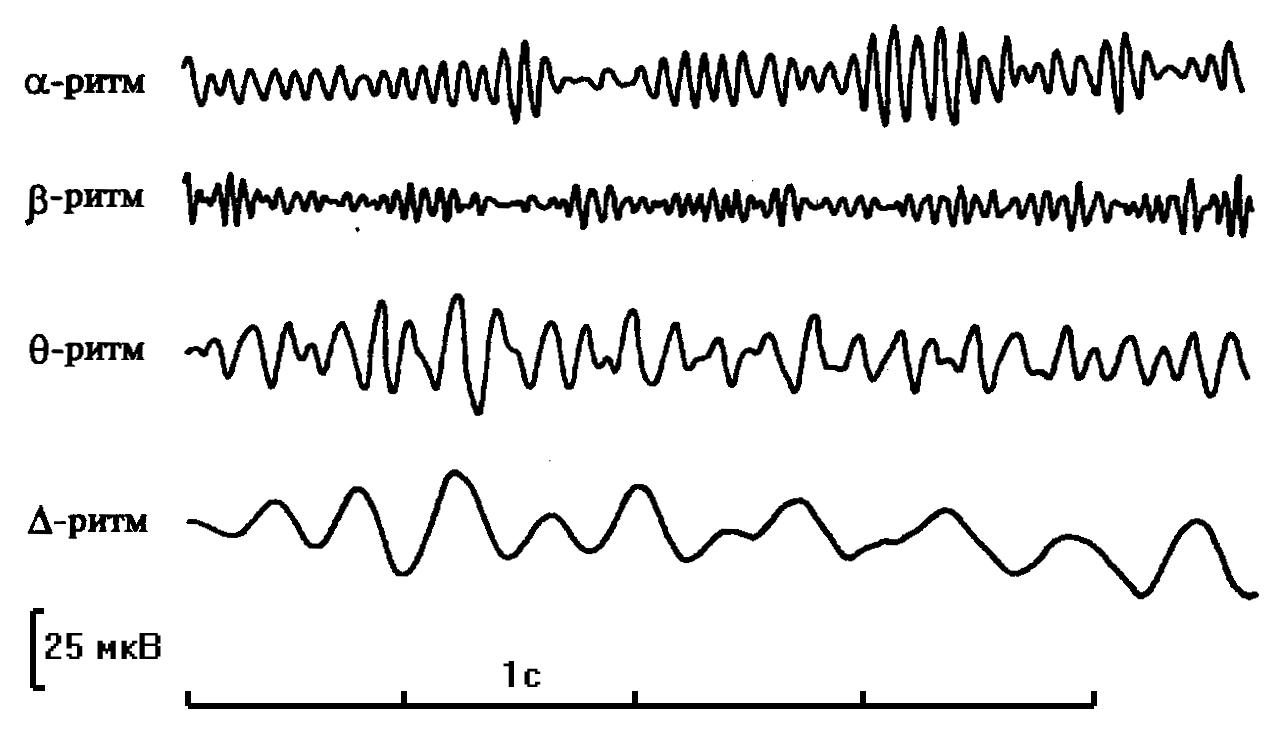 Рис. 5: основные ритмы ЭЭГ. Гамма-ритм Частота: более 30 Гц Амплитуда: до 15 мкВ Наблюдается при решении задач, требующих максимальной концентрации внимания и при сильной физической активности. С помощью ЭЭГ можно: следить за динамикой действия лекарственных препаратов; ценить степень нарушения работы мозга; исследовать функциональное состояние мозга; при повторных исследованиях ЭЭГ помогает оценить скорость и полноту исчезновения признаков нарушения работы мозга, от чего зависит дальнейшее лечение, можно выявить: 1) эпилепсия, не эпилептические кризовые состояния, мигрени; 2) объемные поражения мозга; 3) сосудистые поражения мозга; 4) черепно-мозговая травма; 5) воспалительные заболевания головного мозга. ЭЭГ в цикле сна. Первая стадия сна (дремота). Снижение амплитуды и исчезновение альфа-ритма. Появление на ЭЭГ одиночных и групповых низкоамплитудных тета и дельта волн. Появление на ЭЭГ низкоамплитудной высокочастотной активности. ЭЭГ в стадии дремоты описывается как "уплощенная, десинхронизированная с наличием полиморфной низкоамплитудной активности". Вторая стадия сна (поверхностный сон). "Сонные веретена" - диффузные вспышки колебаний частотой 11-15 Гц и амплитудой до 50 мкВ с наибольшей выраженностью в центральных отведениях, модулированные в веретена, генерализованные или билатерально-синхронные. "К-комплексы" - вспышки активности, состоящей из двухфазной высокоамплитудной волны с начальной негативной фазой и максимальной амплитудой в центральных отведениях. Вспышки полифазных высокоамплитудных медленных волн. Третья стадия сна (глубокий сон). Отсутствие "веретен сна" и "К-комплексов". Тета и дельта волны с амплитудой выше 75 мкВ, занимающие 20-50 процентов ЭЭГ. Четвертая стадия сна (очень глубокий сон). Дельта-волны с частотой 2 и менее Гц и амплитудой более 75 мкВ, занимающие более 50 процентов времени ЭЭГ. Пятая стадия сна (быстрый сон или сон с быстрыми движениями глаз).Полиморфная активность с преобладанием низкоамплитудных высокочастотных волн. Диффузное снижение мышечного тонуса с появлением саккадирующих быстрых движений глаз. Отсутствуют "сонные веретене" и "К-комплексы" В передне-центральных отведениях периодически выявляется "пилообразная" активность частотой 2-3 Гц. Алгоритм описания ЭЭГ. 1. Паспортная часть: номер ЭЭГ, дата исследования, фамилия, имя, отчество, возраст, клинический диагноз. 2. Описание ЭЭГ покоя. 3. Описание альфа-ритма: выраженность альфа-ритма (отсутствует, выражена вспышками - указать длительность вспышки и длительность интервалов между вспышками); распределение альфа-ритма; область доминирования альфа-ритма; симметрия альфа-ритма; образ альфа-ритма веретенообразный с хорошо выраженными веретенами, т. е. модулированный по амплитуде (на стыках веретен альфа-ритма нет); веретенообразный с плохо выраженными веретенами, т. е. недостаточно модулированный по амплитуде (на стыках веретен наблюдаются волны с амплитудами более 30% от максимальной амплитуды альфа-ритма); машиноподобный или пилообразный, т. е. не модулированный по амплитуде; пароксизмальный - веретено альфа-ритма начинается с максимальной амплитуды; аркообразный - большая разница в полупериодах; форма альфа-ритма: не искажена, искажена медленной активностью, искажена электромиограммой; частота альфа-ритма, ее стабильность. Частоту альфа-ритма определяют на случайных односекундных отрезках ЭЭГ на протяжении всего времени регистрации и выражают в виде средней величины (при наличии смены частоты при сохранении стабильности периодов указывают на смену частот доминирующего ритма). Амплитуда альфа-ритма. Отсутствие альфа-ритма отмечают всегда на первом месте. 4.Описание доминирующих и субдоминмрующих ритмов. Если альфа-ритм имеется, но есть и другая частотная компонента, представленная в меньшей степени, то после описания альфа-ритма ее описывают по тем же правилам. Пример 1. ЭЭГ N 3021 от 05.02.87. И-ов Ю.С., 42 года. Обследование. Альфа-ритм выражен регулярной компонентой, распределен правильно, доминирует в затылочных отделах мозга, симметричный, веретенообразный, с хорошо выраженными веретенами, не искажен, без вспышек гиперсинхронизации, частотой 10 колеб./с., амплитудой до 80 мкВ, индексом 85 %. Появления патологической активности необнаружено. 3. Анализ вызванных потенциалов или потенциалов связанных с событием у человека. Метод вызванных потенциалов (ВП) мозга основан на записи электроэнцефалограммы (ЭЭГ), которая измеряет спонтанную ритмическую активность мозга, происходящую с разной частотой. Вызванными потенциалами (event-related potentials, ERPs) называются биоэлектрические сигналы мозга, которые появляются с постоянными временными интервалами после определенных внешних воздействий, или стимулов. Выделяются следующие характеристики потенциала: форма (наличие или отсутствие пиков), латентность (временной промежуток от момента подачи стимула до появления пика), длительность и амплитуда пиков. Каждый потенциал представляет собой синусоидальную волну, амплитуда которой изменяется во времени, и при этом полярность участков волны меняется от положительной к отрицательной. Участки волны разной полярности принято называть компонентами и обозначать латинскими буквами P (positive) и N (negative). Положительная фаза первичного ответа есть результат местного возбуждения клеточных тел (перикарионов) пирамидных нейронов и слоёв коры полушарий переднего мозга под действием залпа афферентных импульсов. Отрицательная фаза первичного ответа возникает за счёт потенциалов, генерируемых дендритами поверхностных слоёв коры. В зависимости от периода времени анализа, т.е. времени возникновения мозговой активности после стимула, потенциалы подразделяются на коротколатентные, средне- и длиннолатентные. Коротколатентные потенциалы возникают уже через 10 мс после подачи стимула, в то время как среднелатентные после 100 мс, а длиннолатентные регистрируются значительно позднее, начиная от 300 мс и больше после сигнала. В основе метода ВП лежит суммация и усреднение большого количества потенциалов, каждый из которых сам по себе слишком слаб и часто не отличим от спонтанных ритмов, не имеющих отношения к сигналу. В течение определенного времени после подачи стимула производится вычисление амплитуд электро сигналов мозга, через временные интервалы, зависящие от частоты квантования. Полученные данные запоминаются и суммируются. В результате амплитуда стабильно возникающих после стимула потенциалов неуклонно возрастает, а амплитуда спонтанной ритмов в той же степени уменьшается. Для получения результируюших амплитуд ВП, амплитуда в каждой точке усредняется, т.е. делится на число стимулов. Вызванные потенциалы мозга широко применяются как в научных исследованиях, так и в клинической практике. Процедура проведения ВП эксперимента. Кресло испытуемого устанавливается на расстоянии 1 метра от экрана компьютера, на котором предъявляются стимулы. Испытуемому объясняются необходимые детали: минимизировать непроизвольные мускульные движения, по возможности контролировать движения глаз. ВП, вызванные движениями головы, других частей тела, и в особенности, глаз и морганием, считаются артефактами, и обычно удаляются из ЭЭГ в процессе автоматического фильтрования после окончания эксперимента. Результаты опыта: зарегистрировать ВП человека: зрительный (ВЗВП) на вспышечный стимул (в виде стимула используется светодиодная вспышка от матрицы светодиодов, вставленных в специальные очки, активные электроды размещают на затылочной области); слуховые (СВП) (применяются щелчки или тоны, подаваемые моноурально или биноурально через наушники, активные электроды размещают в вертексе), соматосенсорные (ССВП) (ВП, выделяемые на скальпе при тактильной или электрической стимуляции различных нервов, данные ВП отражают проведение афферентной волны возбуждения по путям общей чувствительности, электроды устанавливаются в центральной части скальпа) и когнитивные ВП. Применение:Исследование ЗВП – одна из важнейших областей применения методики ВП. Дает возможность: - лучить объективную информацию о состоянии зрительного нерва; - объективно оценить остроту зрения; - оценить зрительные нарушения; - оценка динамики лечения; - нарушения полей зрения и т.д. объективная оценка слуха; -дифференцировка органической и функциональной природы изменений; -расстройства улитки; -центральные расстройства адекватный метод исследования и диагностики поражений спинного и головного мозга; рассеянный склероз; оценка нарушений сенсорных чувствительных функций. ВП – класс электрофизиологических феноменов, которые специализированными методами выделяются из «фоновой» или «сырой» ЭЭГ. В характеристиках ВП проявляется связь активности мозга с событиями во внешней среде с психологическими характеристиками активности испытуемого (с ожиданием, принятием решения). ВП, с одной стороны, отражают активность мозга, с другой – характеристики поведения и психологическую феноменологию. ВП – представляют собой суммарный электрический потенциал различных компонентов ткани мозга, вклад в который вносят нейроны (сома, дендриты, аксоны), глиальные клетки, мембраны клеточных органелл. ВП может состоять из первичного ответа или же из первичного и вторичного. Первичные ответы характеризуются коротким латентным периодом (ЛП) и двухфазностью колебания: вначале положительная, затем — отрицательная. Первичный ответ формируется за счет кратковременной синхронизации активности близлежащих нейронов. Вторичные ответы более вариабельны по ЛП, длительности, амплитуде, чем первичные. Как правило, вторичные ответы чаще возникают на сигналы, имеющие определенную смысловую нагрузку. В зависимости от выделяемых реакций мозга ВП обычно классифицируют по модальности предъявляемого стимула или по условиям выделения генерации компонентов ответа (ВП ближнего или отдаленного поля). Кроме этого, ВП классифицируют на экзогенные и эндогенные стимулы. Экзогенные – колебания ВП с латентным периодом менее 100 мс, с зависимостью параметров от физических характеристик стимула. Эндогенные - колебания ВП с латентным периодом более 100 мс, с широким модально-неспецифическим распределением амплитуд по поверхности головы, с независимостью характеристик ВП от физических свойств события, их вызвавшего; связь параметров ВП с задачей, которую выполняет испытуемый и его психологическим состоянием. Особый вклад в генерацию ВП вносят потенциалы ВПСП и ТПСП дендритных волокон коры или различных ядер мозга. Меньший вклад в регистрацию ВП вносят собственно потенциалы действия. 4. Компьютерная томография (КТ) — новейший метод, дающий точные и детальные изображения малейших изменений плотности мозгового вещества. КТ соединила в себе последние достижения рентгеновской и вычислительной техники, отличаясь принципиальной новизной технических решений и математического обеспечения. Главное отличие КТ от рентгенографии состоит в том, что рентген дает только один вид части тела. При помощи компьютерной томографии можно получить множество изображений одного и того же органа и таким образом построить внутренний поперечный срез, или "ломтик" этой части тела. Томографическое изображение — это результат точных измерений и вычислений показателей ослабления рентгеновского излучения, относящихся только к конкретному органу. Таким образом, метод позволяет различать ткани, незначительно отличающиеся между собой по поглощающей способности. Измеренные излучение и степень его ослабления получают цифровое выражение. По совокупности измерений каждого слоя проводится компьютерный синтез томограммы. Завершающий этап — построение изображения исследуемого слоя на экране дисплея. Для проведения томографических исследований мозга используется прибор нейротомограф. Помимо решения клинических задач (например, определения местоположения опухоли) с помощью КТ можно получить представление о распределении регионального мозгового кровотока. Благодаря этому КТ может быть использована для изучения обмена веществ и кровоснабжения мозга. В ходе жизнедеятельности нейроны потребляют различные химические вещества, которые можно пометить радиоактивными изотопами (например, глюкозу). При активизации нервных клеток кровоснабжение соответствующего участка мозга возрастает, в результате в нем скапливаются меченые вещества и возрастает радиоактивность. Измеряя уровень радиоактивности различных участков мозга, можно сделать выводы об изменениях активности мозга при разных видах психической деятельности. Последние исследования показали, что определение максимально активизированных участков мозга может осуществляться с точностью до 1 мм. 5. Магнитно-резонансная томография (МРТ, MRT, MRI) — томографический метод исследования внутренних органов и тканей с использованием физического явления ядерного магнитного резонанса — метод основан на измерении электромагнитного отклика ядер атомов водорода на возбуждение их определённой комбинацией электромагнитных волн в постоянном магнитном поле высокой напряжённости, для этого используют аппарат для магнитно-резонансной томографии. Метод ядерного магнитного резонанса позволяет изучать организм человека на основе насыщенности тканей организма водородом и особенностей их магнитных свойств, связанных с нахождением в окружении разных атомов и молекул. Ядро водорода состоит из одного протона, который имеет магнитный момент (спин) и меняет свою пространственную ориентацию в мощном магнитном поле, а также при воздействии дополнительных полей, называемых градиентными, и внешних радиочастотных импульсов, подаваемых на специфической для протона при данном магнитном поле резонансной частоте. На основе параметров протона (спинов) и их векторном направлении, которые могут находиться только в двух противоположных фазах, а также их привязанности к магнитному моменту протона можно установить, в каких именно тканях находится тот или иной атом водорода. Если поместить протон во внешнее магнитное поле, то его магнитный момент будет либо сонаправлен, либо противоположно направлен магнитному моменту поля, причём во втором случае его энергия будет выше. При воздействии на исследуемую область электромагнитным излучением определённой частоты часть протонов поменяют свой магнитный момент на противоположный, а потом вернутся в исходное положение. При этом системой сбора данных томографа регистрируется выделение энергии во время «расслабления» (релаксации) предварительно возбужденных протонов. Для определения расположения сигнала в пространстве, помимо постоянного магнита в МР-томографе, которым может быть электромагнит, либо постоянный магнит, используются градиентные катушки, добавляющие к общему однородному магнитному полю градиентное магнитное возмущение. Это обеспечивает локализацию сигнала ядерного магнитного резонанса и точное соотношение исследуемой области и полученных данных. Действие градиента, обеспечивающего выбор среза, обеспечивает селективное возбуждение протонов именно в нужной области. Мощность и скорость действия градиентных усилителей относится к одним из наиболее важных показателей магнитно-резонансного томографа. От них во многом зависит быстродействие, разрешающая способность и соотношение сигнал/шум. Современные технологии и внедрение компьютерной техники обусловили возникновение такого метода, как виртуальная эндоскопия, который позволяет выполнить трёхмерное моделирование структур, визуализированных посредством КТ или МРТ. Данный метод является информативным при невозможности провести эндоскопическое исследование, например при тяжёлой патологии сердечно-сосудистой и дыхательной систем. Метод виртуальной эндоскопии нашёл применение в ангиологии, онкологии, урологии и других областях медицины. 6. Функциональная МРТ (ФМРТ) — метод картирования коры головного мозга, позволяющий определять индивидуальное местоположение и особенности областей мозга, отвечающих за движение, речь, зрение, память и другие функции, индивидуально для каждого пациента. Суть метода заключается в том, что при работе определенных отделов мозга кровоток в них усиливается. В процессе проведения ФМРТ больному предлагается выполнение определенных заданий, участки мозга с повышенным кровотоком регистрируются, и их изображение накладывается на обычную МРТ мозга.7. 7. Ультразвуковая допплерография сосудов головного мозга(УЗДГ). Это аппаратный метод исследования кровотока в сосудах, демонстрирующий в реальном времени в графическом, звуковом и количественном виде показатели кровотока в сосудах. УЗДГ позволяет заранее обнаружить предрасполагающие факторы для развития нарушений кровообращения. С помощью УЗДГ можно провести анализ целой совокупности параметров по группе сосудов головного мозга и шеи. Метод УЗДГ сосудов основан на эффекте Допплера: сигнал, посланный специальным датчиком, отражается от движущихся объектов (форменных элементов крови), и частота сигнала меняется пропорционально скорости кровотока. УЗДГ позволяет оценить равномерности потока крови в сосудах и характере его изменения, из-за сужения или закупорки просвета сосуда, обусловленное наличием атеросклеротической бляшки, тромба или воспаления. Также УЗДГ позволяет определить компенсаторные возможности кровотока, присутствие аномалий строения и хода сосудов - извитости, перегиба, аневризм; наличие и степень выраженности артериального спазма; вероятности сдавления артерии извне - рубцами, спазмированными мышцами или позвонками (позвоночных артерий). Важным компонентом УЗДГ исследования является оценка состояния венозного кровотока - нарушение оттока из полости черепа, проходимость глубоких вен нижних конечностей и состоятельность клапанов вен конечностей. Благодаря универсальности УЗДГ метода возможно обследование сосудов следующих органов и систем: сосудов головы и шеи, включая расположенные внутри головы, сосудов глаза, сосудов рук и ног. Метод применяется для: выявления ранних поражений сосудов; определения стенозов (сужение просвета) артерий и определить их значимость; определения состояния сосудистых стенок (нарушение эластических свойств, гипертонус, гипотония); исследования состояния позвоночных артерий; диагностика УЗДГ исследует состояние венозного кровотока шеи, головы, верхних и нижних конечностей; УЗДГ дает полную картину состояния артерий и вен верхних и нижних конечностей (проходимость, извитость, стеноз, варикозное расширение, тромбозы и т.п.). УЗДГ рекомендуется проводить пациентам, у которых наблюдаются: гипертоническая болезнь; головные боли; повторяющихся случаи потери сознания; варикозные болезни ног; судороги. В процессе исследования УЗДГ пациент находится в положении лежа, врач с помощью датчика производит исследование в контрольных точках, соответствующих проекции исследуемых сосудов. УЗДГ одинаково информативно как для крупных, так и для мелких сосудов. Исследуется как артериальное, так и венозное кровообращение. Дополнительные факторы, влияющими на линейную скорость кровотока (ЛСК) при УЗДГ сосудов шеи и головного мозга, являются показатели гематокрита, содержания фибриногена и иных показателей, определяющих вязкость крови. Метод позволяет оценивать линейную скорость кровотока (ЛСК) в см/сек в сонных и позвоночных артериях при тяжелой травме мозга, особенно сочетанной с травмой шеи. Исследования УЗДГ сосудов шеи и головного мозга проводят на специальной аппаратуре, применяя датчики с частотой 2–10 МГц. Оценку данных УЗДГ сосудов шеи и головного мозга можно проводить в абсолютных значениях или в сравнении с параметрами аналогичной артерии противоположной стороны. Противопоказаний к использованию УЗДГ сосудов шеи и головного мозга практически нет, за исключением обширных ран мягких тканей в зоне исследования, что препятствует приложению датчика. 8. Позитронно-эмиссионная компьютерная томография (ПЭТ-КТ). Позитронно-эмиссионная томография (ПЭТ) относится к методам ядерной медицины и для получения изображений использует радиофармпрепараты (РФП), меченные позитрон-излучающими ультракороткоживущими радионуклидами ( УКЖР ). Основным доводом в пользу применения УКЖР явилось то обстоятельство, что их применении позволяет уменьшить время исследования и радиационную нагрузку на больного, т.к. большая часть препарата распадается уже во время исследования. Кроме того, многие элементы, имеющие позитрон -излучающие УКЖР, такие как 11C, 13N, 15O (а также 18F, выступающий как аналог водорода ) принимают самое активное участие в большинстве биологических процессов человеческого организма. По сути, методом ПЭТ можно исследовать любую функцию организма. Необходимо только выбрать химическое соединение, критически важное для осуществления этой функции. Химическое соединение, помеченное таким радионуклидом, выбранным из ряда " физиологичных " УКЖР, может быть метаболическим субстратом или одной из важных в биологическом отношении молекул. Эта технология при использовании соответствующих РФП и фармакокинетических моделей, описывающих распределение и метаболизм препарата в тканях, кровяном русле и межтканевом пространстве, позволяет неинвазивно и количественно оценивать ряд физиологических и биохимических процессов. В этом и состоит принципиальное отличие ПЭТ, которую называют «функциональной томографией », от КТ и МРТ, оценивающих структурные изменения тканей. Биохимические процессы нарушаются фактически при всех заболеваниях, и эти изменения обычно предшествуют анатомическим поражениям или распространяются за их пределы. ПЭТ дополняет диагностический процесс информацией о физиологических и метаболических расстройствах в очагах поражения, что существенно уточняет характеристику заболевания. Однако в клинических исследованиях наиболее распространенный РФП- 18F- фтордезоксиглюкоза (ФДГ), используемый для оценки энергетического метаболизма. Причина успеха этого препарата - высокий уровень его накопления в патологических очагах, в первую очередь злокачественных опухолях и метастазах, что сделало ПЭТ с ФДГ незаменимым в диагностике онкологических заболеваний. Очевидный недостаток ПЭТ - бедная анатомически информация изображений, что сильно затрудняет локализацию выявленных патологических очагов . Для преодоления этого несколько лет назад был создан совмещенный ПЭТ /КТ, прибор, позволяющий одновременно проводить два исследования . ПЭТ /КТ программно совмещает изображения этих диагностических модальностей и позволяет на одном срезе получить анатомическое изображение с наложенной на него картой метаболических процессов. Радиофармпрепараты для ПЭТ. Чаще всего в позитронно - эмиссионной томографии используются ультракороткоживущие изотопы -18F, 11C, 13N и 15O, с периодами полураспада 109, 20, 10 и 2 минуты соответственно . Использование УКЖ-изотопов для метки РФП, вводимых пациенту , предоставляет два основных преимущества по сравнению с другими видами радиоизотопной диагностики. Во-первых, метка именно этими изотопами ( в отличие от используемых в ОФЭКТ изотопов 99Tc или 123I) не меняет химических свойств РФП, следовательно, они являются функциональными аналогами естественных метаболитов, и распределение в организме надлежащим образом выбранных РФП адекватно отражает параметры исследуемого биохимического процесса и/или функционального состояния организма. Во- вторых, короткий период полураспада данных изотопов позволяет проводить многократные исследования (в частности, при использовании РФП, меченных 15O - каждые 15 минут). В настоящее время существует множество различных РФП для ПЭТ , что позволяет по праву рассматривать этот метод как инструмент для изучения биологических процессов in vivo . Так, например, аналоги природной глюкозы :18F- фтордезоксиглюкоза (18F- ФДГ ), [1-11C]-D-глюкоза - используются для оценки скорости метаболизма глюкозы , меченная [15O] вода служит для оценки мозгового кровотока, [15O2]– для оценки метаболизма кислорода. [11C]-метил-L-метионин, [11C]-лейцин, [18F]-тирозин, 18F - фторхолин – для определения уровня метаболизма и транспорта аминокислот и синтеза белков , 18F-фтортимидин для оценки скорости пролиферации опухолевых клеток, 18F - фтормизонидазол для выявления тканевой гипоксии . [ β -11С ]-L-3,4-дигидроксифенилаланин ([11С]-L-DOPA), 18F-DOPA и [ О-метил-11C]-раклоприд используются для изучения пре- и постсинаптических процессов в дофаминэргической системе, а (18F)-флюмазенил- в бензодиазепиновой.Таким образом, разнообразие существующих РФП позволяет выбрать оптимальный вариант, в зависимости от целей исследования для наиболее адекватной ПЭТ -методики. В последние годы появились сообщения об успешном применении 18F-холина и 11С-ацетата в исследованиях рака предстательной железы и опухолей мозга, 18F-DOPA для нейроэндокринных и гломусных опухолей , феохромоцитомы, медуллярного рака щитовидной железы, 11С-метионина для опухолей головы и шеи, легких , молочной железы, но этих данных пока недостаточно . Поэтому в клинических исследованиях используется ограниченное количество РФП, а в подавляющем большинстве случаев применяется 18F- ФДГ . Противопоказания общие с другими радионуклидными исследованиями: общее тяжелое состояние больного, трудности транспортировки в лабораторию , невозможность выдержать время исследования ( его продолжительность вместе с подготовкой более двух часов) неподвижно. В силу того , что биологические соединения присутствуют в РФП в ничтожно малых они не имеют побочных действий , не вызывают аллергических реакций и не оказывают фармакологических эффектов. Показания к ПЭТ исследованиям. В европейских странах и США они отличаются , что связано с оплатой ПЭТ исследований страховыми компаниями. Например, в Италии любые ПЭТ исследования покрывает медицинская страховка, а в Германии и России ПЭТ не входит в программу обязательного медицинского страхования. В США, Франции , Великобритании, Швейцарии оплата ПЭТ зависит от заболевания, по поводу которого проводилось исследование . Тем не менее на основании многолетнего опыта и независимо от политики страховых компаний составилось представление, когда применение ПЭТ может принести наибольшую пользу для пациента: опухоли головы и шеи; опухоли неясной локализации (при выявленных отдаленных метастазах); рак легкого; рак молочной железы; рак пищевода и желудка; рак толстой кишки; рак поджелудочной железы; лимфома (болезнь Ходжкина и неходжкинская лимфома ); меланома; опухоли костей и мягких тканей; опухоли мочеполовой системы; опухоли головного мозга; эпилепсия; сосудистые заболевания головного мозга, травмы головного мозга; деменции; дифференциальная диагностика сосудистой деменции от других типов (Альцгеймера, Пика). Принцип позитронно-эмиссионной компьютерной томографии (ПЭТ-КТ) основывается на вводимом через вену радиоактивном индикаторе, который доходит до органов с повышенным обменом веществ – например, к раковым клеткам. Обследование всегда начинается с компьютерной томографии с низкой дозой облучения, за которой следует этап позитронно-эмиссионной компьютерной томографии. Снимки сливаются, т.е. компьютер объединяет снимки, сделанные при КТ и при ПЭТ. В отношении определённых видов рака съёмка может быть произведена во время задержки дыхания, для получения наиболее чёткой картины объекта путём устранения неточностей, возникающих во время дыхания. Перед съёмкой необходимо полежать около получаса, чтобы уравновесить обмен веществ. Инъекция индикаторов производится внутривенно, после чего необходимо отдохнуть ещё около часа. Непосредственно сканирование длится около 25 минут. Профильный материал для студентов лечебного факультета ЭЭГ взрослого человека в норме. ЭЭГ в существенной степени однородна для всего мозга и симметрична. Функциональная и морфологическая неоднородность коры определяет особенности электрической активности различных областей мозга. Пространственная смена типов ЭЭГ отдельных областей мозга происходит постепенно. У большинства (85-90%) здоровых взрослых при закрытых глазах в покое на ЭЭГ регистрируется доминирующий α-ритм (индекс ритма может составлять около 60%) с максимальной амплитудой в затылочных отделах. Электроэнцефалографическое исследование взрослого человека проводится в состоянии пассивного бодрствования, при закрытых глазах. На электроэнцефалограмме в 85-90 процентах случаев доминирует альфа-ритм с правильными зональными различиями, модулированный в веретена амплитудой 50-100 мкВ. В норме на электроэнцефалограмме регистрируется альфа, бета активность. Появление на электроэнцефалограмме взрослого человека медленных ритмов расценивается однозначно как признак патологии. После 60 лет – регресс ЭЭГ. Альфа ритм замедляется, появляется в лобных отведениях. Теряется зональность ритмов. |
