почвоведение ганжара. Учебники и учебные пособия для студентов высших учебных заведений
 Скачать 7.4 Mb. Скачать 7.4 Mb.
|
|
Осадочные породы ■ кварц [fflff Полевые шпаты ^ Слюды Магматические породы 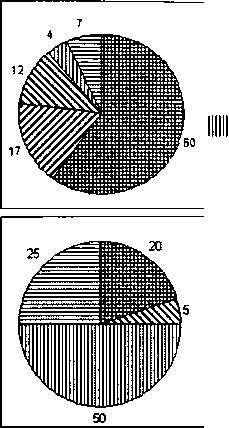 В Полевые шпаты Й2? Амфиболы и лироксены >$$ Слюды Кварц = Прочие Рис. 12.1. Минералогический состав магматических и осадочных пород 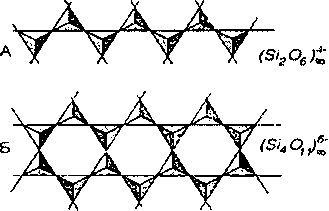 Рис. 12.2. Кремнекислородные радикалы: А — цепочные; Б — ленточные; В — листовые Свойства силикатов, в том числе устойчивость к выветриванию, определяются строением кристалли- ческои решетки, состоящей из кремнекислородных тетраэдров (SiO„)4-. Во всех силикатах каждый атом кремния соединен с четырьмя атомами кислорода, расположенными в вершинах тетраэдра, в центре которого находится атом кремния. Кремнекислородный тетраэдр обладает четырьмя свободными валентными связями, которые могут быть компенсированы присоединением катионов или соединением с другими кремнекислородными тетраэдрами. Тетраэдры, соединяясь через кислородные ионы, могут образовывать различные сочетания, или типы структур: островные (оливин), ленточные (амфиболы), листовые (слюДы), каркасные (поле- ВЬ1е шпаты, кварц) (Рис. 12.2). Если тетра-эдры в структуре располагаются изолированно, соединяясь между собой через положительно заряженные атомы металлов, получается самый простой — островной тип структуры. При соединении тетраэдров через кислородные ионы образуются цепочки, ленты, листы или слои, каркасы. В каркасных структурах часть ионов кремния может замещаться алюминием, при этом образуются алюмосиликаты.  Кварц (Si02). По химической природе кварц — типичный оксид, а по кристаллической структуре его относят к каркасным силикатам. Известны разновидности кварца, имеющие разный цвет и прозрачность: горный хрусталь, аметист, раухтопаз, морин. Кварц весьма стойкий к выветриванию минерал, поэтому он накапливается в осадочных породах и в почвах. Особенно много кварца содержится в песчаных и супесчаных почвах. Обогащен- ность почв кварцем обусловливает пониженное плодородие, из-за его химической инертности, неспособности удерживать влагу и элементы питания. Существуют разновидности кварца вторичного (экзогенного) происхождения: халцедон — скрытокристаллическая разновидность кварца; опал — аморфная разновидность, содержащая воду; гейзерит — гидротермальный опал. Все перечисленные минералы вместе с кварцем объединены в группу свободного кремнезема. Полевые шпаты. Эта наиболее распространенная в литосфере группа минералов имеет каркасный тип кристаллической решетки. В каркасных структурах часть ионов четырехвалентного кремния замещена трехвалентным алюминием, в результате создается комплексная алюмокремниевая группа (поэтому их относят к алюмосиликатам) и возникает свободная валентность кислорода, которая компенсируется ионами калия, натрия и кальция. По химическому составу полевые шпаты подразделяются на три подгруппы: 1) калиево-натриевые полевые шпаты, в состав которых входят K[AlSi3Og] и Na[AlSi308], к этим соединениям относятся ортоклаз, микроклин и др.; 2) натриево-кальциевые полевые шпаты, или плагиоклазы, представляющие собой изоморфные смеси натриевой молекулы — Na[AlSi308] (в чистом виде называется альбит) и кальциевой — Ca[Al2Si208] (в чистом виде называется анортит); 3) фельдшпатиды по химическому составу сходны с полевыми шпатами, но имеют меньшее содержание оксидов кремния, они часто замещают полевые шпаты в основных породах. В зависимости от содержания оксида кремния полевые шпаты подразделяются на кислые, с повышенным содержанием 104 кремнезема (ортоклаз, микроклин, альбит); средние и основные __ с пониженным содержанием (лабрадор, анортит и др.). Полевые шпаты являются менее устойчивыми к выветриванию, по сравнению с кварцем. Среди них наиболее устойчивыми считаются кислые полевые шпаты, содержащиеся в кислых породах (гранит, липарит). Средние и основные, содержащиеся в основных магматических породах (габбро, базальт), менее устойчивы и могут являться источником элементов питания (калия, кальция и др.) для растений. Пироксены и амфиболы. Пироксены и амфиболы занимают в литосфере по массе второе место после полевых шпатов (около 17%). В почвах и осадочных породах они присутствуют в небольших количествах, в связи с низкой устойчивостью к выветриванию. Пироксены относятся к цепочечным силикатам. Типичным представителем является авгит —• породообразующий минерал основных и ультраосновных пород. Амфиболы относятся к ленточным силикатам. Типичным и наиболее распространенным представителем является роговая обманка. Группа слюд. Эта группа минералов имеет листовую, слоистую структуру. В земной коре содержится около 4% слюд. В осадочных породах и почвах — встречаются в небольших количествах. В этой группе минералов часть кремнекислородных тетраэдров заменена на алюмокислородные, поэтому они относятся к алюмосиликатам. Типичными представителями являются мусковит и биотит, в своем составе содержат калий, магний, железо. Слюды более устойчивы к процессам выветривания, по сравнению с амфиболами и пироксенами.
Вторичные минералы содержатся только в осадочных породах и в почвах. Они представлены в основном глинистыми минералами, оксидами железа, алюминия и простыми солями. Глинистые минералы. Минералы этой группы относятся к слоистым алюмосиликатам. Их название связано с тем, что они, как правило, преобладают в составе глин. К глинистым минералам относятся минералы групп каолинита, гидрослюд, монтмориллонита, смешаннослоистых минералов, хлорита. Глинистые минералы обладают рядом общих свойств: 1) высокая дисперсность; 2) по- 105 глотательная, или обменная способность по отношению к катионам; 3) содержат химически связанную воду, которая выделяется при температурах в несколько сотен градусов; 4) имеют слоистое строение, сочетающее тетраэдрические и октаэдрические слои. Различают двух-, трех- и четырехслойные минералы. Минералы группы каолинита. Каолинит Al4(OH)8(Si4O10) — двухслойный минерал с жесткой кристаллической решеткой, состоящей из одного слоя кремнекислородных тетраэдров и одного слоя алюмогидроксильных октаэдров (рис. 12.3). Каолинит не набухает в воде, так как вода не проникает в межплоскостное пространство минерала из-за сильной связи между пакетами. Этот минерал характеризуется узким отношением Si02: А1203 = 2. Он обладает низкой поглотительной способностью (не более 20 мг- экв на 100 г), обусловленной исключительно теми свободными связями, которые имеются на краях элементарных пакетов. К группе каолинита относится минерал галлуазит, отличающийся значительным содержанием межпакетной влаги и более высокой емкостью катионного обмена (40-60 мг-экв на 100 г). Наиболее высокое содержание каолинита — в почвах, формирующихся в условиях субтропических и тропических влажных областей на ферраллитных и аллитных корах выветривания. В почвах умеренных широт его содержание незначительное, за исключением древних кор выветривания. Почвы, содержащие каолинит, характеризуются низкой емкостью катионного обмена, обеднены основаниями, меньше накапливают гумуса, характеризуются пониженным плодородием. 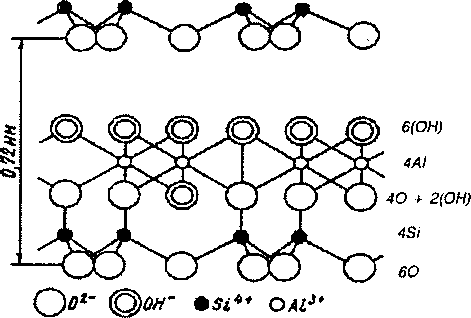 Рис. 12.3. Схема строения кристаллической решетки каолинита 106 Минералы группы гидрослюд (гидробиотит, гидромусковит И др.)* Их еще называют минералами группы иллита. Эти минералы представляют собой трехслойные алюмосиликаты с нерасширяю- щейся решеткой, а поэтому межпакетная вода в них отсутствует. Емкость катионного обмена гидрослюд достигает 45-50 мг- экв на 100 г. Часть кремния в тетраэдрах замещена на алюминий. Образующийся при этом отрицательный заряд компенсируется необменными ионами калия, который прочно связывает пакеты между собой. Гидрослюды характеризуются повышенным содержанием калия (до 6-8%), который частично используется растениями. Представитель гидрослюд — глауконит является агрономической рудой, калийным удобрением, после соответствующей термической обработки. Минералы этой группы широко распространены в осадочных породах и почвах, в том числе в подзолистых, серых лесных и др. К гидрослюдам близок минерал вермикулит, характеризующийся расширяющейся решеткой и очень высокой емкостью катионного обмена (до 100-120 мг-экв на 100 г). Вермикулит ^асто используют как компонент тепличных грунтов. Минералы группы монтмориллонита (монтмориллонит, нонт- ронит, бейделит и др.). Их еще называют минералами группы смектита (Fe, Al)2[Si4O10](OH)2 nH2O, молярное отношение Si02: А1203 = 4. Эта группа минералов имеет трехслойное строение с сильно расширяющейся при увлажнении кристаллической решеткой, при этом они поглощают влагу, сильно набухают и увеличиваются в объеме (рис. 12.4). Отличительной особенностью этих минералов является высокая дисперсность. Разнообразные изоморфные замещения кремния на алюминий, алюминия на железо и магний влекут за собой появление отрицательных зарядов, которые уравновешиваются обменными катионами. Повышенная дисперсность и изоморфные замещения обусловливают высокую емкость катионного обмена — 80-120 мг-экв на 100 г. Минералы группы монтмориллонита чаще содержатся в почвах с нейтральной и щелочной реакцией среды (черноземы, каштановые, солонцы) и практически полностью отсутствуют в субтропических и тропических почвах на ферраллитных и аллит- ных корах выветривания. Много монтмориллонита содержится в слитых почвах. Минералы группы хлорита. Они имеют четырехслойную набухающую решетку. Содержат в своем составе железо, магний. Могут быть как магматического, так и экзогенного происхождения. Име- 107Рис. 12.4. Схема строения кристаллической решетки монтмориллонита. 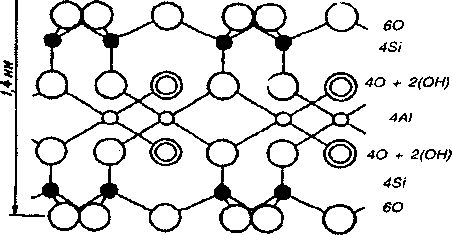 О ©0/г •л4* Ол»* ются данные (Соколова Т.А., 1982), что почвенные хлориты участвуют в формировании гидролитической кислотности почв. Группа смешаннослойных минералов. Смешаннослойные минералы имеют кристаллические решетки, в которых чередуются слои разных минералов: монтмориллонита с иллитом, вермикулита с хлоритом и др. Соответственно составным частям они получают название — иллит-монтмориллонит, вермикулит-хлорит и др. В зависимости от состава и доли участия тех или иных минералов свойства их сильно изменяются. Эта группа минералов наиболее распространена в почвах умеренного и холодного гумидного и арктического поясов, в которых они занимают 30-80% от общего содержания глинистых минералов (Б.П. Градусов, 1976). Минералы гидроксидов и оксидов железа и алюминия. Наибольшее распространение имеют гематит Fe203, гетит Fe203H20, гидрогетит, гиббсит (гидрагелит) А1203-ЗН20. Минералы этих групп встречаются в иллювиальных горизонтах подзолистых, серых лесных почв, почв влажных тропических и субтропических областей (красноземы, ферраллиты и др.). Они образуются путем кристаллизации из аморфных гидратов оксидов железа и алюминия. Минералы этой группы принимают участие в оструктурива- нии почв, в связывании фосфорной кислоты. В условиях кислой реакции среды гидраты оксидов железа и алюминия растворяются и принимают активное участие в процессах почвообразования.Аллофаны. Группа вторичных минералов, состоящая из октаэдров и тетраэдров, но расположенных не систематически, а беспорядочно и поэтому имеющих аморфное строение. Они повышают емкость поглощения, увеличивают гидрофильность, липкость и набухаемость почв. Минералы — соли. Могут быть как вторичными, так и первичными. Наибольшее распространение имеют карбонаты: кальцит — СаС03, доломит — CaC03 MgC03, сода — Na2C03 ЮН20. Среди сульфатов наиболее распространены гипс — CaS042H20, мирабилит — Na2S0410H20, среди хлоридов — галит NaCl. Много солей содержится в засоленных почвах и почвообразующих породах в аридных областях, где они оказывают ведущее влияние на свойства и плодородие почв.
Минералогический состав почв наследуется от почвообразующих пород, является довольно устойчивым во времени и практически не поддается регулированию, за исключением приемов пескования, глинования; химических мелиораций — известкования, гипсования; удаления из почв водорастворимых солей промывками. С минералогическим составом тесно связаны гранулометрический и химический составы почв, физико-механические, а также физические и физико-химические свойства. Очень часто он определяет направленность почвообразовательных процессов и приводит к формированию специфических типов почв, получивших название литогенных, в составе и свойствах которых в меньшей степени проявляется влияние биологического и климатического факторов почвообразования. Минералогический состав оказывает влияние на прочность связи гумусовых веществ с минеральной частью почв и, в целом, на количество накапливающегося гумуса, на емкость катионного обмена, реакцию среды, потенциальный запас элементов питания для растений, на процессы формирования агрономически ценной структуры и поэтому является одним из ведущих факторов, определяющих уровень почвенного плодородия. Глава 13. Химический состав почв и почвообразующих пород
Почва является четырехфазной системой. Она включает твердую, жидкую, газообразную и живую фазы. Каждая фаза имеет специфический химический состав. Твердая фаза автоморфных почв является преобладающей по массе и преимущественно состоит из минеральных — 80-90% и, в меньшей мере, — 10-15% — органических веществ. Минеральная часть почвы в основном состоит из кислорода и кремния. Затем идут в убывающем порядке алюминий и железо, кальций, калий, натрий и магний (табл. 13.1). Эти 8 элементов в сумме составляют около 99% минеральной части почв и почвообразующих пород. Около 1% приходится на все остальные элементы. Среди них повышенное содержание имеют титан, фосфор, марганец, сера и хлор, водород и углерод, которые относятся к макроэлементам. Очень незначительную часть почвы занимают микроэлементы: Си, Zn, Мо, В, РЬ и др. Углерод, азот и, частично, водород, сера и фосфор содержатся в основном в составе органических веществ. Литосфера и почвы имеют близкий химический состав. Однако в составе почв значительно больше содержится углерода и азота, что связано с их биологическим накоплением в составе органических веществ. Несколько больше в почвах, по сравнению с литосферой, содержится кислорода, водорода и кремния и меньше — алюминия, железа, кальция, магния, натрия, калия и других металлов, что связано с процессами выветривания и поч-
|
