Учебники ил и материал их электронных учебников основная литература
 Скачать 94.37 Kb. Скачать 94.37 Kb.
|
|
ЗАКОНСПЕКТИРУЙТЕ ЭТОТ МАТЕРИАЛ И ЗАПОЛНИТЕ ТАБЛИЦЫ, ИСПОЛЬЗУЯ УЧЕБНИКИ ИЛ И МАТЕРИАЛ ИХ ЭЛЕКТРОННЫХ УЧЕБНИКОВ Основная литература: 1. Биохимия : учебник / под ред. Е. С. Северина. - 5-е изд., испр. и доп. - М. : ГЭОТАР-Медиа, 2014. - 768 с. : ил. http://www.studentlibrary.ru Список полезных web-страниц Наглядная биохимия/ Я. Кольман, К.- Г. Рем, - Москва “Мир” 2000 http://www.chem.msu.su/rus/teaching/kolman/index.htm Биохимия: Учеб. для вузов, Под ред. Е.С. Северина., 2003 http://www.biochemistry.ru/biohimija_severina/B5873Content.html Биологическая химия под ред. Е.С. Северина, 2011 г (новая редакция учебника с упражнениями, тестами и задачами для студентов специальности Лечебное дело и Фармация) http://biochemistry.ru/Biologicheskajahimija2011/#/1/ Очень полезный ресурс, в котором представлен хороший лекционный материал http://biokhimija.ru/lekcii-po-biohimii.html ♦ ◊ ♦ Тема: Белки. Белки (протеины) – высокомолекулярные азотсодержащие органические соединения, играют важную роль в построении живой ткани и в осуществлении процессов жизнедеятельности. Особенности структуры и наличие ряда уникальных свойств обеспечивают функционирование белков как одного из основных материальных носителей жизни. Представление о структуре, физико-химических свойствах и биологических функциях белков являются теоретической основой изучения всех последующих разделов биологической химии. Строение и функции белков. Методы качественного и количественного анализа белков. Используя лекции и учебники по биохимии, изучите химический состав, строение, уровни организации белковой молекулы, биологические функции белков, письменно ответьте на вопросы в тетради. Используйте таблицу 1 и рисунок 1. Таблица 1.
ПЕРВИЧНАЯ СТРУКТУРА 1-Й ЭТАП – ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТНОГО СОСТАВА 2-Й ЭТАП – ФРАГМЕНТАЦИЯ ПОЛИПЕПТИДА ПОЛНЫЙ ГИДРОЛИЗ РАЗДЕЛЕНИЕ И ИДЕНТЕФИКАЦИЯ СМЕСИ АМИНОКИСЛОТ МЕТОДОМ ХРОМАТОГРАФИИ ВТОРИЧНАЯ СТРУКТУРА ТРЕТИЧНАЯ СТРУКТУРА ЧЕТВЕРТИЧ-НАЯ СТРУКТУРА РЕНТГЕНОСТРУКТУРНЫЙ АНАЛИЗ, ЭЛЕКТРОННАЯ МИКРОСКОПИЯ ИЗБИРАТЕЛЬНЫЙ ГИДРОЛИЗ ОЛИГОПЕПТИДЫ 3-Й ЭТАП ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ДЕГРАДАЦИЯ ОЛИГОПЕПТИДОВ ПО ЭДМАНУ СОСТАВЛЕНИЕ КАРТ ПЕРЕКРЫВАЮЩИХСЯ ПЕПТИДОВ УСТАНОВЛЕНИЕ УНИКАЛЬНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ВСЕЙ ПОЛИПЕПТИДНОЙ ЦЕПИ Рисунок 1. Графологическая структура «Качественный анализ – установление структуры белка» Обучающие задачиЗадача 1.Будет ли одинаковой интенсивность окраски, полученной в реакции с биуретовым реактивом, для 100 молекул альбумина (Mr 64000 D) и 100 молекул иммуноглобулина G (Mr 175000D)? В чем заключается принцип биуретовой реакции? Ответ. С биуретовым реактивом реагируют пептидные группы белков – образуется хелатный комплекс фиолетового цвета. По сравнению с иммуноглобулинами, альбумин содержит меньше остатков аминокислот, так как имеет меньшую молекулярную массу, следовательно, интенсивность окраски раствора альбумина будет меньше. Задача 2.Подавляющее большинство протеиногенных аминокислот дают синее окрашивание с нингидрином, а пролин и оксипролин – желтое. Объясните это различие, принимая во внимание химизм нингидриновой пробы и особенности структуры протеиногенных аминокислот. Ответ. Нингидрин является специфичным реагентом для -аминокислот, тогда как пролин и оксипролин являются иминокислотами. С -аминокислотами нингидрин реагирует по следующей схеме: нингидрин α - аминокислота 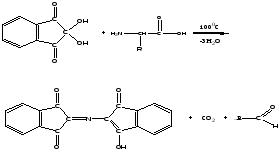 продукт реакции сине-фиолетового цвета альдегид (светопоглощение в области 550-570 нм) Физико-химические свойства белков. При подготовке к занятию следует изучить обратимые и необратимые методы осаждения белков, их физико-химические свойства согласно таблице 2 и рисунку 2. Таблица 2.
БЕЛОК В РАСТВОРЕ СТАБИЛИЗИРУЮТ 2 ФАКТОРА – ЗАРЯД И ГИДРАТНАЯ ОБОЛОЧКА ВЫСАЛИВАНИЕ ДЕНАТУРАЦИЯ МЕТОДЫ ОСАЖДЕНИЯ ДЕГИДРАТАЦИЯ И НЕЙТРАЛИЗАЦИЯ ЗАРЯДА БЕЛКОВЫХ ЧАСТИЦ НАРУШЕНИЕ ВТОРИЧНОЙ, ТРЕТИЧНОЙ И ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ УТРАЧИВАЕТСЯ БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ СОХРАНЯЕТСЯ Рисунок 2. Графологическая структура «Методы осаждения белка» Примеры обучающих задач Задача 1.Сделайте предположение об аминокислотном составе впервые выделенного пептида, принимая во внимание следующие экспериментальные данные: -пептид не обладает электрофоретической подвижностью в щелочной среде (рН 9,8); -при электрофорезе в кислой среде (рН5,6) движется к катоду; -не дает окрашивания при обработке концентрированной азотной кислотой (ксантопротеиновая проба отрицательна). Задача 2.Многие патологические состояния могут сопровождаться изменением рН мочи. Например, для цистита характерна щелочная реакция мочи. Объясните, почему при анализе мочи на содержание белка, в частности при осаждении белков кипячением, необходимо контролировать рН и, если необходимо, доводить его до слабокислой реакции? Задача 3.Белок, синтезируемый in vivo, принимает биологически активную конформацию. В то же время, при синтезе белка in vitro не всегда удается получить функционально активный белок, даже при отсутствии сбоев, ошибок в первичной структуре. Объясните этот феномен. Эталоны ответов на задачи Задача 1.Аминокислотный состав пептида отличается высоким содержанием диаминомонокарбоновых кислот – лизина и аргинина, в то же время, в структуре пептида отсутствуют ароматические и гетероциклические аминокислоты - фенилаланин, тирозин, гистидин и триптофан, дающие положительную ксантопротеиновую реакцию. В частности, тирозин с концентрированной азотной кислотой реагирует по следующей схеме:  желтая окраска желтая окраска оранжевая окраска Задача 2.В сильнокислой и щелочной среде осаждению белков препятствует заряд (отрицательный в кислой и положительный в щелочной). Поэтому, если рН исследуемой мочи не соответствует слабокислой реакции, можно получить ложно отрицательный результат. Задача 3.В живой клетке процесс укладки синтезируемой полипептидной цепи - фолдинг регулируется особыми белками шаперонами. Эти белки контролируют формирование стабильной и биологически активной конформации, предотвращая образование из полипептидной цепи неспецифических клубков и агрегатов, а также участвуют в доставке белков к субклеточным мишеням. Методы выделения и очистки белков Таблица 3.
ХРОМАТОГРАФИЯ'>ГОМОГЕНИЗАЦИЯ БИОЛОГИЧЕСКОГО МАТЕРИАЛА ЭКСТРАКЦИЯ БЕЛКОВ ФРАКЦИОНИРОВАНИЕ БЕЛКОВ ВЫСАЛИВАНИЕ ХРОМАТОГРАФИЯ ЭЛЕКТРОФОРЕЗ КРИСТАЛЛИЗАЦИЯ ИНДИВИДУАЛЬНЫЙ БЕЛОК ОЧИСТКА ОТ НИЗКОМОЛЕКУЛЯРНЫХ ПРИМЕСЕЙ ДИАЛИЗ ГЕЛЬ- ХРОМАТОГРАФИЯ УЛЬТРА- ЦЕНТРИФУГИРОВАНИЕ Рисунок 3. Графологическая структура «Выделение и очистка белков» Примеры обучающих задач Задача 1.При электрофорезе на бумаге белков сыворотки крови больного Р.С. получили следующие результаты: альбумины-48,5%, α1-глобулины-12,6%, α2-глобулины-7,3%, β-глобулины-14,8%, γ-глобулины-16,8%. Выделите изменения, обнаруженные в белковом спектре крови больного и рассчитайте величину белкового коэффициента, если общее содержание белка в крови у данного больного составляло 62 г/л. Задача 2.Необходимо разделить смесь белков, содержащую церрулоплазмин (Mr151000, ИЭТ 4,4), β-лактоглобуллин (молекулярная масса 150000, ИЭТ 6,3) и γ-глобулин (молекулярная масса 37100, ИЭТ 5,2). Предложите методы разделения смеси этих белков. В какой последовательности будут выделяться эти белки из смеси? Эталоны ответов на задачи Задача 1.Снизилось процентное содержание альбуминов (в норме альбумины составляют 55,4-78,9%), повысилось содержание α1- и β-глобулинов. Белковый коэффициент снижен и составляет 0,93. Альбуминов в сыворотке крови больного содержится 30 г/л, глобулинов – 32 г/л. Задача 2.Для отделения β-лактоглобулина, значительно отличающегося по величине молекулярной массы, можно использовать метод гель-фильтрации. Для разделения церрулоплазмина и γ-глобулина, имеющих различные значения ИЭТ, целесообразно использовать электрофорез. |
