Вариант 8 (4) Контрольная работа 1. Вопервых, некоторые одноосновные кислоты (HF, hcl, hbr, hi, и hio3) формально могут образовывать кислые соли типа KHF2, P4RHCl2, NaH(IO3)2 и т п.
 Скачать 25.25 Kb. Скачать 25.25 Kb.
|
|
Вариант 8 Приведите три формулы кислот, которые могут образовывать кислые соли, и укажите их названия. Во-первых, некоторые одноосновные кислоты (HF, HCl, HBr, HI, и HIO3) формально могут образовывать кислые соли типа K[HF2], [P4R][HCl2], Na[H(IO3)2] и т.п., в анионе присутствует водородная связь. Во-вторых, не всякая одноосновная кислота содержит один атом водорода. Например, H3PO2, H2SO5 - одноосновные. Следует уточнить - один атом водорода, связанный с атомом кислорода и способный отщепляться в виде протона. 2. Приведите формулы солей, которые могут образоваться при взаимодействии оксида серы (IV) с гидроксидом натрия, и укажите их названия. Реакция оксида серы (iv) и гидроксида натрия SO2 + 2NaOH → Na2SO3 + H2O 3. Расшифруйте схему превращений HNO3 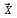 NH4NO3 NH4NO3  NH3, приведите уравнения реакций и назовите вещества Х и Y. NH3, приведите уравнения реакций и назовите вещества Х и Y.HNO3(разб. ) + NH3 = NH4NO3 NH4NO3 + NaOH(конц. ) = NaNO3 + NH3 + H2O 4NH3 + 5O2 = 4NO + 6H2O Условия :800°C, кат. Pt/Rh 2NO + O2 = 2NO2 H2O + 2NO2 = HNO2 + HNO3 Решение: HNO3+NH3=NH4NO3 NH4NO3+KOH=KNO3+NH3+HOH 2NH3+O2=2NO+3H2 1)4 HNO3 = 2 H2O + 4 NO2 + O2 2 NH4NO3 = 4 H2O + 2 N2 + O2 4 HNO3 = 2 H2O + 4 NO2 + O2 2)2 NH4NO3 = 4 H2O + 2 N2 + O2 2 NH3 = 3 H2 + N2 2 NO = N2 + O2 2 NO2 = 2 NO + O2 Дальше по идеи должен быть HNO3 4 HNO3 = 2 H2O + 4 NO2 + O2 2 Ca(NO3)2 = 2 CaO + 4 NO2 + O2 4. Составить реакции, с помощью которых можно осуществить превращения: олово 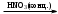 Х1 Х1 Х2 Х2 Х3 Х3 Х4 Х4оловоHNO3 конХ1 KOH Х2 HCL Х3 H2O Х4 |
