Вопросы к коллоквиуму потенциометрические методы анализа
 Скачать 262.66 Kb. Скачать 262.66 Kb.
|
|
ВОПРОСЫ К КОЛЛОКВИУМУ ПОТЕНЦИОМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА 1. Начертите схему электрохимической цепи для измерения фторид-ионов с использованием фторид-селективного электрода. 2. Почему большинство металлических электродов не могут быть использованы в качестве индикаторных в потенциометрии? 3. Электроды из каких металлов можно использовать для измерения окислительно-восстановительных потенциалов? 4. С использованием каких металлических электродов можно проводить потенциометрическое титрование с использованием реакций окисления -восстановления? 5. Для определения восстановителей используется потенциометрическое титрование окислителями. Какие электроды можно использовать для измерений (индикаторные и электроды сравнения)? Приведите вид возможных кривых титрования. 6. Для определения окислителей используется потенциометрическое титрование с восстановителями. Какие электроды можно использовать для этих целей (индикаторные и электроды сравнения)? Приведите вид возможных кривых титрования. 7 Что характеризует коэффициент селективности ионоселективного электрода? Что означает КK+/Na+=1*10-3? 8. Почему для прямых ионометрических определений необходимо создать постоянную ионную силу растворов? Каким образом это осуществляют? 9. Начертите вид градуировочных кривых для катионселективного электрода: а) в отсутствии мешающих веществ; б) в присутствии мешающих веществ. 10. Начертите вид градуировочных кривых для анионселективного электрода: а) в отсутствии мешающих веществ, б) в присутствии мешающих веществ. 11. Объясните, почему при определении фторид-ионов с использованием фторид-селективного электрода, гидроксид-ионы мешают определению, а хлорид-ионы не мешают? 12. Чем обусловлена высокая селективность твердых кристаллических мембранных электродов? 13. Почему при использовании прямых ионометрических измерений необходимо регулировать рН растворов? Каким образом это осуществляют? 14. При определении Сu+2 в воде медь-селективным электродом к исследуемой пробе в процессе определения добавляют раствор, содержащий: ацетат натрия, уксусную кислоту, фторид калия, нитрат калия и формальдегид. Объясните назначение этих компонентов. 15. Начертите градуировочные графики для катионселективного электрода при различной ионной силе раствора (0,1 М; 0,5 М; 1,0 М; 2,0 М). 16. Начертите градуировочные графики для анионселективного электрода при различной ионной силе раствора (0,1 М; 0,5 М; 1,0 М; 2,0 М). 17. Какие основные моменты необходимо учесть при подготовке пробы для определения концентрации фторид-ионов с использованием фторид-селективного электрода? 18. Для получения данных, необходимых при построении градуировочного графика для фторид-селективного электрода, "забыли" создать постоянную ионную силу раствора. Каков должен быть вид полученной градуировочной зависимости EF- от -lg CF- ? 19. При измерениях с калий-селективным электродом были получены следующие значения ЭДС: 44 мВ для стандартного раствора с концентрацией 100 мг/л калия и 5 мВ для раствора с концентрацией 5 мг/л. Определите крутизну электродной функции для этого электрода. 20. Оцените коэффициент селективности для иодид-селективного электрода на основе иодида серебра КI-/Cl- и КI-/Br- 21. Какие из катионов должны мешать определениям с хлорид-селективным электродом на основе хлорида серебра? 22. Для Ag -селективного электрода для стандартных растворов с концентрациями ионов серебра 100 и 10 мг/л получены значения ЭДС равные соответственно 350,2 и 293,0 мВ. Определите крутизну электродной функции. ВОЛЬТАМПЕРОМЕТРНЯ И КЛАССИЧЕСКАЯ ПОЛЯРОГРАФИЯ 1. Каковы особенности ячейки для вольтамерометрии и чем они обусловлены? 2. Объясните, почему вещество, участвующее в электродной реакции, называют в полярографии деполяризатором? 3. Почему величина Е1/2 характеризует природу определяемого вещества? 4. От каких факторов зависит наклон полярограммы? 5. Оцените какова должна быть величина ΔЕ=Е1-Е2, если электродный процесс обратим и в нем участвует два электрона. Оцените степень превращения окисленной формы в востановаленную при Е2 99%, при Е1 1%. 6. Почему при регистрации вольтамперограммы необходима высокая концентрация индифферентного электролита? Что означает термин "индифферентный"? 7. При каких условиях предельный ток является диффузионным? 8. Каковы отличительные признаки диффузионного тока? 9. Почему метод классической полярографии не позволяет определять концентрации веществ ниже 10-5 М? 10. Оцените какова должна быть величина ΔЕ=Е1/2-E1 мВ (Е1-начало площадки предельного тока) на классической полярограмме, если электродный процесс обратим и в нем участвует один электрон. Степень превращения окисленной формы в восстановленную при Е1 соответственно 99%. 11. Оцените какова должна быть величина ΔЕ=Е1-E1/2 мВ (E1-начало подъема поляризационной волны) на классической полярограмме, если электродный процесс обратим и в нем участвует один электрон. Степень превращения окисленной формы в восстановленную при Е1 соответственно 1%. 12. Оцените какова должна быть величина ΔЕ=Е1-E1/2 мВ (Е1-начало подъема поляризационной волны) на классической полярограмме, если электродный процесс обратим и в нем участвуют два электрона. 13. Объясните, какие из перечисленных ниже органических соединений могут быть определены методом классической полярографии: предельные углеводороды, углеводороды с сопряженными двойными и тройными связями, пероксиды, меркаптаны. 14. Объясните, какие из перечисленных ниже органических соединений могут быть определены методом классической полярографии: альдегиды, нитро-соединения, амины, фенолы. 15. Потенциалы полуволн веществ А, В и С на одном и том же фоне равны соответственно: -0,30; -0,40 и -0,70 В. Начертите полярограммы растворов, содержащих смесь этих веществ в сравнимых концентрациях. 16. Потенциалы полуволн веществ А, В и С на одном и том же фоне равны соответственно: -0,42; -0,75; -1,10 В. Начертите полярограммы растворов, содержащих смесь этих веществ в сравнимых концентрациях. 17. Оцените соотношение высот волн для полярограмм, полученных для веществ А и В, если потенциалы полуволн их соответственно равны -0,65 и -0,95 В, концентрации их одинаковы, электродные процессы обратимы и число электронов соответственно равны 2 и 1. 18. При использовании каких предельных токов необходимо использовать термостатированные ячейки при полярографировании? Ответ поясните. 19. Полярографическим методом определяют вещества молекулярного типа. Нужен ли в этом случае фоновый (индифферентный) электролит и каково его назначение? 20. При полярографическом определении низких концентраций веществ с Е1/2 отрицательнее -0,4 В, необходимо удалять растворенный кислород из раствора. Почему это необходимо делать? 21. Проведению полярографических определений часто мешает растворенный кислород. Объясните почему. Каким образом устранить его мешающее действие? 22. Почему при количественных полярографических определениях необходимо проводить градуировку аналитического сигнала? 23. В каких случаях при количественных полярографических определениях необходимо использовать метод стандартных добавок? 24. Выведите уравнения для количественных полярографических определений с использованием метода добавок (обозначения: V0 - объем пробы; Сст. -концентрация определяемого вещества в стандартном растворе; VCT. - объем стандарта; Сх - концентрация определяемого вещества в пробе; hx и hCT -высоты волн для пробы исследуемого раствора и раствора после введения добавки). 25. Полярографическим методом определяют примесь нитробензола в бензоле. Можно ли при определениях не вводить в полярографируемый раствор индифферентный электролит, а использовать в качестве фона матрицу объекта -бензол? КУЛОНОМЕТРИЯ 1. Почему и при прямых и при косвенных кулонометрических определениях необходим 100%-ный выход по току? 2. Чем отличается ячейка для кулонометрических определений от полярографической ячейки? 3. Почему при избытке вспомогательного реагента процесс получения электрогенерированного кулонометрического титранта протекает со 100%-ным выходом по току? 4. Напишите реакции, протекающие при генерировании титрантов для кулонометрического титрования кислоты основанием. 5. Начертите кривую кулонометрического титрования слабой кислоты электрогенерированными ОН-ионами (способ определения окончания титрования - потенциометрический, индикаторный электрод - стеклянный). 6. Начертите кривую кулонометрического титрования слабого основания электрогенерированными Н+-ионами (способ индикации потенциометрический, индикаторный электрод - стеклянный). 7. Восстановитель (А) титруется окислителем (В) кулонометрически по реакции: А + В ↔ С + Д. Генерируемый кулонометрический титрант получают окислением вспомогательного компонента С ( С - n*е- → В ) на рабочем электроде. Из какого материала следует изготовить генераторный электрод? Начертите форму кривой кулонометрического титрования, если использовать потенциометрический способ определения завершения титрования (выбрать индикаторный электрод).  На рисунке приведена вольтамперная кривая, полученная на рабочем (генераторном) электроде для некоторой концентрации вспомогательного компонента, из которого генерируют титрант. Какие значения тока электролиза можно использовать для получения титранта. 9. Какого вида получится кривая кулонометрического титрования мышьяка (Ш) генерируемым иодом, если окончание титрования устанавливается по диффузионному току восстановления иода? 10. Какие параметры поддерживаются постоянными при кулонометрическом титровании с амперометрической фиксацией конечной точки титрования? 11. Какие величины используются для определения количества электричества, затраченного на генерирование титранта? 12. Какие факторы влияют на воспроизводимость определения при использовании кулонометрического титрования? 13. Каковы преимущества кулонометрического титрования по сравнению с амперометрическим и потенциометрическим титрованием? 14. С какой целью в прямой потенциостатической кулонометрии потенциал рабочего электрода поддерживается постоянным? 15. Изменением какого параметра можно менять скорость кулонометрического титрования? Амперометрическое титрование 1.  На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 2.  На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 3.  На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 4.  На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 5. 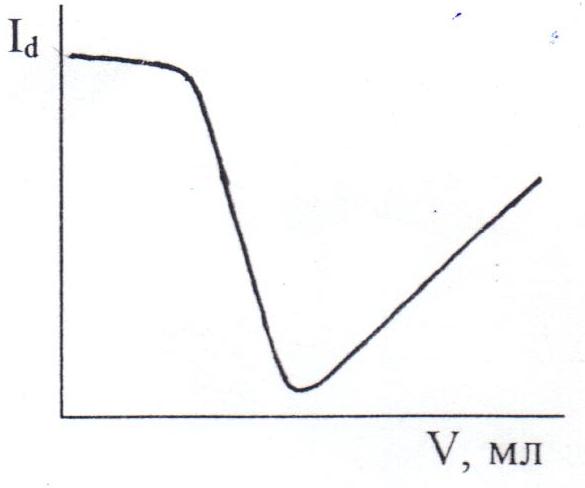 На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 6. 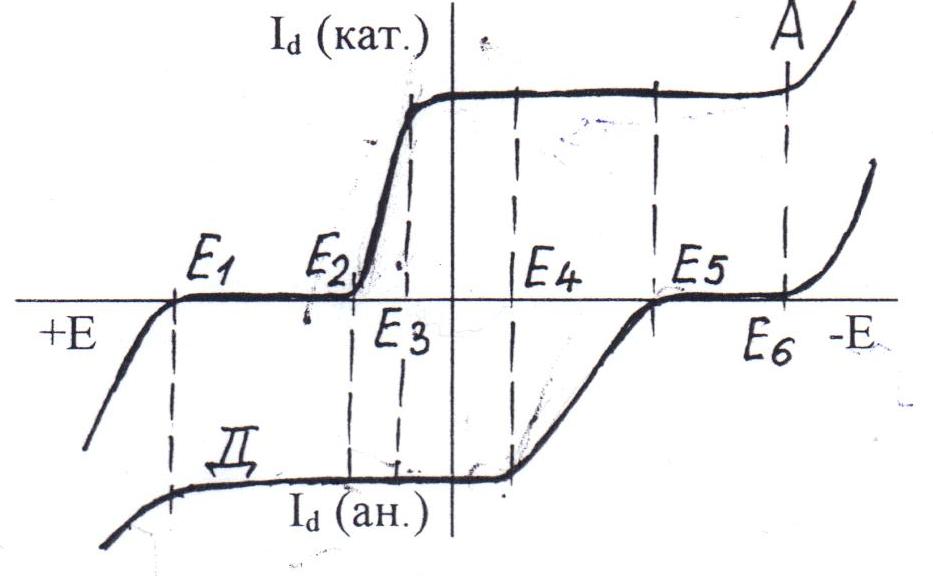 На рисунке приведены кривые электроактивных компонентов реакции, протекающей по схеме: А + В = С + Д. В какой области потенциалов индикаторного электрода можно осуществить титрование? Начертите схемы возможных кривых амперометрического титрования. 7. 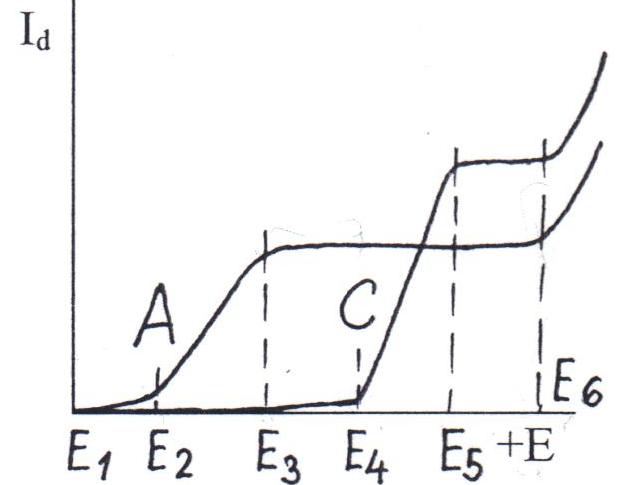 На рисунке приведены схемы вольтамперных кривых электроактивных компонентов реакции: А + В = С + Д. В какой области потенциалов индикаторного электрода можно осуществить титрование? Начертите возможные кривые амперометрического титрования. 8. 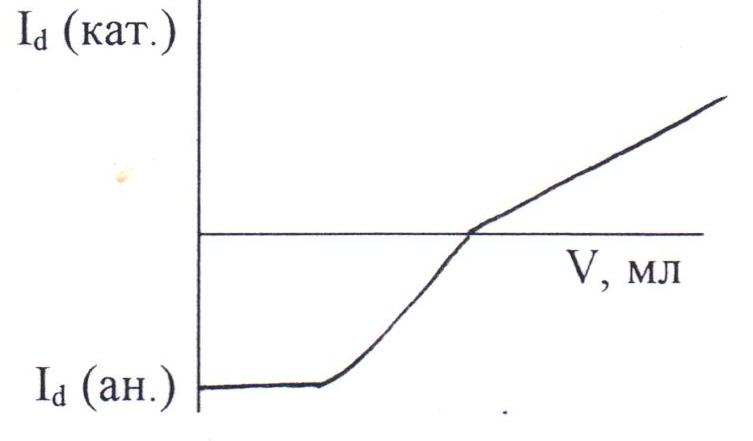 На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 9.  На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 10.  На рисунке приведена кривая амперометрического титрования смеси веществ. Какое минимальное число компонентов титровали? Какие из компонентов реакции электроактивны? Начертите схемы вольтамперных кривых этих компонентов. 11.  На рисунке приведены схемы вольтамперных кривых электроактивных компонентов реакции: А + В = [АВ]. В какой области потенциалов индикаторного электрода можно осуществить титрование? Начертите возможные кривые амперометрического титрования. 12.  На рис. Приведены кривые амперометрического титрования одних и тех же проб в одних и тех же условиях с использованием реакции, протекающей по схеме. А + В = АВ ↓. Объясните, почему может меняться наклон участка кривой титрования (1,2,3,4 - последовательно титруемые пробы). 13. Амперометрическое титрование вещества А по току окисления этого компонента осуществляли одним и тем же титрантом Т, использовав: 1) С(Т) = С(А) и 2) С(Т) = 20*С(А). Объясните, чем будут различаться кривые амперометрического титрования. 14. Возможно ли осуществить амперометрическое титрование, если: определяемое вещество (является примесью) и основной компонент объекта анализа дают однородную электродную реакцию, но с титрантом взаимодействует только определяемое вещество? Ответ обоснуйте. 15. Поясните, можно или нельзя осуществить амперометрическое титрование при потенциале индикаторного электрода равного Ею электроактивного вещества. 16. Потенциалы полуволн определяемого вещества и титранта (на одном и том же фоне), соответственно равны -1.10 и -1.45 В. Фон начинает разряжаться при потенциале -2,0 В. Какие значения потенциалов индикаторного электрода (какого?) можно выбрать для амперометрического титрования? Начертите схемы возможных кривых титрования. 17. Для амперометрического титрования ионов Ва+2 используют их осаждение в виде хромата (Ва+2 + СгО4-2 = ↓ ВаСгО4) С применением какого индикаторного электрода можно выполнить определение? Изобразите вид кривой амперометрического титрования. 18. При амперометрическом определении Рb+2 используют их осаждение в виде сульфата (Pb+2 + SO4-2 = ↓ PbS04 ). Какой индикаторный электрод следует выбрать для амперометрического титрования? Начертите схемы вольтамперных кривых и кривой титрования. 19. Амперометрическое определение I- ионов проводят с использованием реакции: I- + Ag+ = ↓AgI. Какой индикаторный электрод можно использовать для этого? Изобразите вольтамперную кривую электроактивного компонента и кривую титрования. 20. Концентрацию Fe+2 определяют амперометрическим титрованием, используя их окисление дихроматом калия ( фон - 2М H2S04). Какой индикаторный электрод следует использовать в этом случае? Начертите схемы вольтамперных кривых и кривой титрования. 21. В растворе находятся два определяемых вещества ( А и В ), взаимодействующие с одним и тем же титрантом ( С ) последовательно. При выбранном потенциале индикаторного электрода один из определяемых компонентов и титрант дают однородную электродную реакцию. Начертите соответствующие вольтамперные кривые и возможные кривые амперометрического титрования. 22. В растворе находятся два определяемых вещества А и В, последовательно реагирующие с титрантом С. При выбранном потенциале индикаторного электрода электрохимически активными являются: одно из определяемых веществ и титрант, вступающие в разнородные электродные реакции. Изобразите схемы вольтамперных кривых и возможные кривые амперометрического титрования. |
