химия. Задание Вычислите относительную молекулярную массу карбоната натрия, определите массовую долю кислорода в данном веществе. Ответ Mr(Na2CO3) 2Ar(Na) Ar( c ) 3Ar(O) 22312316 106 гмоль W(O) 316100106 45. 28 Задание 2
 Скачать 69.56 Kb. Скачать 69.56 Kb.
|
|
Задание 1. Вычислите относительную молекулярную массу карбоната натрия, определите массовую долю кислорода в данном веществе. Ответ: Mr(Na2CO3) = 2*Ar(Na) + Ar( C ) + 3*Ar(O) = 2*23+12+3*16 = 106 г/моль W(O) = 3*16*100/106 = 45.28% Задание 2. Выпишите в строчку знаки химических элементов с порядковыми номерами 3-7. Подчеркните наиболее ярко выраженный неметалл. Составьте типичные формы соединений для химических элементов с порядковыми номерами 3 и 7. Отметьте характер (основной или кислотный) их оксидов и гидроксидов. Li Be B C N-неметалл Li2O - основный оксид LiOH - высший гидроксид, основание N2O5 - высший оксид, кислотный HNO3 - кислородсодержащая кислота NH3 - летучее соединение Задание 3. Предложенные вещества разделите на 4 группы в соответствии с видами химической связи: 1) Ионная = NaNO3, CaO, AgCI, Na3PO4, CaS 2) Ковалентная неполярная = Si, P, Cl2, 3) Металлическая = Fe, Cu, 4) Ковалентная полярная = SO3, CH4, C6H6, HNO3, C2H5OH Задание 4. Закончите уравнения практически осуществимых реакций, назовите продукты реакции: а) CaO + H2O = Ca(OH)2 гидроксид кальция б) K2O + H2O = 2KOH гидроксид калия в) Li + H2O = LiOH гидроксид лития г) Cu + H2O = не реагирует с водой д) SO2 + H2O = 2SO2 + 2H2O + O2 = 2H2SO4 сернистая кислота Задание 5. Дайте классификацию химическим реакциям, уравнения которых приведены ниже: 1) 2KMnO4 → K2MnO4 + MnO2 + O2 термохимическое разложение 2) NH3 + HCl → NH4Cl соединение 3) Fe + CuCl2 → Cu + FeCl2 замещение 4) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O реакция обмена 5) NaOH + HCl → NaCl + H2O реакция обмена Задание 6. Определите среду водного раствора соли для следующих веществ: Сульфид калия – K2S щелочная, бромид алюминия –AlBr3 кислая хлорид лития – LiCl нейтральная сульфат калия – K2SO4 нейтральная сульфит натрия – Na2SO3 щелочная сульфат аммония – (NH4)2SO4 кислая Задание 7. Перечислите методы предупреждения металлических изделий от коррозии. 1.Электрохимические – метод протектора, катодная зашита, анодная защита. 2.Неэлектрохимическая – легирование, защитные покрытия, изменение свойств коррозийной среды, рациональное конструирование изделий. Задание 8. Из предлагаемых веществ найдите изомеры: = 135 и 246 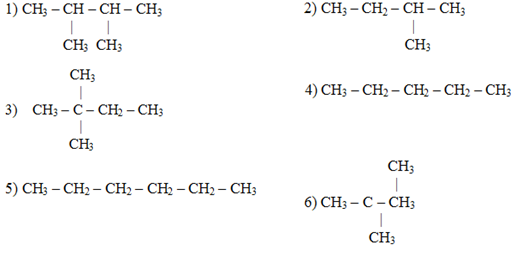 Задание 9. Какие реакции характерны для класса: а) алканы; замещение CH4 + Cl2 = CH3Cl + HCl б) алкены. присоединение C2H4 + Cl2 = C2H4Cl2 Задание 10. Маргарин получают путем: г) гидрирования жидких жиров Задание 11. С помощью, каких реакций можно распознать белки? а) ксантопротеиновая — при действии концентрированной азотной кислоты на раствор белка выпадает ярко-желтый осадок. б) биуретовая — при действии раствора щелочи в присутствии сульфата меди (II) на раствор белка появляется сине-фиолетовое окрашивание раствора. Задание 12. Заполните таблицу
|
