Химия. химия11. Закон ВантГоффа. Осмотическое давление плазмы крови. Онкотическое давление
 Скачать 0.57 Mb. Скачать 0.57 Mb.
|
|
1. Осмос. Осмотическое давление. Закон Вант-Гоффа. Осмотическое давление плазмы крови. Онкотическое давление. Осмос.В животных и растительных организмах, а также в экспериментальных исследованиях существуют и применяются полупроницаемые перегородки — мембраны, разделяющие растворитель и раствор или растворы различной концентрации. Мембраны различают по составу, структуре, размеру пор, отношению к различным растворителям. Они могут быть животного (например, мочевой пузырь), растительного (оболочка клетки) и искусственного происхождения (пленки из целлофана, коллодия). Некоторые из них проницаемы только для растворенного вещества, другие - только для молекул растворителя. Например, глиняная мембрана, содержащая в порах соль Сu2[Fe(CN)6], проницаема только для молекул воды. Именно мембраны последнего типа будут рассмотрены здесь. При наличии мембран в растворах наблюдают явление осмоса. Осмосом называют преимущественно одностороннее проникновение молекул растворителя (диффузию) через полупроницаемую мембрану из растворителя в раствор или из раствора с меньшей концентрацией в раствор с большей концентрацие (рис. 1). 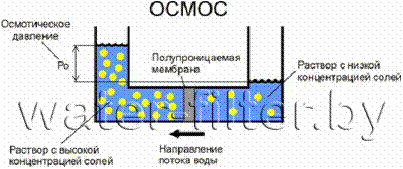 Рис.1. Возникновение осмоса. Необходимым условием возникновения осмоса является наличие растворителя и раствора или двух растворов различной концентрации, разделенных полупроницаемой мембраной. Пусть, например, вода и водный раствор глюкозы разделены мембраной перепонкой из свиного мочевого пузыря, проницаемой только для молекул воды (рис. 2 а). Тогда будет наблюдаться переход воды в раствор и через некоторое время свиной пузырь вздувается. Точнее говоря, вода диффундирует через мембрану в обоих направлениях. Но в раствор по градиенту химического потенциала в соответствии с законом Фика переходит больше молекул воды, чем в обратном направлении, так как концентрация воды в растворе меньше. Аналогично протекает процесс, если полупроницаемой мембраной разделены два водных раствора глюкозы различной концентрации (рис. 2 б). В этом случае наблюдается переход воды из менее концентрированного раствора в концентрированный также в направлении падения химического потенциала. 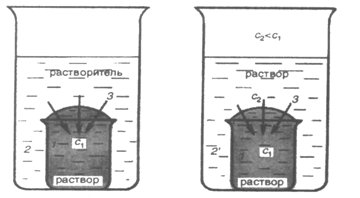 Рис. 2. Осмос в системе растворитель – раствор (а) и в системе раствор – раствор (б). 1 – водный раствор глюкозы (концентрация с1; 2 – чистый растворитель (вода); 2’ – водный раствор глюкозы (концентрация с2); 3 – мембрана. С точки зрения термодинамики движущей силой осмоса является стремление системы к выравниванию концентраций; так как при этом энтропия системы возрастает (ΔS>0), поскольку система переходит в менее упорядоченное состояние, энергия Гиббса системы G соответственно уменьшается, химические потенциалы выравниваются. Поэтому осмос — самопроизвольный процесс. Иллюстрацией, поясняющей связь механизма осмоса с изменением давления пара над раствором, может служить простой опыт (рис. 3). Если в закрытый стеклянный сосуд поместить стакан 1 с чистым растворителем и стакан 2 с раствором какого-либо нелетучего вещества (уровни жидкостей в сосудах 1 и 2 одинаковы), то через некоторое время уровень жидкости в стакане 1 понизится, а уровень раствора в стакане 2 повысится. В этом случае происходит переход растворителя из стакана 1 в стакан 2, что обусловлено (закон Рауля) более низким давлением пара растворителя над раствором (стакан 1), чем над чистым растворителем (стакан 2). 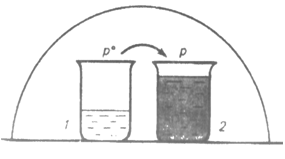 Рис.3. Механизм осмоса. Таким образом, воздушное пространство между растворителем и раствором выполняет роль полупроницаемой мембраны. Осмотическое давление. Наполним сосуд 2 (рис. 4 а) с полупроницаемыми стенками водным раствором глюкозы и поместим в сосуд 3 с водой так, чтобы уровни жидкостей в сосудах 3 и 2 совпадали. В результате осмоса объем раствора в сосуде 2 увеличивается, и уровень жидкости в сосуде 2 постепенно повышается. При этом создается препятствующее осмосу дополнительное гидростатическое давление ргидр столба жидкости высотой h. При некоторой высоте hмакс гидростатическое давление достигает такого значения, при котором осмос прекратится, т. е. наступит осмотическое равновесие. Дополнительное гидростатическое давление столба жидкости можно рассчитать по формуле: рr = hρg где pr - гидростатическое давление (дополнительное), Н/м2; h - высота столба жидкости, м; ρ — плотность жидкости, кг/м3; g - ускорение силы тяжести, равное 9,8 м/с2. 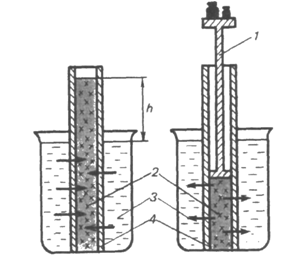 а) б) Рис. 4. Принцип действия осмотической ячейки. а) – гидростатическое давление, создаваемое столбом жидкости; б) – гидравлическое давление, создаваемое поршнем; 1 – поршень; 2 – сосуд с раствором; 3 – сосуд с растворителем; 4 – мембрана; Х – молекулы растворенного вещества. Гидростатическое давление столба жидкости при осмотическом равновесии определяет осмотическое давление раствора. Осмотическое давление можно измерить и другим способом. Допустим, что в сосуд 2 с раствором (рис. 4 б) вставлен запирающий поршень 1. В результате осмоса объем раствора в сосуде 2 увеличивается и поршень 1 поднимается вверх. Чтобы прекратить осмос, необходимо приложить к раствору внешнюю силу. Осмотическим давлением называют величину, измеряемую минимальным гидравлическим давлением, которое нужно приложить к раствору, чтобы осмос прекратился. Закон осмотического давления. Вант-Гофф предложил эмпирическое уравнение для расчета осмотического давления разбавленных растворов неэлектролитов: π = c(X)RT, (1.1) где π — осмотическое давление, кПа; с(Х) — молярная концентрация, моль/л; R — универсальная газовая постоянная, равная 8.31кПа • л/(моль•К); Т — абсолютная температура К°. Хотя закон Вант-Гоффа был установлен на основе экспериментальных данных, он может быть выведен из условий термодинамического равновесия при ΔG = 0. Поэтому этот закон следует рассматривать как следствие 2-го начала термодинамики. Выражение закона Вант-Гоффа аналогично уравнению Клапейрона – Менделеева для идеальных газов, однако эти уравнения описывают разные процессы. В растворах электролитов количество частиц в единице объема раствора больше, так как каждая молекула диссоциирует на определенное число ионов. Потому и осмотическое давление растворов электролитов значительно больше, чем растворов неэлектролитов той же концентрации. Формула для расчета осмотического давления растворов электролитов имеет следующий вид π = i c(X)RT, (1.2) где i – изотонический коэффициент Вант-Гоффа, зависит от степени диссоциации электролита α и числа ионов β, на которые диссоциирует электролит: i = 1 + α (β – 1), (1.3) Как следует из формулы, коэффициент i всегда больше единицы, отсюда и осмотическое давление раствора электролита больше, чем неэлектролита. Осмотическое давление плазмы крови. Онкотическое давление. Осмотическое давление плазмы крови человека характеризуется достаточным постоянством. Оно равно 7,7 атм. Такое высокое осмотическое давление крови обусловлено наличием в ней большого числа ионов, низкомолекулярных и высокомолекулярных соединений. Часть осмотического давления крови, обусловленная высокомолекулярными соединениями, главным образом белками (альбуминами, глобулинами), называется онкотическим давлением. Онкотическое давление составляет 0,5% осмотического давления и равно 0,035-0,039 атм. 2. Закон Рауля. Зависимость температуры замерзания и кипения от концентрации растворов и природы растворителя. Криометрия и эбулиометрия. Закон Рауля. Французский химик Ф. М. Рауль (1830 — 1901) первым провел измерения, которые позволили сформулировать законы, описывающие влияние растворенного вещества на физические свойства растворителя. Эти законы, называемые законами Рауля, могут быть выведены на основе 2-го начала термодинамики из условия термодинамического равновесия ΔG = 0 для физических процессов. Также используют молекулярно-кинетические соображения, приводящие к этим законам. Если в замкнутый сосуд поместить чистый растворитель, например воду, то в этой системе будут протекать два процесса: испарение молекул воды с поверхности жидкости и обратный процесс — конденсация молекул из газовой фазы на поверхности жидкости. Через некоторое время в системе установится динамическое равновесие (ΔG = 0), т. е. такое состояние системы, когда число частиц, испаряющихся с поверхности жидкости за единицу времени, равно числу частиц, переходящих в жидкость из газовой среды. Пар, находящийся в равновесии с жидкостью, называют насыщенным. Давление такого пара р° называют давлением или упругостью насыщенного пара чистого растворителя. При данной температуре давление насыщенного пара чистого растворителя — величина постоянная и является термодинамической характеристикой растворителя. При повышении температуры давление насыщенного пара над растворителем возрастает в соответствии с принципом Ле Шателье, так как испарение — процесс эндотермический (ΔНисп > 0). Каково будет давление насыщенного пара, если в летучий растворитель (спирт, вода и т.д.) внести нелетучее растворяемое вещество, например сахарозу или NaCl. Концентрация растворителя в образовавшемся растворе уменьшится, а следовательно, уменьшится число частиц растворителя, переходящих в газовую фазу, соответственно уменьшится химический потенциал растворителя. А это означает, что давление насыщенного пара над раствором нелетучего вещества должно стать меньше, чем над чистым растворителем: чем концентрированнее раствор, тем ниже давление пара растворителя над раствором. В 1886 г. Рауль сформулировал закон: давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально молярной доле растворителя: где р — давление пара над раствором, Па; КР — константа Рауля, Па; х(Х1) —молярная доля растворителя Х1 равная: где n(X1) —количество вещества растворителя, моль; n(X2) — количество растворенного вещества, моль. В предельном случае, когда молярная доля растворителя x(X1) = 1, коэффициент пропорциональности Кр численно равен давлению пара чистого растворителя р°. Уравнение (2.1) примет следующий вид: C другой стороны, где х(Х2) -молярная доля растворенного вещества X2. Если это выражение подставить в уравнение (2.2), после преобразования получают 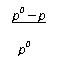 = х(Х2). (2.3) = х(Х2). (2.3)где р° давление пара над чистым растворителем, Па; р — давление пара растворителя над раствором нелетучего вещества, Па; р0 — р абсолютное понижение давления пара над раствором, Па; 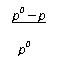 - относительное понижение давления пара над раствором. Уравнение (2.3) отражает другую, более часто применяемую формулировку закона Рауля: относительное понижение давления насыщенного пара растворителя над раствором нелетучего неэлектролита равно молярной доле растворенного вещества. Закон Рауля точно соблюдается только для идеальных растворов и приближенно для разбавленных реальных растворов: чем разбавленнее раствор, тем более он приближается к идеальному. Понижение температуры замерзания и повышение температуры кипения растворов. Криометрия и эбулиометрия. Прямыми следствиями понижения давления пара над раствором являются изменения температуры замерзания ΔТз и кипения растворов ΔТк по сравнению со значениями этих величин для чистого растворителя. Соотношения между этими величинами также вытекают из 2-го начала термодинамики. Температурой кипения жидкости является температура, при которой давление ее паров становится равным внешнему давлению (так, при 101,3 кПа температура кипения воды равна 100°С). Температурой замерзания (кристаллизации) жидкости является температура, при которой давление пара над жидкостью равно давлению пара над твердой фазой. Если обозначить температуры замерзания и кипения раствора Тз и Тк , а эти же величины для растворителя Тзº и Ткº , то получают: Эффекты повышения температуры кипения и понижения температуры замерзания растворов могут качественно быть объяснены с помощью принципа Ле Шателье. Действительно, если в равновесную систему жидкость – пар, например Н2О (ж) ↔ Н2О (г), ввести растворимое нелетучее вещество, то давление пара растворителя над раствором уменьшится. Чтобы компенсировать понижение давления пара и достигнуть прежнего равновесного состояния, раствор нужно нагреть до более высокой температуры (больше 373º К), так как процесс эндотермический (ΔНк > 0). Пусть имеется равновесная система твердая фаза – жидкость, например Н2О (т) ↔ Н2О (ж), при 273º К. Если растворить в жидкой фазе некоторое количество нелетучего вещества (нерастворимого в твердой фазе), то концентрация молекул воды в жидкой фазе уменьшится. В соответствии с принципом Ле Шателье начнет идти процесс, увеличивающий количество воды в жидкой фазе, — плавление льда. Для установления, нового равновесия раствор необходимо охладить, т. е. понизить температуру, так как процесс экзотермический (ΔНпл< 0). По закону Рауля для разбавленных растворов понижение давления пара пропорционально концентрации раствора. Следовательно, повышение температуры кипения и понижение температуры замерзания таких растворов должно возрастать с увеличением их концентрации. Изучая замерзание и кипение растворов, Рауль установил: повышение температуры кипения ΔТК и понижение температуры замерзания ΔТз разбавленных растворов неэлектролитов прямо пропорционально моляльной концентрации раствора: где b (X) — моляльная концентрация, моль/кг; Кэ и Кз — коэффициенты пропорциональности, кг•К•моль–1, которые называются соответственно эбулиометрической и криометрической константами. Физический смысл констант Кэ и Кз становится ясен, если принят b (X) = 1. Тогда Кэ = ΔТК а Кз = ΔТз . Иначе говоря, эбулиометрическая константа численно равна повышению температуры кипения одномоляльного раствора, а константа криометрическая — понижению температуры замерзания одномоляльного раствора. Эбулиометрические и криометрические константы зависят только от природы растворителя и не зависят от природы растворенного вещества (идеальные растворы). В табл. 1 представлены значения эбулиометрических и криометрических констант некоторых растворителей. 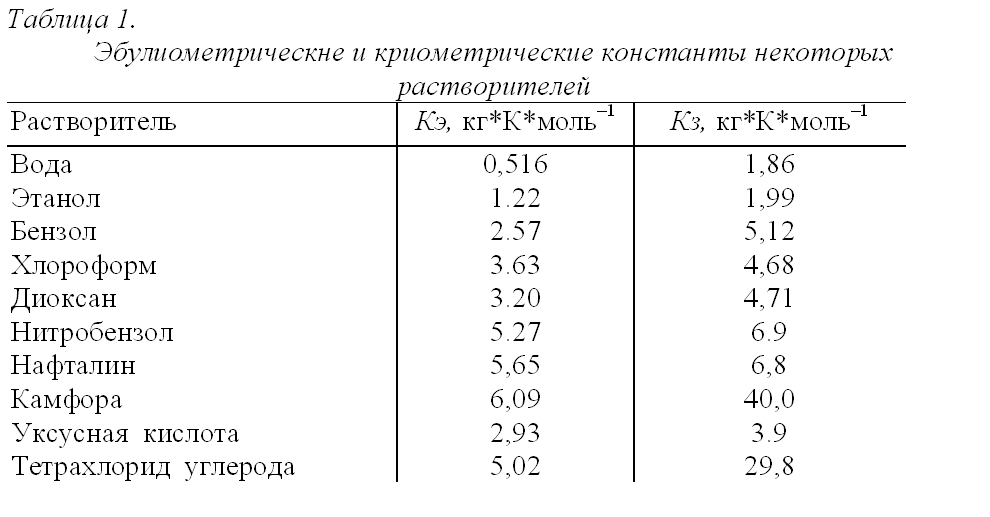 где mра - масса растворенного вещества, г; mр-ль — масса растворителя, г; ΔТз - понижение температуры замерзании и Δ Тк — повышение температуры кипения, определенные экспериментально, К°; Кэ, Kз — эбулиометрическая и криометрическая константы, кг•К•моль–1. 3. Роль осмоса и осмотического давления в биологических системах.Явление осмоса играет важную роль во многих химических и биологических системах. Благодаря осмосу регулируется поступление воды в клетки и межклеточные структуры.  Рис. 6. Благодаря осмосу вода поступает по корням к стволу дерева. Упругость клеток (тургор), обеспечивающая эластичность тканей и сохранение определенной формы органов, обусловлена осмотическим давлением. Животные и растительные клетки имеют оболочки или поверхностный слой протоплазмы, обладающие свойствами полупроницаемых мембран. При помещении этих клеток в растворы с различной концентрацией наблюдается осмос.  Рис.7. Под действием корневого давления вода выделяется на листьях растений. Растворы, имеющие одинаковое осмотическое давление, называют изотоническими. Если два раствора имеют различное осмотическое давление, то раствор с большим осмотическим давлением является гипертоническимпо отношению ко второму, а второй - гипотоническимпо отношению к первому. При помещении клеток в изотонический раствор (рис. 8 а) клетки сохраняют свой размер и нормально функционируют. При помещении клеток в гипотонический раствор вода из менее концентрированного внешнего раствора переходит внутрь клеток, что приводит к их набуханию, а затем к разрыву оболочек и вытеканию клеточного содержимого. Такое разрушение клеток называют лизисом(рис. 8 б). В случае эритроцитов этот процесс называют гемолизом. Кровь с клеточным содержимым, выходящим наружу при гемолизе, за свой цвет называется лаковой кровью. 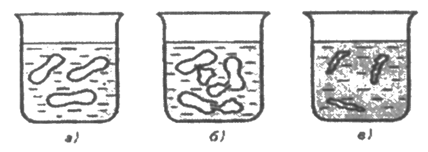 Рис. 8. Изменения, происходящие с кровяными тельцами в растворах NaCl различной концентрации. а) – изотонический раствор NaCl (0,9%); б) – гипотонический раствор NaCl (0,1%); в) – гипертонический раствор NaCl (2,0%); 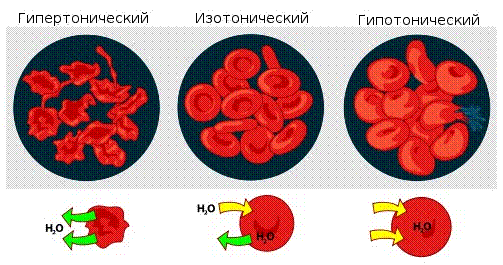 Рис. 9. Изменения, происходящие с эритроцитами в растворах с различной концентрацией NaCl. При помещении клеток в гипертонический раствор вода из клеток уходит в более концентрированный раствор и наблюдается сморщивание (высушивание) клеток (рис. 8 в). Это явление называется плазмолизом. Процессы плазмолиза и лизиса зависят от проницаемости оболочек клеток. Так, если концентрированные растворы солей, глюкозы вызывают стойкий плазмолиз, то растворы спирта, хлороформа его не вызывают. Это связано с тем, что последние вещества, как и вода, легко проникают через клеточные мембраны. Биологические жидкости человека — кровь, лимфа, тканевые жидкости — представляют собой водные растворы низкомолекулярных соединений — NaCl, KC1, СаСl2, высокомолекулярных соединений — белков, полисахаридов, нуклеиновых кислот и форменных элементов — эритроцитов, лейкоцитов, тромбоцитов. Их суммарным действием определяется осмотическое давление биологических жидкостей. Осмотическое давление крови человека при 310 К (37 °С) составляет 780 кПа (7,7 атм). Такое же давление создает и 0,9 %-ный водный раствор NaCl (0,15 моль/л), который, следовательно, изотоничен с кровью. Этот раствор называется физиологическим.  Рис 10. Форма выпуска изотонического раствора для инъекций. 5% раствор глюкозы тоже изотоничен крови.  Рис 11. Форма выпуска раствора глюкозы для инъекций. Однако в крови кроме ионов Na+ и С1–имеются и другие ионы, а также ВМС и форменные элементы. Поэтому в медицинских целях более правильно использовать растворы, содержащие те же компоненты и в том же количестве, что и входящие в состав крови. Эти растворы применяют в качестве кровезаменителей в хирургии. Осмотическое давление биологических жидкостей у разных живых организмов неодинаково. Так, некоторые морские животные имеют осмотическое давление крови выше, чем у человека. Это связано с обитанием этих животных в среде с высоким содержанием солей. 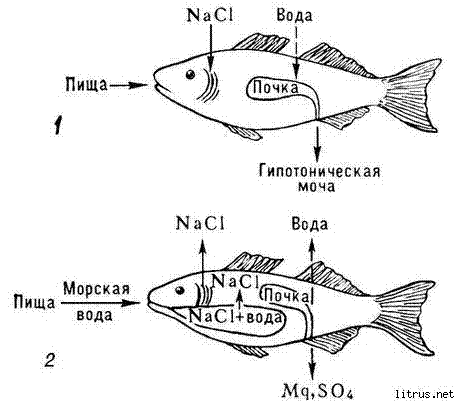 Рис.12. Осморегуляция у рыб: 1) пресноводная рыба; 2) морская рыба. Пунктиром обозначено движение воды по осмотическому градиенту. Пресноводные рыбы всасывают соли натрия жабрами: у морских рыб клетки жаберного аппарата выделяют их. Почка морских рыб выделяет соли магния (сульфаты), избыток которых поступает с пищей и морской водой. Осмотическое же давление крови лягушек ниже, чем у человека. Осмотическое давление тканевых жидкостей растений и многих морских животных в известной степени колеблется при изменении содержания растворенных веществ во внешней среде. Высокоорганизованные животные обладают постоянным осмотическим давлением крови и других биологических жидкостей, т. е. имеет место осмотический гомеостаз. Человеческий организм помимо осмотического давления характеризуется постоянством (гомеостазом) и других физико-химических показателей крови, например кислотности. Допустимые колебания осмотического давления крови весьма незначительны и даже при тяжелой патологии не превышают нескольких десятков кПа. Таким образом, при различных процедурах в кровь человека и животных в больших количествах можно вводить только изотонические растворы. При больших потерях крови, например, после тяжелых операций, травм, больным вводят по нескольку литров изотонического раствора для возмещения потери жидкости с кровью. Явление осмоса широко используют в медицинской практике. Так, в хирургии применяют гипертонические повязки (марля, смоченная в гипертоническом 10 %-ном растворе NaCl), которые вводят в гнойные раны (рис. 13). 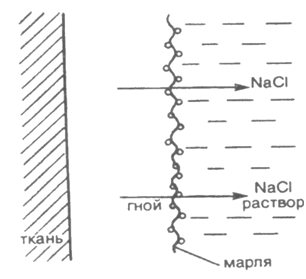 Рис.13. Принцип применения гипертонических повязок для очистки пораженных тканей от гноя и продуктов распада. По закону осмоса ток жидкости раны через марлю направляется наружу, в результате чего рана постоянно очищается от гноя, микроорганизмов и продуктов распада. 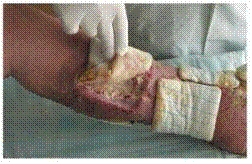 Рис.14. Лечение гнойных ран наложением гипертонической повязки. Действие слабительных — горькой соли MgSO4•7H2O и глауберовой соли Na2SO4•7H2O также основано на явлении осмоса. Эти соли плохо всасываются при попадании в желудочно-кишечный тракт. В результате применения гипертонических растворов этих солей в просвет кишечника устремляется большое количество воды через слизистую оболочку, что способствует послабляющему действию этих солей.  Рис.15. Горькая или английская соль.  Рис.16. Кристаллы глауберовой соли. Гипертонические растворы в небольших количествах вводятся иногда внутривенно при глаукоме, чтобы уменьшить избыточное количество влаги в передней камере глаза.  Рис.17. Глаукома. Гипертонические растворы соли (рассол) и сахара (сироп) используют при консервировании продуктов, так как в этой среде происходит плазмолиз микроорганизмов.  Рис 18. Консервированные продукты. При уменьшении содержания в крови белка (альбуминов и глобулинов) происходит снижения онкотического давления крови. При этом развиваются онкотические отеки. 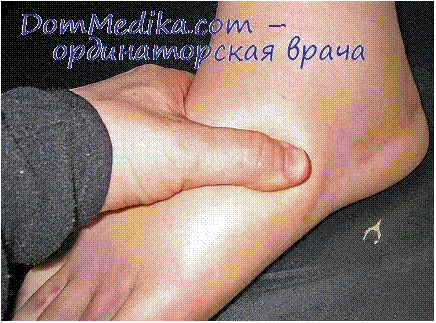 Рис. 19. Онкотичекий отек. |
