Микрофлора полости рта. Микробиология. Занятие 1 микрофлора полости рта, её состав и характеристика (микрофлора зубной бляшки, слюны, десневых карманов)
 Скачать 0.85 Mb. Скачать 0.85 Mb.
|
|
Понятие о биопленках В настоящее время ученые рассматривают зубной налет как биопленку. Биопленки (биологические пленки) – это организованные сообщества микробов, формирующиеся в условиях текучих сред. Основными свойствами биопленки являются: 1) взаимодействующая общность разных типов микроорганизмов (микробиоценоз) с симбиотическими связями; 2) микроорганизмы образуют микроколонии; 3) микроколонии окружены защитным матриксом, пронизанным каналами, по которым циркулируют питательные вещества, продукты жизнедеятельности, ферменты, метаболиты и кислород; 4) микроорганизмы имеют определенную систему связи; 5) микроорганизмы в биопленке устойчивы к антибиотикам, антимикробным средствам и реакции организма хозяина. Исследования, проведенные на биопленках в их естественном состоянии, показали, что существуют большие различия в поведении бактерий в лабораторной культуре и в их естественных экосистемах. К примеру, бактерия в биопленке вырабатывает такие вещества, которые она не продуцирует, будучи в культуре. Кроме того, матрикс, окружающий микроколонии, служит защитным барьером. Это помогает понять, почему антимикробные средства как общего действия, так и применяемые местно, не всегда дают успешные результаты, даже тогда, когда они нацелены на конкретный вид микроорганизмов. Факторы, способствующие развитию кариеса Кариес - это патологический процесс, при котором происходит деминерализация и размягчение твердых тканей зуба с последующим образованием полости. В инициировании кариозного процесса принимает участие множество факторов. Все их можно разделить на общие и местные. Общие факторы: 1.Неполноценная диета и плохая питьевая вода. 2.Соматические заболевания, сдвиги в функциональном состоянии органов и систем в период формирования и созревания тканей зуба. 3.Экстремальные физические и нервно–психические воздействия на организм (стрессы). 4.Наследственность, обусловливающая полноценность структуры и химический состав тканей зуба. Местные факторы: 1. Зубная бляшка и зубной налет. 2.Нарушение состава и свойств ротовой жидкости. 3.Углеводистые липкие пищевые остатки в полости рта. 4.Отклонения в биохимическом составе твердых тканей зуба. 5.Состояние пульпы зуба. 6. Состояние зубочелюстной системы в период закладки, развития и прорезывания постоянных зубов. Кариесогенные факторы могут иметь различную интенсивность и характер, однако ведущим из них является микрофлора полости рта. Патогенез кариеса В настоящее время общепризнанным механизмом возникновения кариеса является прогрессирующая деминерализация твердых тканей зубов под действием органических кислот, образование которых связано с деятельностью микроорганизмов. В норме зубная эмаль находится в состоянии динамического равновесия между постоянно протекающими процессами де- и реминерализации. Деминерализация обусловлена свободными ионами водорода Н+, главным источником которых являются органические кислоты – продукты метаболизма оральных микроорганизмов. Скорость разрушения эмали значительно повышается при снижении значения рН среды ниже 5. Большое значение при развитии кариозного процесса имеет длительность контакта кислых продуктов с зубной эмалью. Кариес развивается на тех поверхностях зуба, которые находятся в длительном контакте с образовавшимися кислотами. Это приводит к постепенному увеличению микропространств между кристаллами эмалевых призм. В образовавшиеся мельчайшие дефекты проникают микроорганизмы и повреждают эмаль на участках, расположенных параллельно наружной и внутренней поверхности. Длительный процесс деминерализации завершается растворением устойчивого поверхностного слоя и образованием полости в зубе. Главное условие развития кариеса - формирование зубной бляшки, благодаря чему обусловливается местное деминерализующее действие микробной флоры, населяющей её (продукция молочной кислоты в результате гликолиза). Развитию кариеса способствует поступление в полость рта углеводов, которые являются пищевыми субстратами для микроорганизмов и исходным веществом для синтеза органических кислот. Кариесогенные микроорганизмы К кариесогенным относят, в первую очередь, микроорганизмы, способные вызвать кариес в чистой культуре или в ассоциации с другими микробами у гнотобиотных животных. Наибольшее значение в развитии кариеса имеют оральные стрептококки (S. mutans, S. sangius), лактобактерии и некоторые актиномицеты. Ведущая роль отводится виду S. mutans, состоящему из 8 сероваров. Он является наиболее кислотообразующим представителям среди стрептококков полости рта и может существовать при низких значениях рН. Одним из важнейших биологических свойств S. mutans является способность этих бактерий прикрепляться к гладким поверхностям зуба. Адгезия к зубам обеспечивает формирование бляшек этими микробами. Стрептококки ферментируют многие углеводы с образованием молочной кислоты. При этом рН в бляшках снижается до критического уровня (рН 5 и ниже). Наряду с кислотообразованием патогенетическое значение имеет способность оральных стрептококков образовывать внеклеточные полисахариды — растворимый и нерастворимый гликан (декстран) и леван (фруктан). Растворимый гликан и леван легко расщепляются как S.mutans, так и другими микроорганизмами, а нерастворимый гликан активно участвует в процессе адгезии оральных микроорганизмов. Образование гликана вызывает межклеточную агрегацию S. mutans и других бактерий, присутствующих в бляшке (Noccardia, Neisseria, A. vicosus, С. albicans). Гликаны стабилизируют бляшку. Липкий гликановый матрикс зубной бляшки препятствует диффузии большого количества молочной кислоты, образуемой микробами, что продлевает её пребывание на поверхности зубов и ведёт к деминерализации эмали, вызывая кариес зубов. Кроме того, внеклеточные полисахариды, заполняя весь объем бляшки или очага поражения, затрудняют процесс реминерализации, препятствуя поступлению в эмаль ионов кальция и фосфатов. Если стрептококки превалируют в полости рта, то количество лактобактерий в бляшке составляет примерно 1% от общего количества микробов, находящихся в зубной бляшке. Лактобактерии играют незначительную роль на начальных этапах адгезии микробов к эмали зуба и в формировании бляшки. Однако их роль резко возрастает в прогрессировании кариеса по мере увеличения степени выраженности кариозного поражения. Лактобактерии толерантны к низкой рН и способны синтезировать большое количество молочной кислоты из углеводов. Очевидно, эти микробы играют решающую роль в деструкции дентина после деформации эмали. Что же касается роли актиномицетов в возникновении кариеса, то они, видимо, участвуют в кариозных поражениях корней зубов у пожилых людей при обнажении корневого участка зуба. Кроме того, актиномицеты, бактероиды и другие микроорганизмы выделяют протеазы, которые участвуют в разрушении дентина, а, следовательно, увеличивают кариозные поражения. На кариесогенную активность оральных микроорганизмов влияет слюна - её агрегирующие факторы, которые, с одной стороны, способствуют прикреплению микробных клеток к поверхности зуба, а с другой - удаляют их при омывании полости рта. На равновесие между процессами де- и реминерализации влияют многие факторы - наличие в слюне бикарбоната, мочевины, ионов кальция, фосфора и другие. При снижении рН ниже критического уровня (5 и менее) ионы кальция и фосфора выходят из зубной эмали в окружающую среду. При повышении рН они входят в состав эмали обратно. Способностью повышать значение рН и, следовательно, противокариозным действием обладает система буферов бикарбонат-карбоновая кислота и сиалин, находящийся в слюне. 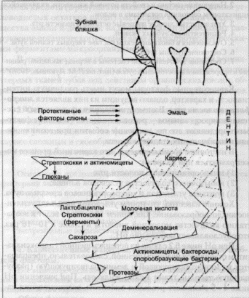 Рис. 1. Роль микроорганизмов в патогенезе кариеса зубов. Профилактика кариеса Для профилактики кариеса разрабатывается ряд направлений: Применение антимикробных веществ. Применение сахарозаменителей (следствие – уменьшение образования молочной кислоты). Разработка вакцины. Профилактика кариеса может быть направлена на уменьшение количества кариесогенных микроорганизмов в полости рта. Механическое удаление зубных бляшек нецелесообразно, поскольку на очищенную поверхность сразу же оседают новые бактериальные клетки, что приводит к быстрому восстановлению микрофлоры. Более эффективно применение различных бактерицидных и бактериостатических препаратов. Хорошие результаты получают с помощью антисептиков, в частности 0,2% хлоргексидина. При этом количество клеток S. mutans в зубных бляшках снижается на 80-85%, а в слюне на 55%. Покрывая зубную поверхность, хлоргексидин не только оказывает на микроорганизмы бактерицидное действие, но и препятствует их адгезии, нарушая при этом микробное равновесие. Угнетающим действием на микроорганизмы обладает фтор и его соединения, особенно соли ZnF2 и CuF2, а также пятиатомный спирт - ксилит, который нарушает процесс гликолиза у бактерий. Для профилактики кариеса используют химические ингибиторы, подавляющие определенные метаболические реакции у S. mutans. Например, фтор угнетает действие ферментов, участвующих в процессе гликолиза, к которым относятся: фосфатазы, эндолазы и фосфоглицеромутазы. Это приводит к торможению кислотообразования. Подобным действием обладает Н-лаурилсаркозинат и гидроацетат натрия. Другой путь снижения кислотообразования и накопления глюканов - замена сахарозы другими углеводами, например, соединениями ксилита, при ферментативном расщеплении которых эти продукты не образуются. Основной защитный механизм местного иммунитета полости рта при кариесе состоит в способности секреторного IgA препятствовать адгезии S. mutans. Признание ведущей роли микробов группы "мутанс" в качестве этиологического агента кариеса позволило осуществить опыты по получению препаратов для иммунизации против кариеса (убитые вакцины, очищенные белки клеточной стенки, рибосомальные антигены, глюкозилтрансфераза, ДНК). Исследования, проведённые как на животных, так и на людях - добровольцах, показали определённую эффективность такой вакцинации. Продемонстрирована также защита от кариеса в результате пассивной передачи секреторного IgA и сывороточного IgG. Недостатки вакцинации: эти микробы содержат перекрёстные антигены с тканями сердца, почек, скелетных мышц человека и животных, что может обусловить различные патологические реакции аутоиммунного характера; ввиду общности антигенов стрептококков группы "мутанс" с другими оральными стрептококками выработка антител к St. mutans может привести к нарушению микробного биоценоза в полости рта. Рассматриваются также возможности создания вакцин против Actinomycis viscosus , принимающего активное участие в патогенезе кариеса. Микробиологические методы изучения микрофлоры при кариесе и его осложнениях. Исследование микрофлоры при кариесе проводят при помощи бактериоскопического и бактериологического методов. Материалом для исследования могут служить зубная бляшка, материал из кариозной полости, ротовая жидкость. Методические указания Особенности забора исследуемого материала при кариесе. Исследование зубной бляшки Перед снятием зубного налета необходимо провести тщательную гигиеническую обработку полости рта, используя различные механические методы и контролируя обработку определением индекса гигиены. С этой целью пользуются специальными красящими растворами, определяя зону зубного налета. При исследовании зубной бляшки необходимо учитывать: методику забора бляшки с поверхности зуба; методику дисперсии материала бляшки; методику микроскопического подсчета и подсчета выживаемости микробов при культивировании. Методика взятия материала зубной бляшки Бляшка, расположенная на доступной гладкой поверхности зуба (щечная, язычная), может быть снята путем соскабливания обычным стерильным инструментом: экскаватором, скейлером. Для снятия бляшки с проксимальных поверхностей можно использовать стерильную нитку. Бляшку из ямок, фиссур можно получить острым зондом или заостренной ортодонтической проволокой. В некоторых случаях материал берут маленькими стерильными ватными тампонами. Однако из-за плотности прилипания бляшки и трудности ее снятия этот способ годится только для изучения начальной стадии колонизации микробов на эмали. Наддесневую зубную бляшку можно снять стерильными экскаватором или скейлером. Для бактериологического исследования материал должен быть сразу после забора помещен в транспортную питательную среду с целью сохранения жизнеспособности микробов. Полученный материал взвешивается на аналитических весах с последующим разведением от 1:100 до 1:1000 и посевом на питательные среды. Методика дисперсии материала бляшки Точность определения количества и видов бактерий в бляшке зависит от тщательности дисперсии материала. Можно разбивать конгломераты бляшки путем встряхивания со стеклянными бусами в гомогенизаторе, обработкой материала в ультразвуковых дезинтеграторах. Однако ультразвук может вызвать гибель некоторых бактерий: особенно чувствительны к ультразвуковой обработке спирохеты и некоторые грамнегативные бактерии. В связи с этим обработку ультразвуком обычно проводят в течении 10 сек. Микроскопический подсчет, подсчет выживаемости микробов при культивировании Примой микроскопический подсчет суспензированных микробов можно осуществлять в камере Горяева.  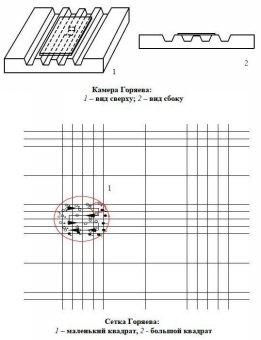 Рис. 2. Камера Горяева - это приспособление предназначенное для подсчета количества клеток в заданном объеме жидкости. Можно также изучать материал в темном поле или фазово-контрастном микроскопировании. Подсчет жизнеспособных клеток из взятого образца проводят методом серийных разведений в стерильном физиологическом растворе (1:10, 1:20 и так далее). Из каждого разведения определенный объем засевают на поверхность плотной среды. После инкубации подсчитывают количества КОЕ (колониеобразующие единицы) и пересчитывают количество на исходный объем. Успех метода зависит от использования подходящих питательных сред и условий культивирования, так как большая часть резидентов является строгими анаэробами и микроаэрофилами. Низкую высеваемость микробов можно объяснить недостаточной дисперсией, прилипанием микробов к поверхности стекла при приготовлении разведений и неудачным подбором питательной среды. Забор материала из кариозной полости Сначала из кариозной полости стерильным бором убирают поверхностные слои размягченного дентина, смоченного слюной. Не допуская попадания в исследуемый материал слюны, другим стерильным бором обрабатывают полость и помещают дентин с помощью стерильной гладилки в транспортную среду. Забор ротовой жидкости Ротовую жидкость обычно у больных утром (9-11 час.) через 2 часа после приема пищи собирают в течение 10 мин в стерильные пробирки. Эту слюну называют нестимулированной. Стимулированную слюну получают после нанесения на спинку языка 1-2 капель стерильного 2% раствора лимонной кислоты или жевания 5 г. парафина в течении 30 сек. Паротидную слюну получают путем введения в проток специальной стерильной канюли. Ротовая жидкость собирается в стерильную пробирку, исследуется 0,1 мл. Занятие № 3. МИКРОБИОЛОГИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА Вопросы для самоподготовки: Основные представители резидентной микрофлоры при отсутствии патологии тканей пародонта. Особенности состава микрофлоры при гингивите. Особенности состава микрофлоры при пародонтите. Пародонтопатогенные микробы (Porphyromonas gingivalis, Prevotella melaninogenica). Доказательства их участия в патогенезе заболевания. Механизм и условия возникновения заболеваний пародонта Методы изучения количественного и качественного состава микрофлоры десневого желобка и пародонтальных карманов. Информационный материал Микрофлора пародонта при отсутствии патологий Ткани здорового пародонта связаны с довольно ограниченной флорой, расположенной под десной на поверхности зуба. Микробы пародонта составляют слой толщиной от 1 до 20 клеток. Исследование в области десневого желобка выявило довольно тонкий слой (около 60 нм.), состоящий на 3/4 из грамположительных кокков. Вместе с палочками они составляют 90% популяции. Спирохеты встречаются редко - около 1,8%. Соотношение подвижных форм к неподвижным составляет в здоровых тканях – 1/49. В десневом желобке бляшка состоит в основном из грамположительных факультативных анаэробных кокков (стрептококки, в меньших количествах - стафилококки, пептострептококки) и палочек (актиномицеты: A. israelii, A. naeslundii, A. viscosus, A. odontolyticus, а также пропионибактерии). Болезни пародонта. Определение, классификация Болезни пародонта – это разнородная группа заболеваний воспалительной и обменно-дистрофической природы, сопровождающихся разрушением тканей десны, включая коллагеновую основу периодонта и кости альвеолярного отростка. К заболеваниям пародонта относят: 1. Гингивит (локальное воспаление десны). 2. Пародонтит (прогрессирующий воспалительный процесс с деструкцией тканей пародонта и кости). 3. Пародонтоз (преимущественно дистрофическое поражение тканей пародонта). 4. Пародонтомы (опухолевые и опухолеподобные процессы тканей пародонта). Воспалительные заболевания пародонта (гингивит и пародонтит) широко распространены среди населения: 60-70% после 30 лет и 85-97% - после 65, и являются ведущей причиной потери зубов у большинства взрослых. |
