Химия практика. Зертханалық жұмыс 2. Бөлшектеп талдау. Зертханалы жмыс 2. Сілтілік металдар жне аммоний топтары катиондар оспасыны жекелік реакциялары жне оларды блшектеп талдау
 Скачать 22.19 Kb. Скачать 22.19 Kb.
|
|
Зертханалық жұмыс №2. Сілтілік металдар және аммоний топтары катиондар қоспасының жекелік реакциялары және оларды бөлшектеп талдау (1-аналитикалық топ катиондары) І-аналитикалық топ катиондарын бөлшектеп талдау І. рН анықтау: Егер рН>7 болса, зерттеуге алынған ерітіндіде Na+ мен K+ катиондарының тұздары басым болады. 2.NH4+ катионын анықтау: Зерттелетін ерітіндіден NH4+ катионын ашуға ерітіндідегі Na+ мен K+ катиондары кедергі жасамайды. а) Несслер реактивімен ашу: Заттық шыны бетіне 1 тамшы зерттелетін ерітінді, 1 тамшы Несслер реактивін K2[HgJ4]+KOH тамызып, оларды шыны таяқшамен қосу керек. Тамшылар арасында қоңыр - қызыл түсті тұнбаның түзілуі, ерітіндіде NH4+ катиондары бар екендігін дәлелдейді: NH4CI + 2K2[HgI4] + 4KOH → [OHg2NH2]I2+7KI +KCI+3H2O б) Гидроксидтермен ашу: Сынауыққа 5-6 тамшы зерттелетін ерітіндіні тамызып үстіне сонша мөлшерде 2 н натрий гидроксиді NaOH ерітіндісін қосып қыздырады. Сынауықтың аузына суланған универсалды немесе қызыл лакмус қағазын ұстау керек.Зерттелетін ерітінді құрамында NH4+ катиондары болған жағдайда, фенолфталеин қағазы қызарады, ал қызыл лакмус қағазы көгереді. Сынауықтың ауызына концентрленген тұз қышқылы НСl ерітіндісіне батырылған таяқшаны апарғанда, таяқшаның маңында (сынауықтың ішінде) «ақ түтін» пайда болады (HCl +NH4+→NH4Cl +H+). Индикатор қағазы түсінің өзгеруі: 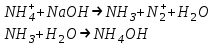 ІІ. Егер ерітіндіде NH4+ катиондары жоқ болса, Na+ мен K+ катиондары бөлшектеп анықталады. 3. K+ катионын ашу: а) Натрийдің гексанитрокобальтатыNa3[Co(NO2)6] реактивімен анықтау: Зерттелетін ерітіндінің 2-3 тамшысына сонша көлемде ннтрийдің гексанитрокобальтаты Na3[Co(NO2)6] ерітіндісін қосқанда сары түсті тұнба түзіледі. Реакцияны заттық шыны бетінде де орындауға болады. б) Натрийдің гексанитроқорғасынкупраты Na2[PbCu(NO2)6] реактивімен ашу реакциясын орындау арқылы дәлелдеуге болады. 4. Na+ катионын ашу: Калийдің дигидроантимонаты KH2SbO4 реактивімен ашу (K+ катиондары кедергі жасамайды): Бұл реактивпен Na+ катионын ашу үшін ерітіндідегі натрий тұздарының концентрациясы жоғары болуы керек. Сондықтан фарфор тигельге 10-15 тамшы зерттелетін ерітіндіні көлемі 2 есе азайғанша қыздырып, суалту керек. Ерітіндіні сынауыққа ауыстырып, суытып, үстіне реактив қосады. сынауықтың қабырғасын шыны таяқшамен ысқылап, ерітіндіні араластыру керек. Na+ катиондары бар болған жағдайда, ақ кристалды (аморфты емес!) тұнба түзіледі. Егер зерттелетін ерітіндіде NH4+ катиондары бар болса, онда К+ катионын анықтамастан бұрын одан арылу керек. NH4+ катиондарынан арылу: Ерітіндідегі аммоний тұздарын термиялық әдіспен ыдыратып, NH4+ катиондарын жоюға болады: Фарфор табақшасындағы 15-20 тамшы зерттелетін ерітіндіні будақтатып «ақ түтін» бөлінгенше қыздыру керек. Табақшаны суытып, 8-10 тамшы дистильденген сумен құрғақ қалдықты ерітіп, ерітіндіде NH4+ катиондарының бар жоғы Несслер реактивімен тексеріледі. NH4+ катиондары бар тұздар былайша ыдырайды: 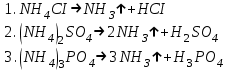 5. K+ және NH4+ катиондарын қатар анықтау: (NH4+ катиондарынан арылуды қажет етпейтін әдіс). Зерттелетін ерітіндінің (рН=7) 5-6 тамшысына 6-7 тамшы натрийдің гексанитрокобальтаты Na3[Co(NO2)6] ерітіндісін қосу нәтижесінде сары түсті аралас құрамды тұнбалар түзіледі: 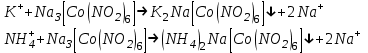 Түзілген сары кристалдық тұнбаның химиялық құрамын анықтау үшін, тұнбасы бар сынауық су моншасында 5-10 минут қыздырылады. Тұнбаның құрамында К2Na[Co(NO2)6] ғана болған жағдайда, тұнбаның түсі де, көлемі де өзгермейді. Егер тұнба еріп, еру кезінде газ тәріздес зат бөлініп, ерітіндінің түсі өзгерсе (қызғылт түске боялса), онда тұнбаның құрамында (NH4)2Na[Co(NO2)6] болғаны. Болатын өзгерістерді былай өрнектеуге болады: 4(NH4)2Na[Co(NO2)6]+22О2→4Co(NO3)2+4Na(NO3)2+16Н2О+20NO2 |
