потенциометрия. Цель работы ознакомиться с основами потенциометрического метода анализа, изучить принцип действия и работы рНметра и комбинированных стеклянных электродов,
 Скачать 284 Kb. Скачать 284 Kb.
|
|
Цель работы: ознакомиться с основами потенциометрического метода анализа, изучить принцип действия и работы рН-метра и комбинированных стеклянных электродов, измерить активность ионов водорода (pH) в водных растворах методом прямой потенциометрии (измерение ЭДС электродных систем и автоматическое вычисление параметров с использованием градуировочного графика). 1. Теоретические сведения 1.1. Потенциометрический метод анализа. Физико-химические основы метода Метод потенциометрического измерения концентрации ионов в растворе основан на измерении разности электрических потенциалов двух специальных электродов, помещенных в испытуемый раствор, причем один электрод — вспомогательный — в процессе измерения имеет постоянный потенциал. Потенциал Е отдельного электрода определяют по уравнению Нернста через его стандартный (нормальный) потенциал Е0 и активность ионов а+, которые принимают участие в электродном процессе. Стандартным (нормальным) является потенциал, который возникает на электроде, когда активность a+ = 1. У идеальных растворов коэффициент активности равен единице, поэтому активность и концентрация совпадают: где Уравнение Нернста, выведенное для узкого класса электрохимических систем металл — раствор катионов этого же металла, справедливо в значительно более широких пределах. На границе между электродом из инертного металла и раствором, содержащим окислительно-восстановительную систему, также возникает скачок потенциала где Ох— число ионов окисленной формы; Rd — число ионов восстановленной формы; п — число электронов, принимающих участие в реакции. Скачок потенциала определяется динамическим равновесием, при котором переход электронов от восстановителя к электроду и от электрода к окислителю происходит с одинаковыми скоростями. Скачок потенциала зависит от отношения активностей ионов окисленной (аОх) и восстановленной (aRd) форм: где Таким образом, потенциометрический метод можно использовать для измерения активности различных ионов в растворах электролитов. Для измерения величины рН используют различные электроды, подчиняющиеся уравнению Нернста, в котором потенциал электрода является функцией не концентрации, а активности ионов. В связи с этим в настоящее время применяют другое определение понятия рН – логарифм активности ионов водорода, взятый с обратным знаком: Пока еще нет способа экспериментального определения коэффициента активности отдельного иона. Активность зависит от свободной энергии системы и определяется не только концентрацией, но и температурой, характером растворителя и физико-химическим процессом, происходящим в растворе. Таким образом, коэффициент активности какого-либо иона является его характеристикой в данной среде и при данных условиях. Для измерения активности ионов водорода потенциометрическим методом можно использовать «водородный» измерительный электрод. Он представляет собой пластинку с пористой поверхностью (обычно губчатая платина), помещенную в контролируемый раствор, который непрерывно продувается газообразным водородом при атмосферном давлении. Водород адсорбируется поверхностью электрода, который благодаря этому приобретает свойства водородного, т.е. его потенциал определяется активностью ионов водорода в растворе в соответствии с уравнением Нернста. Производственные рН-метры имеют измерительные стеклянные электроды, аналогичные по свойствам водородному электроду. 1.2. Измерительная ячейка для потенциометрических измерений Поскольку абсолютную величину электродного потенциала практически определить нельзя, измеряют его относительное значение, для чего составляют гальванический элемент из измерительного (индикаторного) электрода, анализируемой среды и вспомогательного (в литературе встречается термин «сравнительный» электрод) электрода. Схематическое изображение такого элемента: измерительный электрод – анализируемая среда – вспомогательный электрод. В отличие от индикаторного электрода, потенциал которого функционально связан с активностью контролируемых ионов, потенциал вспомогательного электрода должен всегда оставаться постоянным. Такой гальванический элемент называется в дальнейшем измерительной ячейкой для потенциометрических измерений. ЭДС измерительной ячейки равна алгебраической сумме потенциалов индикаторного и вспомогательного электродов: где Если известны нормальный потенциал индикаторного электрода Стеклянные электроды из специальных сортов стекла, как экспериментально установлено, при погружении в растворы электролитов обнаруживают свойства, аналогичные свойствам водородного электрода. На границе стекло – раствор возникает скачок потенциала, зависимость которого от активности ионов водорода (так называемая «водородная функция») подчиняется уравнению Нернста. Стеклянный электрод (рис. 3) представляет собой трубку 4 из обычного стекла, на конце которой напаяна чувствительная мембрана 1 (плоская, конусообразная или сферическая) из специального электродного стекла. Трубка закрыта пробкой 5. Стеклянный электрод заполнен так называемой приэлектродной жидкостью 2 (например, раствором соляной кислоты), в которую погружен контактный вспомогательный электрод 3 (обычно хлорсеребряный, бромсеребряный или каломельный). Потенциал внутренней поверхности мембраны по отношению к приэлектродной жидкости зависит от величины рН этой жидкости, в то время как потенциал наружной поверхности мембраны определяется величиной рН контролируемого раствора. 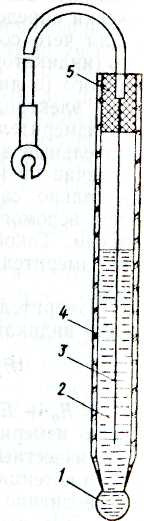 Рис. 3. Стеклянный электрод Таким образом, потенциал стеклянного электрода является алгебраической суммой потенциалов внутренней и наружной поверхностей измерительной мембраны. При условии постоянства рН при электродной жидкости результирующая ЭДС стеклянного электрода является функцией рН контролируемого раствора. Экспериментально установлено, что свойства наружной и внутренней поверхностей чувствительной стеклянной мембраны не совсем одинаковы. Помещенные по обе стороны от мембраны одинаковые растворы вызывают появление разных скачков потенциала, разность между которыми получила название потенциала асимметрии стеклянного электрода. Несмотря на проведение многочисленных работ, посвященных указанному явлению, исчерпывающего объяснения этого явления не дано. Известно, что потенциал асимметрии возрастает с увеличением толщины стенки мембраны и зависит от состава электродного стекла. Замечено, что с увеличением тугоплавкости стекла и его электрического сопротивления возрастает и потенциал асимметрии стеклянного электрода. Потенциал асимметрии не зависит от рН растворов, но меняется при изменении температуры. Электрическая цепь из стеклянного индикаторного СЭ и каломельного вспомогательного КЭ электродов показана на рис. 4.  Рис. 4. Электрическая цепь измерительной ячейки рН-метра Внутри стеклянного электрода помещен вспомогательный контактный электрод, чаще всего хлорсеребряный, служащий для создания электрической цепи ячейки. Таким образом, электрическая цепь измерительной ячейки состоит из нескольких самостоятельных элементов, каждый из которых влияет на суммарную ЭДС. 1.3. Приборы для потенциометрических измерений Специфические особенности электродной системы со стеклянным индикаторным электродом, обычно применяемым для измерения рН, и, в частности, высокое внутреннее электрическое сопротивление стеклянного электрода определяют ряд требований к приборам, предназначенным для работы в комплекте с электродными системами. Важнейшие из этих требований — высокое входное сопротивление прибора (не менее 1012 Ом) и весьма малая сила тока, протекающего через датчик в процессе измерения (меньше 10-12 А). Невыполнение этих условий приводит к поляризации электродов при подключении их к прибору и к большим погрешностям измерения, вызванным заметным падением напряжения на электродах, которое суммируется с ЭДС электродной системы. Приведенным требованиям отвечают только специальные приборы, называемые высокоомными, основной частью которых, как правило, является усилитель постоянного тока. Современные высокоомные приборы, применяемые для измерения рН, предназначены для работы с датчиками, внутреннее электрическое сопротивление которых может достигать 109 Ом. При этом входное сопротивление прибора, по крайней мере в 1000 раз больше сопротивления датчика, что обеспечивает практическое отсутствие погрешностей, связанных с протеканием тока через измерительную ячейку. Изменению активности ионов водорода в 10 раз (величины рН на единицу) соответствует при температуре 20°С по уравнению Нернста изменение ЭДС измерительной ячейки на 58 мВ. При диапазоне измерения до рН = 14 разность пределов измерения рН-метра, выраженная в единицах измеряемого входного напряжения, составляет 812 мВ. По принципу действия рН-метры можно разделить на три основные группы: приборы с непосредственным отсчетом, приборы с астатической компенсацией, приборы со статической компенсацией. Простейшая принципиальная схема рН-метра с непосредственным отсчетом приведена на рис. 5.  Рис. 5. Принципиальная схема рН-метра с непосредственным отсчетом: 1 и 2 – стеклянный и вспомогательный электроды; 3 – операционный усилитель; 4 – измерительный прибор или цифро-аналоговый преобразователь ЭДС Eхизмерительной ячейки подается на вход усилителя 3, представляющего собой операционный усилитель постоянного тока, охваченный отрицательной обратной связью. Операционные усилители, используемые в схемах рН-метров, имеют на входе полевые транзисторы. Высокая степень изоляции управляющего электрода полевого транзистора (так называемые транзисторы с изолированным затвором) обеспечивает требуемое входное сопротивление усилителя при входной силе тока порядка 10-12–10-14 А. К недостаткам полевых транзисторов с изолированным затвором можно отнести сравнительно невысокую стабильность характеристик и высокий уровень шумов, что приводит к явлению, получившему название «смещение нуля», т.е. наличию на выходе усилителя некоторого напряжения при нулевом сигнале на его входе. Нестабильность смещения нуля во времени, в свою очередь, обусловливает возникновение такого явления, как «дрейф нуля». Основными причинами дрейфа нуля являются изменение параметров усилительных элементов и деталей схемы вследствие их старения и колебаний температуры, а также изменение напряжения источников питания. Для уменьшения дрейфа нуля усилители постоянного тока выполняют по балансным (мостовым) схемам; такие усилители получили название дифференциальных. Дифференциальные усилители обычно выполняют по схеме, в которой один из входов (отмечен на рис. 5 знаком плюс) является неинвертирующим, т.е. изменение выходного сигнала усилителя совпадает по знаку с изменением сигнала на этом входе, а другой вход (отмечен знаком минус) является инвертирующим, т. е. изменение выходного сигнала усилителя противоположно по знаку изменению сигнала на данном входе. Приборы с непосредственным отсчетом просты по устройству, однако по точности они уступают приборам компенсационного типа. Простейшим рН-метром компенсационного типа является прибор, схема которого приведена на рис. 6. 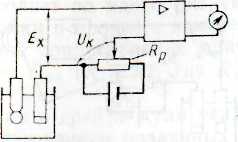   Рис. 6. Принципиальная схема рН-метра с ручной компенсацией измеряемой ЭДС В этом приборе используется метод астатической компенсации, когда последовательно с ЭДС электродной системы включено равное ей по величине и противоположное по знаку, напряжение компенсации Uк, снимаемое с компенсирующего переменного резистора (КПР) Rpили лабораторного потенциометра. Меняя перемещением движка реохорда, напряжение Uк, добиваются того, чтобы выходной сигнал усилителя был таким же, как при нулевом сигнале на входе. При этом напряжение Uкравно измеряемой ЭДС Eх. Шкала КПР отградуирована в единицах рН. Прибор, схема которого приведена на рис. 7, а, отличается от аналогичного рН-метра, работающего по методу ручной компенсации тем, что движок реохорда Rp, механически связанный с указателем шкалы, приводится в движение реверсивным двигателем. В момент компенсации, когда Eх=Uк, напряжение на входе Uвх усилителя равно нулю, и реверсивный двигатель останавливается. Недостатки таких приборов — сложность кинематической схемы для привода движка реохорда и необходимость применения самого реохорда, особенно в условиях химической промышленности. Этих недостатков лишена схема рН-метра, показанная на рис. 7, б. Здесь компенсационное напряжение создается цифроаналоговым преобразователем (ЦАП) 1, управляемым реверсивным счетчиком (PC) 2. Если входное напряжение усилителя Uвх=Eх-Uк отлично от нуля, то усиленное напряжение преобразуется в последовательность импульсов частотой f (в преобразователе 3), которые через переключатель 4 поступают в зависимости от полярности выходного напряжения усилителя либо на суммирующий, либо на вычитающий входы PC. В момент компенсации, когда Eх=Uк, напряжение на выходе усилителя равно нулю, импульсы на PC перестают поступать, а на выходе ЦАП устанавливается постоянное напряжение Uк. Помимо приборов с астатической компенсацией, применяемых при полной компенсации ЭДС измерительной ячейки, используют рН-метры со статической (неполной) компенсацией. Принципиальная схема, поясняющая принцип действия рН-метра со статической компенсацией, приведена на рис. 8. Измеряемая ЭДС Ех сравнивается с напряжением Uвых,образуемым от протекания выходного тока усилителя Iвыхпо резистору R. На вход усилителя поступает разность напряжений Uвх=Eх-Uвых. (8) Если полный коэффициент усиленияK=Uвых/Uвх,то уравнение (8) можно преобразовать к виду Eх=Uвых(1+1/K). При достаточно большом значении K: Eх Таким образом, сила тока, протекающего через оконечный каскад усилителя, практически пропорциональна входному сигналу от измерительной электродной ячейки. Измерив Iвых миллиамперметром, можно определить Ех, т.е. рН раствора. Применение метода статической компенсации позволяет во много раз уменьшить силу тока, потребляемого от ячейки в процессе измерения. В то же время эквивалентное входное сопротивление прибора возрастает в (K+ 1) раз, т.е. Rэкв= Rвх (K+ 1), где Rвх — входное сопротивление усилителя. Значительного уменьшения смещения и дрейфа нуля усилителей постоянного тока достигают использованием различных схем прямого усиления с автоподстройкой (автоматической коррекцией дрейфа нуля), а также преобразованием входного сигнала в переменное напряжение, усилением переменного напряжения и обратным преобразованием на выходе. 1.4. Температурная компенсация при измерении рН При изменении температуры контролируемого раствора электродный потенциал стеклянного электрода меняется вследствие изменения коэффициента RT/Fв уравнении (1). Вследствие этого одной и той же величине рН при разных температурах раствора соответствуют различные значения ЭДС электродной системы. Зависимость ЭДС электродной системы от рН и температуры представляет собой семейство прямых (рис. 9), пересекающихся в одной точке И. Эта точка соответствует величине рН раствора, при которой ЭДС электродной системы не зависит от температуры, поэтому точку пересечения указанных графиков называют изопотенциальной. Координаты изопотенциальной точки, обозначаемые ЕИи рНИ, являются важнейшими характеристиками электродной системы, которыми руководствуются при расчете схемы температурной компенсации рН-метра. Электродная система в соответствии с зависимостью ЭДС от рН и температуры раствора, описывается уравнением где Ех— ЭДС электродной системы в растворе с рНx; Если прибор отградуировать при какой-либо одной температуре раствора и в дальнейшем при измерениях не учитывать изменений его температуры, то погрешность измерения может составить На рис. 10 приведена схема рН-метра с автоматической температурной компенсацией, воспроизводящая зависимость (9). В качестве датчика температуры использован термометр сопротивления Rt. Схема выполнена в виде двойного моста. Питание измерительной схемы осуществляется от двух стабилизированных источников напряжения. Напряжение, компенсирующее ЭДС электродной системы, складывается из напряжения на участке АВ инапряжения в диагонали ВС наружного моста: Схема регулируется резистором REи так, чтобы напряжение на участке АВ было равно ЕИ.Тогда, если Ех=ЕИ, в момент баланса ЕBC=0. Естественно, что если напряжение ЕBCв диагонали наружного моста равно нулю, то оно не зависит от напряжения питания наружного моста, т.е. от напряжения между точками М и N. Подавая на вход прибора сигнал, равный ЕИ, с помощью резистора Rможно добиться такого положения, чтобы баланс (ЕBC=0) наступал, когда указатель прибора, перемещаемый реверсивным двигателем, останавливается против отметки шкалы, соответствующей, величине рН, равной рНИ. Реверсивный двигатель одновременно перемещает и движок КПР Rp. Если на вход поступает сигнал Ех 2. Описание прибора 2.1. Назначение 2.1.1. Назначение и область применения
2.1.2. Функциональные возможности
2.2. Основные технические данные и характеристики Диапазоны: Измеряемых значений ЭДС электродной системы, мВ, от минус 3000 до 3000 Измеряемых значений температуры растворов, °С от минус10 до 120. Преобразования ЭДС в pH, ед. pH от минус 2 до 20. Пределы допускаемых значений основной абсолютной погрешности: При измерении ЭДС электродной системы, мВ, не более ±1,0. При преобразовании ЭДС в pH, ед. pH, не более ±0,02. Выполнение требований п.2.2 обеспечивается в нормальных условиях эксплуатации согласно ГОСТ 22261-94 (далее по тексту НУЭ): температура окружающей среды (20 ± 5) С; относительная влажность воздуха не более 80%; источники электрических и магнитных полей отсутствуют; прибор не подвергается воздействию прямых солнечных лучей; вибрации не допускаются; напряжение питания (220 ± 4,4) В; частота питающего напряжения (50 ± 0,5) Гц. Значения дополнительных погрешностей при условиях эксплуатации, отличающихся от НУЭ, не превышают указанных в табл. 1 значений. Таблица 1 Пределы допускаемых значений дополнительных погрешностей
Пределы допускаемой абсолютной погрешности: Измерения температуры, °С :в диапазоне от 0 °С до 100 °С, °С, не более ±0,5; вне диапазона от 0 °С до 100 °С, в границах рабочего диапазона измерения температуры, °С, не более ±1,5. Автоматической температурной компенсации, ед. pH, не более ±0,01. Измерения ЭДС в рабочем диапазоне температур, мВ, не более ±1,5. Время установления показаний: при измерении ЭДС, с, не более 10; при измерении температуры, мин, не более 5. Время установления рабочего режима (прогрева), мин, не более 15. Время непрерывной работы не ограничено. Требования к электропитанию: Питание прибора должно осуществляться от сети переменного тока частотой (50±1) Гц, напряжением, В от 187 до 242. Мощность, потребляемая прибором от сети переменного тока, ВА, не более 4. Габаритные размеры прибора, мм, не более, 230×220×50. Масса прибора, кг, не более 1,5. 2.3.2. Принцип действия Прибор состоит из следующих функциональных узлов: многоканального аналого-цифрового преобразователя (АЦП); микроконтроллера; энергонезависимой памяти (ЭНОЗУ); клавиатуры; индикатора; сторожевого таймера; интерфейса последовательного порта; блока питания. Работой всех узлов управляет микроконтроллер по программе, находящейся во внутреннем ПЗУ микроконтроллера. Функциональная схема прибора приведена на рис. 15. Сигналы с датчика температуры (1) а также с потенциометрического входа (10) поступают на входы АЦП (2), где преобразуются в двоичный код. Полученный код обрабатывается микроконтроллером (6) и далее информация выводится на индикатор (8) или записывается в ЭНОЗУ (5) прибора, а также при появлении запроса внешнего устройства, может быть передана через интерфейс последовательного порта (4) запрашивающему устройству. Сигналы с клавиатуры (9) поступают непосредственно в микроконтроллер, где происходит их обработка. В случае возникновения сбоя, сторожевой таймер (3) производит перезапуск программы микроконтроллера. Блок питания (7) формирует напряжения для электрического питания остальных узлов.  Рис. 15. Прибор МУЛЬТИТЕСТ ИПЛ–301. Схема функциональная 1 – датчик температуры, 2 – аналого-цифровой преобразователь, 3 – сторожевой таймер, 4 – интерфейс последовательного порта, 5 – энергонезависимая память. 6 – микроконтроллер, 7 – блок питания, 8 – индикатор, 9 – клавиатура, 10 – потенциометрический вход. 2.4.2. Основное меню После включения прибора, на индикатор выводится основное меню. В верхней строке индикатора расположены символы "", соответствующие пунктам меню. Активный пункт обозначается изменяющимся символом "". Название активного пункта выводится в нижней строке индикатора. В основном меню выбирается один из режимов работы: измерение, градуировка или настройка. В   режиме "Измерение" прибор проводит измерение активности ионов согласно проведённой ранее градуировке или индицирует значение ЭДС в милливольтах. Одновременно измеряется и выводится на индикатор температура. Измеренные значения активности могут быть скорректированы с помощью автоматической температурной компенсации. режиме "Измерение" прибор проводит измерение активности ионов согласно проведённой ранее градуировке или индицирует значение ЭДС в милливольтах. Одновременно измеряется и выводится на индикатор температура. Измеренные значения активности могут быть скорректированы с помощью автоматической температурной компенсации.В  режиме "Градуировка" измеряются и настраиваются параметры электродной системы для проведения измерений. режиме "Градуировка" измеряются и настраиваются параметры электродной системы для проведения измерений.В режиме "Настройка" производится настройка звука, таймера, сетевого номера прибора. Перебор пунктов меню осуществляется нажатием клавиши ВЫБОР. Вход в режим - нажатием клавиши ВВОД. 2.4.4. Градуировка Назначение режима: В режиме "Градуировка" измеряются и настраиваются параметры электродной системы для проведения последующих измерений. В  ход в режим осуществляется выбором пункта "Градуировка" основного меню. ход в режим осуществляется выбором пункта "Градуировка" основного меню.Перед проведением градуировки следует провести настройку таймера и звука. Градуировка электродной системы проводится в следующем порядке: сброс всех параметров; ввод pH изопотенциальной точки (если данный параметр указан в паспорте на измерительный электрод); ввод параметров стандартных растворов (от двух до восьми). Введённые параметры градуировки сохраняются в энергонезависимой памяти прибора и не требуют повторного ввода, если не требуется их изменение. П  ункт "Изопотенциальная точка (pHи)" позволяет ввести параметры изопотенциальной точки для последующей работы в режиме автоматической температурной компенсации. При просмотре пункта "Изопотенциальная точка" на индикатор выводится надпись "pHи". ункт "Изопотенциальная точка (pHи)" позволяет ввести параметры изопотенциальной точки для последующей работы в режиме автоматической температурной компенсации. При просмотре пункта "Изопотенциальная точка" на индикатор выводится надпись "pHи".В  ид пункта "Изопотенциальная точка (pHи)" изменяется в зависимости от наличия в памяти значения указанной величины. При наличии ее в памяти пункт имеет вид ид пункта "Изопотенциальная точка (pHи)" изменяется в зависимости от наличия в памяти значения указанной величины. При наличии ее в памяти пункт имеет вид Ввод значения pH изопотенциальной точки: Основное меню → Градуировка → pHи Ввод значения pH изопотенциальной точки необходим для выполнения измерений с автоматической температурной компенсацией. Параметры изопотенциальной точки могут быть указаны в паспорте на конкретный электрод или определены самостоятельно. Общепринятое обозначение данного параметра - pHи (pXи) или pHi (pXi). Для выполнения измерений без температурной компенсации ввод значения pH изопотенциальной точки не требуется. Д  ля ввода параметров изопотенциальной точки следует выбрать пункт "Изопотенциальная точка" (pHи) меню "Градуировка" и нажать клавишу ВВОД. ля ввода параметров изопотенциальной точки следует выбрать пункт "Изопотенциальная точка" (pHи) меню "Градуировка" и нажать клавишу ВВОД.Если значение pH изопотенциальной точки было занесено в память прибора ранее, то пункт "Изопотенциальная точка" (pHи) отображается в меню "Градуировка" символом В  этом случае для ввода нового значения следует сбросить ранее установленное. этом случае для ввода нового значения следует сбросить ранее установленное.Если значение pH изопотенциальной точки не было занесено в память прибора ранее, то пункт "Изопотенциальная точка" (pHи) отображается в меню "Градуировка" символом Для ввода нового значения нажать клавишу ВВОД. Н   а индикатор в верхней строке выводится символ а индикатор в верхней строке выводится символ Цифровыми клавишами и клавишей ТОЧКА следует набрать значение pHи и нажать ВВОД. З  начение pHи будет занесено в память прибора, и прибор вернётся в меню "Градуировка". начение pHи будет занесено в память прибора, и прибор вернётся в меню "Градуировка".Д  ля выхода в меню "Градуировка" без записи нового значения нажмите клавишу ВЫХОД. ля выхода в меню "Градуировка" без записи нового значения нажмите клавишу ВЫХОД.Ввод параметров стандартного раствора: Основное меню → Градуировка → Стандартный раствор Параметры стандартного раствора используются для получения очередной точки градуировочного графика. Для градуировки электродной системы необходимо ввести параметры двух или более стандартных растворов. Если параметры стандартных растворов не установлены, или введены параметры только одного раствора, прибор в режиме "Измерение" позволяет проводить измерение ЭДС электродной системы. 2.4.5. Измерение Назначение режима: В этом режиме прибор измеряет и выводит на индикатор результаты измерения ЭДС электродной системы или значения активности pH. Дополнительно выводится значение температуры. В  ход в режим осуществляется выбором пункта "Измерение" основного меню. ход в режим осуществляется выбором пункта "Измерение" основного меню. Перед проведением измерения следует провести настройку прибора и градуировку электродной системы. Автоматическая температурная компенсация: Основное меню → Измерение → ТК А  втоматическая температурная компенсация (ТК) вносится в результат измерения pH, позволяя учесть влияние температуры на результат измерения. втоматическая температурная компенсация (ТК) вносится в результат измерения pH, позволяя учесть влияние температуры на результат измерения.Е  сли проведена градуировка (введены параметры двух или более стандартных растворов) и введено значение pH изопотенциальной точки, в верхней строке выводится переключатель состояния автоматической температурной компенсации – символ сли проведена градуировка (введены параметры двух или более стандартных растворов) и введено значение pH изопотенциальной точки, в верхней строке выводится переключатель состояния автоматической температурной компенсации – символ 3. Описание электрода 3.1. Назначение Электрод стеклянный комбинированный лабораторный ЭСК-10603 со встроенным одноключевым электродом сравнения предназначен совместно с электронным преобразователем (например, иономером или рН-метром) для измерения активности ионов водорода (рН). Электрод является прибором общего назначения для использования в научных и промышленных аналитических лабораториях. Может применяться взамен электродной пары ЭСЛ-43-07 и ЭВЛ-1М3. Электрод изготавливается в соответствии с ГОСТ 22261-94 и техническими условиями ТУ 4215-004-35918409-02. 3.4. Устройство Комбинированные электроды представляют собой датчик, объединяющий в одном корпусе измерительный электрод и электрод сравнения. Электрод состоит из стеклянного корпуса (2, рис 16), в нижней части которого расположена сферическая рабочая мембрана (5). В верхней части электрода расположен резиновый колпачок (7), из которого выходит соединительный кабель (6). Для обеспечения возможности подключения электрода к преобразователям различных типов на кабель могут устанавливаться разные разъемы. Внутри корпуса смонтирован двухключевой хлорсеребряный электрод сравнения. Этот электрод состоит из стеклянной трубки (3), заполненной 3М раствором КСl. В трубке установлен хлорсеребряный полуэлемент, а в нижнюю ее часть впаян керамический электролитический ключ (внутренний). Полость корпуса датчика заполнена электролитом, а в нижней его части расположен второй (внешний) электролитический ключ (9) выполненный из пористой керамики. Таким образом, встроенный электрод сравнения состоит из двух емкостей (внутренней и внешней), заполненных электролитом и разделенных пористой керамической перегородкой. С анализируемым раствором контакт осуществляется через вторую пористую перегородку (9). Внутренняя часть электрода сравнения заполняется однократно при сборке изготовителем, внешняя часть (солевой мостик) перезаполняемая. Для этого в корпусе датчика имеется отверстие (8), закрываемое защитным кольцом (1). Заправлять электрод сравнения рекомендуется 3М раствором КСl. Однако, в случае необходимости, допустимо временное его заполнение растворами с другой концентрацией КСl (в том числе насыщенным), а также другими равнопереносящими электролитами (KNO3, NH4NO3, NH4Cl и др.) разной концентрации.  Рис. 16. Комбинированный стеклянный электрод 1 – защитное кольцо, 2 – стеклянный корпус, 3 – стеклянная трубка, 4 – , 5 – сферическая рабочая мембрана, 6 – соединительный кабель, 7 – резиновый колпачок, 8 – отверстие, 9 – пористая перегородка, 10 – 4. Описание датчика температуры рН метр поставляется в комплекте совместно с датчиком температуры МУЛЬТИТЕСТ ДТУ-3-01. Датчик температуры ДТУ-3-01 является первичным преобразователем величины температуры в значение электрического сопротивления. Датчик предназначен для измерения температуры совместно с измерительными приборами МУЛЬТИТЕСТ. Датчики одного конструктивного исполнения являются взаимозаменяемыми. 5. Имитатор Имитатор И-02 электродов предназначен для проверки работоспособности pH-метров и других лабораторных измерительных приборов. При помощи имитатора И-02 электродов и электродной системы можно проконтролировать: градуировку pH-метров и pX-метров в производственных и лабораторных условиях; помехозащищенность pH-метров и pX-метров; исправность соединительной линии «электрод-преобразователь». 6. Ход работы
|
