Реферат. анжела химия реферат. Гап оу колледж туризма и гостиничного сервиса Санкт петербурга
 Скачать 0.86 Mb. Скачать 0.86 Mb.
|
     ГАП ОУ колледж туризма и гостиничного сервиса Санкт -Петербурга Комитет по образованию Физико-химические процессы в технологии приготовления продуктов
2022 1) Концентрация раствора (С) – это отношение количества растворенного вещества к объему раствора, показывает количество вещества в единице объема раствора.  2) Массовая доля — это отношение растворенного вещества к массе раствора. Она может измеряться в процентах (от 0 до 100%) или в долях от единицы (от 0 до 1)  . .3) Растворимость – это способность веществ растворяться друг в друге, количественно характеризуется коэффициентом растворимости (к или р) - это масса растворённого вещества ,приходящаяся на 100 или 1000г растворителя, в насыщенном растворе - при определённой температуре. Растворимость вещества зависит от различных факторов: природы вещества и растворителя, от агрегатного состояния, от температуры и давления (для газов).   4) Плазмолиз – процесс отделения протопласта от оболочки клетки, погруженной в гипертонический раствор, то есть раствор, концентрация солей которого больше таковой клеточного сока. 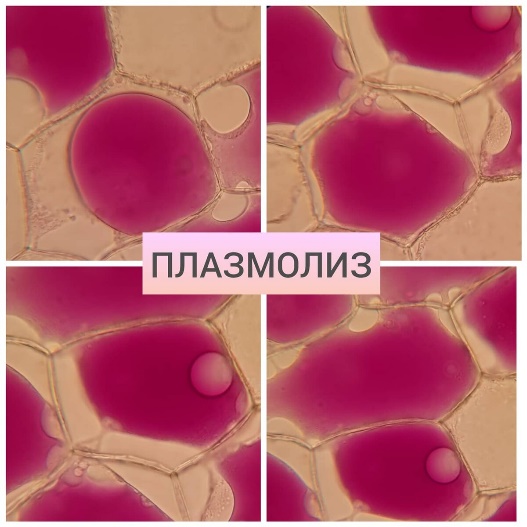 1. Он играет важнейшую роль в сохранении мяса, желе и других пищевых продуктов и тем самым предотвращает их разрушение бактериями и грибками. Засолка пищевых продуктов (подлежащих консервированию) повышает осмотическое давление консервирующей среды. Бактерии и грибы подвергаются плазмолизу и погибают из-за экзосмоса. 2. Плазмолиз также участвует в уничтожении сорняков на газонах, в садах и на сельскохозяйственных полях химическими ядовитыми веществами. 3. Это помогает предотвратить рост растений в трещинах стен. Засолка таких растений вызывает плазмолиз, и нежелательные растения погибают. 5)Гидрофильные вещества – хорошо растворимые в воде вещества, молекулы которых полярны и легко соединяются с молекулами воды. Примеры ; сахара ,аминокислоты ,органические кислоты АммиакАммиак, NH3, является гидрофильным, поскольку его молекула может образовывать несколько водородных связей с водой. Это делает его очень растворимым в воде как в газообразном, так и в жидком состоянии. Щавелевая кислотаЩавелевая кислота, H2C2ИЛИ4, является гидрофильным, поскольку его твердое вещество хорошо растворяется в воде из-за водородных связей, которые он может образовывать с двумя своими группами -COOH. МетанолМетанол, CH3ОН является гидрофильным благодаря своей ОН-группе. СпиртыСпирты обычно являются гидрофильными веществами, если их углеродный скелет не очень большой. Например, 1-пропанол и 2-пропанол смешиваются с водой, но это не относится к 1-бутанолу, смешиваемость которого снижена из-за его более длинной углеродной цепи. КрахмалКрахмал является примером гидрофильного полимера, поскольку его звенья глюкозы имеют несколько групп ОН, с которыми он образует водородные связи с молекулами воды. ДеревоДревесина гидрофильна и, хотя она не растворяется в воде, быстро намокает, если на нее не наносить гидрофобные покрытия. ПротеинБелки имеют полярные группы, тесно связанные с водой. Следовательно, его взаимодействие с молекулами воды эффективно. Однако это не означает, что все белки растворимы в воде, поскольку их структуры (третичные и четвертичные) играют фундаментальную роль в этом процессе растворения. СтеклоСтекло является гидрофильным материалом, потому что, хотя оно состоит не из молекул, а из сеток SiO2 Трехмерные атомы кислорода могут принимать водородные связи из воды. Это причина того, что стеклянные очки потеют во влажной среде.  6) Катализ – это реакция, ускоренная с помощью специального соединения – катализатора. Он применяется во многих природных и промышленных реакциях.   7) Константа равновесия – это отношение произведения равновесных концентраций продуктов реакции, взятых в степени их стехиометрических коэффициентов к произведению равновесных концентраций исходных веществ, взятых в степени их стехиометрических коэффициентов.  8) Выпаривание — это процесс концентрирования растворов твердых нелетучих веществ путем удаления жидкого растворителя в виде паров. Сущность выпаривания заключается в переводе растворителя в парообразное состояние и отводе полученного пара от оставшегося сконцентрированного раствора.  При выпаривании растворов твердых веществ в ряде пищевых производств достигают насыщения раствора; при дальнейшем удалении растворителя из такого раствора происходит кристаллизация, в результате которой выделяется растворенное вещество. Выпаривание применяют для повышения концентрации разбавленных растворов или выделения из них растворенного вещества путем кристаллизации. Процесс выпаривания широко используют в сахарном и консервном производствах при концентрировании сахарных и томатных соков, молока и др. В пищевой технологии выпаривают, как правило, водные растворы. Выпаривание проводят в выпарных аппаратах. Процесс выпаривания может проводиться непрерывно и периодически. Аппараты периодического действия используют в основном в производствах малого масштаба. Выпаривание осуществляют как под вакуумом, так и при атмосферном и избыточном давлениях. Выпаривание под вакуумом позволяет снизить температуру кипения раствора, что особенно важно при выпаривании пищевых растворов, которые особенно чувствительны к высоким температурам. Применение вакуума позволяет увеличить движущую силу теплопередачи и, как следствие, уменьшить площадь поверхности выпарных аппаратов. |
