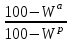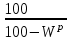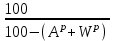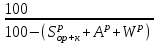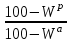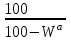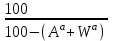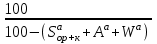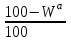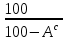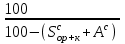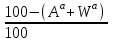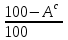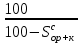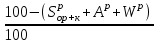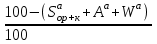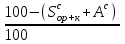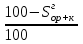Эссе. Характиристики органического топлива. 1 Состав топлива
 Скачать 125.6 Kb. Скачать 125.6 Kb.
|
|
4. ОСНАВНЫЕ ТЕПЛОТЕХНИЧЕСКИЕ ХАРАКТИРИСТИКИ ОРГАНИЧЕСКОГО ТОПЛИВА. 4.1 Состав топлива Состав топлива является его важнейшей начальной характеристикой, определяющей в дальнейшем целый ряд показателей, используемых для анализа процессов, происходящих в различных топливо использующих устройствах или при его технологической переработке. Твердые и жидкие топлива состоят из весьма большого количества сложных соединений, молекулярное строение и минералогический состав которых изучены недостаточно. В состав этих топлив также входят влага и минеральные примеси, образующие при сжигании топлива позволяет определить процентное содержание в его массе таких элементов как углерод С, водород Н, кислород О, азот N, сера S, а также зола А и влага W. Топливо в том виде, в каком оно поступает непосредственно к потребителю называется рабочим топливом, его масса – рабочей массой. Процентное содержание указанных выше элементов, выраженное в отношении к рабочей массе топлива, называется элементарным составом рабочей массы топлива. Cр +Hр +Oр +Nр + S р ор+к +Aр +Wр = 100% В выражении (3.1) индекс р указывает на то, что элементарный состав относится к рабочей массе топлива. В элементарный состав приведенной выше рабочей массы топлива входит сера, которая в твердых топливах встречается в трех видах: органическая Sор, колчеданная Sк и сульфатная Sс. Органическая сера входит в состав высокомолекулярных органических соединений топлива.Колчеданная сера представляет собой сульфиды металлов (чаще всего железный колчедан FeS2). Органическая и колчеданная сера при горении топлива окисляются с выделением тепла. Сульфатная сера встречается в топливах в виде сульфатов СаSO4, MgSO4 и т.д. Эти соединения при горении почти разлагаются и переходят в золу. В жидком топливе сера содержится в виде сероорганических соединеий, элементрарной серы и сероводорода Н2S. Для одного и того же топлива количество минеральных примесей и влажность могут изменяться в достаточно широких пределах в зависимости от условий его добычи, транспортировки, хранения и т.п. В связи с этим для удобства сравнительной оценки теплотехнических характеристик различных сортов твердого топлива введены условные понятия аналитической, сухой, сухой беззольной (горючей) и органической масс топлива (рис.3.1.). Жидкое топливо характеризуется составом рабочей и сухой массы. Для приготовления пробы топлива, используемый при лабораторных анализах, навеска топлива высушивается в лаборатории в естественных условиях до постоянной массы при комнатной температуре и влажности воздуха. Элементарный состав аналитической сухой массы топлива записывается в виде. Cа +Hа +Oа +Nа + S а ор+к+Wа +Aа =100% (4.2) Сухая масса топлива получается после удаления из него влаги путем искусственного высушивания топлива при t≥105°C Cс +Hс +Oс+Nс + Sс ор+к +Aс = 100% (4.3) Безводное и беззольное топливо характеризуется элементарным химичекским составом сухой беззольной (горючей) массы. Cг +Hг +Oг +Nг + Sг ор+к= 100% (4.4) Таблица 4.1 – Расчетные массы топлива и их состав 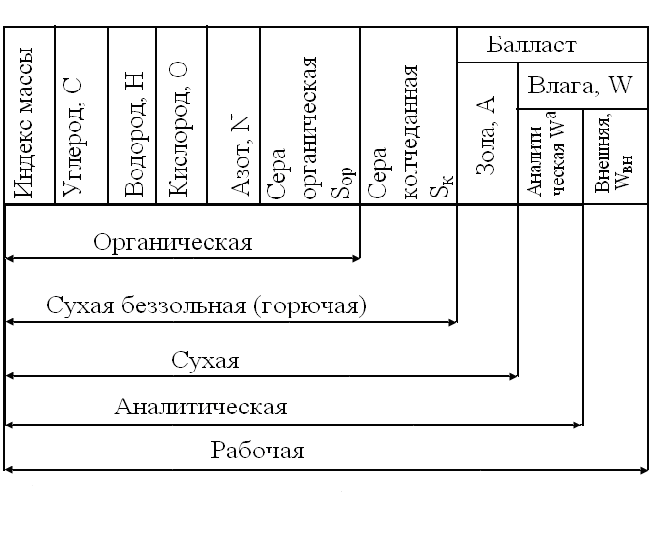 Понятие горючей массы топлива является условным, так как в нее входит азот и кислород, которые находятся в связанном состоянии с горючими элементами топлива. Исключение из элементарного состава горючей массы топлива колчеданной серы позволяет получить состав органической массы топлива. Cо+Hо +Oо +Nо + Sо ор+к= 100% (4.5) Путем несложных расчетов можно произвести пересчет элементарного состава топлива с одной массы на другую, имея в виду, что они связаны простыми пропорциональными соотношениями. Так, например: 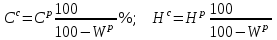 (4.6) (4.6)В табл. 3.1. приведены множители для пересчета состава топлива. Для одного и того же топлива состав горючей массы является величиной постоянной, однако элементарный состав его сухой и рабочей массы может изменяться в достаточно широких пределах из-зи нестабильности величин Ас и Wр. Если известен состав рабочей массы конкретного топлива при Ар1 и Wр1, а у потребителя это же топливо имеет изменившиеся зольность и влажность (Ар2 и Wр2), то пересчет состава топлива производится по формулам: 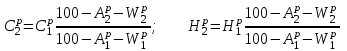 Таблица 4.1. - Множители для пересчета состава топлива с одной массы на другую
Правильность пересчета проверяется выполнением равенства Cр2 +Hр2 +Oр2 +Nр2 + Sр(ор+к)2 +Aр2 +Wр2 = 100% Для смесидвух твердых, жидких или твердого и жидкого топлив, заданный массовыми долями m1 и m2=1-m1 элементарный состав ее рабочей (или любой другой) массы определяется по формуле смещения. Качество твердого и жидкого топлива как источника тепловой энергии в значительной мере определяется его элементарным составом, основным горючим компонентом этих топлив является углерод. При полном сгорании углерода выделяется 34,4 МДж/кг теплоты6 что с учетом его значительного содержания в горючей массе топлива (50% в древесине до 95% в антраците) обеспечивает преимущественную долю общего тепловыделения топлива. Вторым по назначению горючим компонентом топлива является водород, при сгорании которого выделяется 119 МДж/кг. Содержание водорода в горючей массе твердых и жидких топлив изменяется от 2 (антрацит) до 10,5 % (мазут). Кислород и азот является нежелательными составляющими горючей массы топлива, так как их наличие снижает в топливе содержание основных горючих элементов – углерода и водорода. Наличие кислорода в органической массе топлива свидетельствует о частичном содержании углерода и водорода в окисленном состоянии, а это уменьшает теплоту сгорания топлива. Содержание кислорода в топливе уменьшается по мере увеличения геологического возраста топлива. Азот горючей массы при сгорания топлива переходит в продукты сгорания в газообразном состоянии. Кислород и азот иногда называют внутренним или органическим балластом топлива. Входящая в состав твердых и жидких топлив так называемая горячая сера (органическая и колчеданная) окисляется при горения топлива с образованием сернистого газа SO2. при этом выделяется 9,3 МДж/кг теплоты, что существенно меньше, чем при сгорании водорода или углерода. Частично сера сгорает с образованием серного ангидрида SO3, однако это в технических расчетах не учитывается. Наличие серы в топливе снижает содержание водорода и углерода в горючей массе, а значит, уменьшает и теплоту сгорания топлива. Кроме того, образующиеся окислы среды способствуют коррозии металлических элементов топливоиспользующих установок, отрицательно влияют на окружающую среду. Содержание серы в горючей массе твердых и жидких топлив изменяется от 0,5 до 7 % (в горючих сланцах 15%). Зола и влага являются нежелательными компонентами состава топлива, его внешним балластом. Повышение содержания золы и влаги в рабочей массе топлива приводит, к соответствующему уменьшению его горючей части, а значит к снижению тепловыделения единицей массы топлива. При сжигании влажных топлив затрачивается определенное количество теплоты на нагрев и испарение влаги и перегрев водяных паров, что дополнительно уменьшает количество выделившиеся теплоты и соответственно температуру горения. Газовое топливо (природное или искусственное) представляет собой физическую смесь горючих и негорючих индивидуальных газов и водяных паров. К индивидуальным горючим газам относятся: окись углерода СО, водород Н2, метан СН4, сероводород Н2S, разнообразные предельные и непредельные углеводороды СmНn. К негорючим газам относятся: двуокись углерода СО2, сернистый газ SО2, азот N2 и кислород О2. Состав газового топлива определяется процентным содержанием в нем соответствующих газов и для сухого топлива в общем случае представляется в виде: СО+ Н2+ СН4 +Σ СmНn+ Н2S+СО2 + N2 + О2=100% (4.8) Влагосодержание газового топлива dт, г/м3 определяется количеством водяных паров, приходящихся на 1 м3 сухого газового топлива, приведенного к нормальным условиям – температуре 273°C (0°C) и давлению 0,1013 МПа (760мм рт.ст.). При наличии в газовом топливе других примесей (угольной и минеральной пыли, паров смолы и т.п.) их содержание выражается аналогично содержанию водяных паров. Иногда в топливоиспользующих установках сжигается смесь газовых топлив (коксового и доменного газов, природного и коксового и т.д.). Состав смеси двух газовых топлив, заданный объемными долями n1 и n2=1-n1, определяется по формулам смещения аналогично как для твердого топлива. 6. ТЕПЛОТА СГОРАНИЯ ТОПЛИВА Теплота сгорания представляет собой количество теплоты, выделяющееся при полном сгорании массовой (для газовых топлив объемной) единицы количества топлива, МДж/кг или МДж/м3. При сжигании топлива теплота выделяется в результате экзотермических реакций окисления горючих компонентов горючей массы твердого или жидкого топлива (углерода, водорода и серы) или в результате окисления горючих газов, входящих в состав газового топлива (окиси углерода, водорода, метана и других углеводородных газов, сероводорода) Теплота сгорания может относиться к рабочей, аналитической, сухой, горючей или органической массе топлива и обозначается соответственно Qp, Qa, Qc, Qr и Q°. В технических расчетах используется значение теплоты сгорания, отнесенное к рабочей массе топлива. В твердых и жидких топливах горючие элементы являются составной частью весьма сложных и различных по своему химическому строению соединений, учесть все разнообразие которых не представляется возможным. Поэтому точное расчетное определение теплоты сгорания этих топлив невозможно. Теплоту сгорания этих топлив определяют экспериментально калориметрическим методам, сущность которого состоит в сжигании навески топлива b атмосфере кислорода в специальном сосуде (калориметрической бомбе) и определении с помощью водяного калориметра количества выделившейся при этом теплоты. По результатам измерений рассчитывается теплота сгорания топлива, которая называется теплотой сгорания по калориметрической бомбе Q б. Количество теплоты, выделившееся при полном сгорании топлива зависит от того, b каком агрегатном состоянии находится в продуктах сгорания влага (как выделившаяся из топлива, так и образовавшаяся в результате сгорания водорода) — в парообразном или жидком. Если в продуктах сгорания все водяные пары конденсируются и образуют жидкую фазу (температура газов ниже температуры точки росы водяного пара), то теплота сгорания называется высшей QB. Если же конденсации водяного пара не происходит, то теплоту сгорания называют низшей_Qн. Разница между высшей и низшей теплотами сгорания равна теплоте конденсации водяных паров, содержащихся b продуктах сгорания топлив. Аналитически связь между значениями высшей и низшей теплоте сгорания определяется выражением 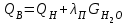 , (6.9) , (6.9)где 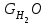 — масса влаги, содержащейся в продуктах сгорания 1 кг топлива, кг; — масса влаги, содержащейся в продуктах сгорания 1 кг топлива, кг;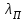 — теплота конденсации водяного пара, принимаемая равной 2,51 МДж/кг. — теплота конденсации водяного пара, принимаемая равной 2,51 МДж/кг.Величина Gн2о при сжигании твердого или жидкого топлива, кг/кг, 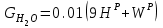 (6.10) (6.10)а при сжигании газового топлива, кг/м3, GH2O=0.00804(H2+2CH4+ ΣCmHn+H2S) (6.11) где Нр и Wp — содержание водорода и влаги в рабочей массе топлива, %; Н2, СН4, CmHn, H2S — концентрации соответствующих газов в газовом топливе, % Экспериментальное значение теплоты сгорания по бомбе, хотя и определяется в условиях конденсации водяных паров, находящихся в продуктах сгорания, не совпадает с величиной QB, так как при сгорании топлива в калориметрической бомбе в кислородной среде дополнительно протекают экзотермические реакции образования серной и азотной кислот, отсутствующие в реальных условиях горения топлива. Поэтому Qб оказывается больше, чем QB для одного и того же топлива, на величину теплот образования указанных кислот. Соотношение между значениями Q6 и QB выражается формулой 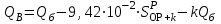 (6.12) (6.12)где 9,42*10-2Spop+k+K — теплота образования серной кислоты, МДж/кг, rQб — теплота образования азотной кислоты, МДж/кг. Коэффициент k принимается равным 0,001 для тощих каменных углей, антрацитов и жидких топлив и 0,0015 для всех остальных углей, горючих сланцев и торфа При подсчете QPB для горючих сланцев дополнительно учитывается, что часть теплоты сгорания расходуется на разложение карбонатов минеральной части этого топлива Формула для расчета горючих сланцев (и других топлив с содержанием карбонатов более 2%), МДж/кг, QPв= Q6— (94,2*10-3 Spop+k +rQб)-40,6*10-3(СО2)к, (6.13) где 40,6* 10-3(СО2)К-теплота разложения карбонатов, МДж/кг; (СО2)К - содержание СО2 карбонатов в топливе, %. В реальных условиях топливоиспользующих установок продукты сгорания топлив в подавляющем большинстве случаев покидают установки при температуре существенно более высокой, чем температура точки росы содержащихся в них водяных паров При этом теплота конденсации водяных паров полезно не используется и в тепловых расчетах не должна учитываться В связи с этим в теплотехнических расчетах используется величина QpH. Для конкретного топлива связь между значением QpH и значениями низших теплоте сгорания его сухой QCH и горючей QrH масс выражается формулами, МДж/кг, QpH =QCH 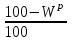 -0,0251Wp , QCH =QrH -0,0251Wp , QCH =QrH 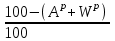 -0,0251Wp -0,0251Wp (6.14) При изменившемся содержании золы и влаги в рабочей массе конкретного топлива новое значение теплоты сгорания, МДж/кг, определяется по формуле 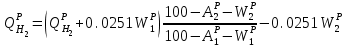 (6.15) (6.15)где QpH1 — теплота сгорания рабочей массы топлива при Ap1, Wp1, МДж/кг; Ap2, Wp2 — соответственно новые значения зольности и влажности топлива, %. Выражение (3.15) получено из следующих соображений. Для одного и того же топлива с различным содержанием балласта справедливы соотношения: 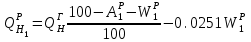 или 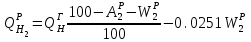 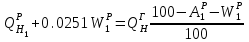 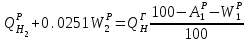 Если взять отношение левых и правых частей этих выражений и учесть, что QrH для обоих топлив есть величина постоянная, то легко получить выражение (3.13) При отсутствии экспериментальных данных по теплоте сгорания какого-либо твердого или жидкого топлива для приближенных расчетов этой величины может быть использована эмпирическая формула Менделеева, МДж/кг, QpH = 0,339CP+l,03Hp—0,109(Ор—Sрор+к) — 0,0251Wp (6.16) Низшая теплота сгорания сухого газового топлива определяется аналитически, как сумма теплот сгорания входящих в него индивидуальных горючих газов с учетом концентрации, МДж/м3, QCH=0.01(QCH4CH4+QCOCO+QH2H2+ QCmHnCmHn++ QH2SH2S), (6.17) где QCH4, Qco, QH2, QcmHn —низшие теплоты сгорания соответствующих газов, МДж/м3; СН4, СО, H2, СmНn, H2S — содержание соответствующих газов в сухом газовом топливе, %. Аналогичную структуру имеет формула для вычисления QCB. Теплота сгорания смеси двух твердых, жидких или условной смеси твердого и жидкого топлив определяется суммированием их теплот сгорания с учетом массовых долей этих топлив в смеси, МДж/кг, Qph cm=m1QpH1+(1-m2) QpH2, (6.18) где m1 — массовая доля первого топлива в смеси; QpH1, и QpH2 — теплоты сгорания первого и второго топлив, МДж/кг. Если смесь топлив задана в долях по тепловыделению каждого из них q1 и q2 = 1—q1 (доле первого и второго топлива в суммарном тепловыделении смеси этих топлив), то для перехода к массовым долям используется зависимость 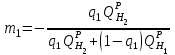 (6.19) (6.19)Выражение (3.19) получено из следующих соображений. Доля первого топлива в суммарном тепловыделении смеси описывается выражением 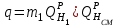 где QPHCM — теплота сгорания смеси, МДж/кг. С учетом формулы (3.18) 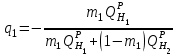 Решив полученное выражение относительно m1, получим зависимость (3.19) Аналогичные формулы устанавливают связь между объемными долями двух газовых топлив, если задана доля участия в общем тепловыделении одного из них. При совместном сжигании твердого (жидкого) топлива с газовым расчеты горения приводятся на 1 кг твердого (жидкого) топлива с учетом удельного количества газового топлива, в смеси, м3/кг При этом рассчитывается условная теплота сгорания смеси, МДж/кг, твердого (жидкого) топлива QpHСМ = QpH+хQcH. (6.20) где QPH и QCH — теплота сгорания соответственно твердого (жидкого), МДж/кг, и газового, МДж/м3, топлив, х — количество газового топлива, приходящееся на 1 кг твердого (жидкого) топлива, м3. Теплота сгорания различных топлив колеблется в очень широких пределах. Для сравнения топлив по энергетической ценности, оценке эффективности их использования, а также для сопоставления различных видов топлива и подсчетов потребности в топливе используется понятие условное топливо. Условному топливу присвоена теплота сгорания (2усл = = 29,33 МДж/кг. Перечет расхода реального топлива в условное производится по формуле В усл =ВQ pH/Qусл, (6.21) где B — расход реального топлива с теплотой сгорания QpH. Отношение QpH/Qyсл называют тепловым эквивалентом топлива Э, т.е. Вусл = В*Э. Учитывая большое влияние влажности и зольности на теплоту сгорания топлива, для сравнительной оценки различных видов органического топлива используются также приведенные характеристики влажности Wпи зольности Ап, определяемые по формулам Wn = Wp / QpН , Аn =Аp / QpН (%*кг)/МДж (6.22) Приведенные характеристики Ап и Wп позволяют сравнивать различные топлива в сопоставимых единицах. При Wп<0,7 (%*кг)/МДж топлива называются маловлажными, при 0,7<Wп<1,89 — средней влажности, а при Wn>1,89 — высоковлажными. Топлива с AП <1,0 считаются малозольными (антрациты и большая часть каменных углей). Бурые угли имеют Aп=1,9—2,4, а горючие сланцы — Ап =5-10 (%*кг)/МДж. Высокие значения Wn и Aп свидетельствуют о сильном балластировании топлива негорючими составляющими, а значит о его пониженной энергетической ценности. Такие топлива экономически нецелесообразно транспортировать на значительные расстояния. Они должны использоваться вблизи места добычи или получения, и поэтому часто называются местными топливами. 7. ЛЕТУЧИЕ ВЕЩЕСТВА И КОКС ТВЕРДОГО ТОПЛИВА Все твердые топлива при нагревании без доступа воздуха подвергаются термическому распаду с выделением горючих газов — окиси углерода СО, водорода H2 , различных углеводородов CnHm и негорючих газов — азота N2, кислорода О2 ,углекислого газа СО2, водяных паров. Выделение этих газов называется выходом летучих веществ. Твердый остаток, образующий после выделения летучих веществ, называется коксом. В состав кокса входит углерод и прокаленные минеральные примеси (зола). Выход летучих обычно относят на горючую массу топлива и обозначают Vг. Выход летучих веществ и свойства коксового остаткаa являются важными теплотехническими характеристиками топлива, определяющими условия организации его сжигания и термохимической переработки. Летучие вещества играют существенную роль при воспламенении и на начальных стадиях горения, в значительной мере определяют реакционную способность твердых топлив — их способность к воспламенению и активному горению. По мере увеличения геологического возраста природных твердых топлив выход летучих снижается, но относительное содержание горючих газов в их составе возрастает, что ведет к увеличению теплоты сгорания летучих веществ. Одновременно повышается температура 'начала выхода летучих. Таблица 7.1 - Характеристики выхода летучих
Средние показатели по выходу летучих и примерные температуры начала их выделения для некоторых видов топлива приведены табл. 3.2. Характер твердого горючего остатка играет решающую роль при определении рационального пути использования топлива. Угли со сплавленным коксовым остатком являются ценным технологическим топливом и используются в первую очередь для производства металлургического кокса. ЗОЛА И ВЛАГА ТОПЛИВА Зола представляет собой минеральный остаток, получаемый при полном сгорании топлива. Основой образования золы является наличие минеральных примесей. Различают первичную, вторичную и третичную золу. Первичная зола образуется из минеральных примесей, входящих в состав веществ топливообразователей; вторичная зола— из ,минеральных примосей, попадающих в топливо в процессе топливо-образования. и третичная — в момент добычи. К таким примесям относятся сульфаты, карбонаты, силикаты, фосфаты, хлорид, пириты и другие соединения. В состав золы входят также Аl2О3, СаО, Na2О, К2О, SiO2, FeO и др. Содержание минеральных примесей в твердых топливах изменяется в широких пределах: в древесном топливе 1-2%, в горючих сланцах до 70%, в угле 10-40%, в жидком топливе до 1%. Зольность топлива определяется в лабораторных условиях сжиганием представительно высушенной пробы и последующим прокалыванием полученного остатка в платиновом тигле до постоянной массы при 500°C (для мазутов) или 850°C (для твердого топлива). Взвешивание негорючего осадка позволяет определить содержание золы в исходном топливе. В процессе горения топлива минеральные примеси могут из твердого состояния переходить в жидкое, образуя раствор минералов. Называемый шлаком. Важной характеристикой золы является ее плавкость. В лабораторных условиях плавкость золы определяют путем нагревания в электрической печи в полувосстановительной газовой среде (СО-60% и СО2 -10%) пирамидки стандартных размеров, сформированной из мелкораздробленной пробы испытуемой золы. Температура, при которой пирамидка начинает сгибаться или вершина ее закругляется, носит название температуры начала деформации золы t1. Температура, при которой вершина пирамидки наклоняется до ее основания, называется температурой начала размягчения золы t2. температура начала жидкоплавкого состояния t3 соответствует температуре, при которой золовая пирамидка растекается по подставке. По характеристике плавкости золы твердые топлива разделяются на следующие группы: с легкоплавкой золой (t3 ≤1350°C) с золой средней плавкости (t3 =1350-1450°C), с тугоплавкой золой (t3≥1450°C). Повышенное содержание золы в топливе снижает технико-экономические показатели топливоиспользующих установок за счет увеличений затрат на шлако- и золоудаление и газоочистку, а также за счет увеличение потерь тепла со шлаком и золой. Влагу твердого топлива принято разделять на внешнюю и внутреннюю. К внешней влаге относят поверхностные и грунтовые воды, влагу атмосферного воздуха, которые при транспортировке и хранении топлива увлажняют его поверхность, проникают в капилляры и поры, особенно сильно развитые у торфа поверхность топлива резко возрастает, что приводит к увеличению содержания внешней влаги. Внешняя влага может быть удалена подсушкой топлива. К внутренней влаге относят коллоидную и гидратную (кристаллогидратную) влагу. Коллоидная влага равномерно распределена по всей массе топлива, а ее количество зависит от химической природы и состава топлива. По мере увеличения геологического возраста топлива количество коллоидной влаги в нем существенно сокращается. Гидратная влага входит в структуру химических соединений минеральной части топлива (главным образом сульфата кальция). Количество гидратной влаги в топливе относительно невелико, но ее удаление требует нагревания топлива до высоких температур. При хранении на воздухе переувлажненное топливо теряет, а подсушенное приобретает влагу до тех пор, пока давление насыщенного водяного пара над поверхностью топлива не сравняется с парциальным давлением паров во влажном воздухе. Топливо с установившейся в естественных условиях влажностью называют воздушно-сухим. Повышение влажности приводит к снижению теплоты сгорания топлива, увеличению объема продуктов сгорания и, как следствие этого, уменьшению температуры горения. В результате снижается производительность топливоиспользующих установок и увеличивается удельные ( на единицу продукции ) расходы топлива, а в зимние время приводит к его смерзаемости, что резко затрудняет условия транспорта и пользования топлива. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||