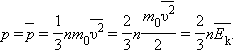Лекция Идеальный газ. Идеальный газ. Идеальный газ. Основное уравнение мкт
 Скачать 120.24 Kb. Скачать 120.24 Kb.
|
|
Идеальный газ. Основное уравнение МКТ Изучение свойств веществ с точки зрения МКТ начнем с изучения свойств газов. Простейшей моделью молекулярно-кинетической теории газов является модель идеального газа. Модель идеального газа достаточно хорошо описывает поведение реальных газов в широком диапазоне давлений и температур. В кинетической модели идеального газа молекулы рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений. 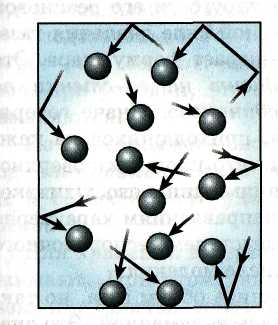 Суммарный объем всех молекул предполагается малым по сравнению с объемом сосуда, в котором находится газ. Получить на практике такой газ можно откачав из закрытого сосуда большую часть молекул газа. Идеальный газ – это модель газа, взаимодействие между молекулами которого пренебрежимо мало. Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между: микроскопическими параметрами (масса, скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, объем, температура). В результате каждого столкновения между молекулами и молекул со стенкой скорости молекул могут изменяться по модулю и по направлению; на интервалах между последовательными столкновениями молекулы движутся равномерно и прямолинейно. В модели идеального газа предполагается, что все столкновения происходят по законам упругого удара, т. е. подчиняются законам механики Ньютона. И 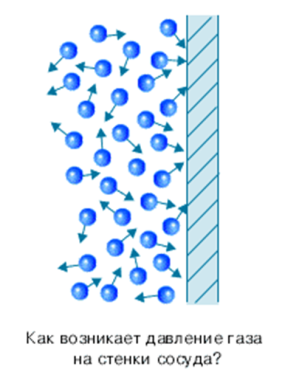 спользуя модель идеального газа, вычислим давление газа на стенку сосуда. спользуя модель идеального газа, вычислим давление газа на стенку сосуда. Вследствие теплового движения, частицы газа время от времени ударяются о стенки сосуда. При каждом ударе молекулы действуют на стенку сосуда с некоторой силой. Складываясь друг с другом, силы ударов отдельных частиц образуют некоторую силу давления, постоянно действующую на стенку. 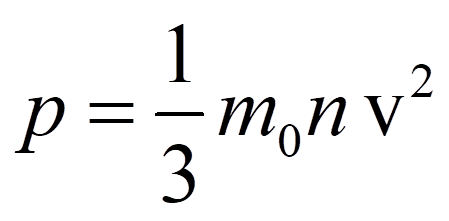
где m0 - масса молекулы  n - концентрация молекул формуле, которую можно найти по формуле n - концентрация молекул формуле, которую можно найти по формуле( N – число молекул в сосуде в сосуде неизменного объема V ) Используя формулу кинетической энергии, получаем
Э Таким образом, давление газа равно двум третям средней кинетической энергии поступательного движения молекул, содержащихся в единице объема. 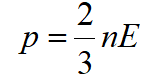 Выполните задания: 1. Запишите в рабочую тетрадь конспект лекции. 2. Ответьте на вопросы теста (письменно) Выполненное задания приносим в колледж на занятие. Примечание: По всем вопросам обращаться в сообщении на портале. Ответьте на вопросы теста. Для этого поставьте номер вопроса и запишите правильные ответы, их может быть несколько. ТЕСТ Вопрос 1 Укажите основные положения МКТ. Варианты ответов все вещества состоят из частиц частицы находятся в непрерывном тепловом движении между частицами действуют силы молекулярного взаимодействия частицы находятся в постоянном покое между частицами не действуют силы молекулярного взаимодействия между частицами преобладают гравитационные силы взаимодействия Вопрос 2 Идеальный газ - Варианты ответов это модель газа. молекулы газа можно считать МТ, которые хаотически движутся силы взаимодействия между молекулами идеального газа практически отсутствуют при столкновениях молекулы идеального газа ведут себя как неупругие шарики силы взаимодействия между молекулами идеального газа очень существенны Вопрос 3 Физические величины, которые характеризуют некоторое количество идеального газа как макроскопическую систему Варианты ответов Макроскопические параметры состояния идеального газа Микроскопические параметры состояния идеального газа Механическая система Термодинамические параметры Вопрос 4 Укажите отдельно макро- и микропараметры газа Варианты ответов Давление Объём Температура Масса молекулы Средняя скорость Импульс Кинетическая энергия Вопрос 5 Из основного уравнения молекулярно-кинетической теории ясно, что... Варианты ответов Давление газа прямо пропорционально средней кинетической энергии его молекул Давление газа обратно пропорционально концентрации Давление газа пропорционально силе, с которой молекулы ударяются о стенки сосуда Давление газа зависит от рода газа Давление газа зависит от концентрации его молекул Вопрос 6 Концентрация газа равна 3 · 1027 м-3, а средняя кинетическая энергия его молекул составляет 6 · 10-22 Дж. Какое давление ( в МПа) оказывает газ на стенки сосуда? В ответ запишите решение . Вопрос 7 Выберете верные утверждения. Варианты ответов Давление газа обусловлено соударениями его молекул о стенки сосуда. Давление газа не зависит от объёма, в который он помещен. Давление газа зависит от среднего значения квадрата скорости молекул. Давление газа в сосуде постоянно меняется, причём колебания давления являются хаотическими. Вопрос 8 Газ оказывает давление на стенки сосуда, равное 200 кПа. Найдите среднюю силу воздействия газа на стенки сосуда (в кН), если площадь стенок равна 0,01 м2. В ответ запишите решение. |