|
|
отчёт по комплексам. Лабораторная работа 3 Исследование комплексных соединений студент гр. Рги21 Жидкова П. С
Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский горный университет» 
Кафедра общей химии
ОТЧЕТ
ЛАБОРАТОРНАЯ РАБОТА №3
«Исследование комплексных соединений»
Выполнил: студент гр. РГИ-21 Жидкова П.С.
(номер группы) (подпись) (Ф.И.О.)
Проверил
руководитель работы: доцент ___________
(должность) (подпись) (Ф.И.О.)
Оценка:
Дата:
Санкт-Петербург
2021
Общие теоретические свойства:
Комплексными называют соединения, в структуре которых можно выделить центральный атом – акцептор электронов, находящийся в донорно-акцепторной связи с определенным числом доноров-лигандов. Лигандами могут быть как ионы, так и нейтральные молекулы. Центральный атом и лиганды образуют внутреннюю сферу комплексного соединения, которую при записи формулы выделяют квадратными скобками. Внутренняя сфера часто имеет заряд, который компенсируют противоположно заряженные ионы, располагающиеся во внешней сфере. Внешнесферные ионы не имеют связей с центральными атомами, а образуют ионные связи с комплексными ионами. Поэтому в полярных растворителях комплексные соединения диссоциируют на комплексный и внешнесферный ионы
Цель работы:
Познакомиться с методами получения комплексных соединений и их свойствами.
3. Порядок выполнения работы:
Опыт 1.Образование и разрушение амминокомплекса серебра.
Налить в пробирку 3−4 капли раствора нитрата серебра, добавить столько же
раствора хлорида натрия (или хлорида калия). Отметить выпадение осадка хлорида
серебра. Затем в вытяжном шкафу добавить в пробирку 3−5 капель концентрированного
раствора аммиака и несколько раз встряхнуть. Осадок должен раствориться вследствие
образования амминокомплекса серебра. Подкислить раствор аммиката серебра азотной кислотой.
Опыт 2. Образование и реакции амминокомплекса никеля.
Налить в пробирку 3−4 капли раствора сульфата никеля. Добавить каплю
разбавленного раствора аммиака, который находится в штативе с реактивами. В пробирке
образуется студенистый осадок сульфата гидроксоникеля. Добавить в вытяжном шкафу
4−10 капель концентрированного раствора аммиака до полного растворения осадка. К полученному раствору добавить 1 мл насыщенного раствора
бромида натрия (или бромида калия).
Опыт 6. Образование гидроксокомплекса цинка.
В пробирку налить 3−4 капли раствора сульфата цинка и добавить по каплям
раствор гидроксида натрия, находящийся в штативе с реактивами, до выпадения осадка
гидроксида цинка. Затем в вытяжном шкафу добавить по каплям 6 н. раствор едкого натра
до полного растворения осадка вследствие образования комплексного аниона
тетрагидроксоцинка (2−).
Опыт 7. Образование труднорастворимого гексацианоферрата
А. Налить в пробирку 3-4 капли раствора гексацианоферрата (II) калия K4[Fe(CN)6]. Добавить 2-3 капли раствора хлорида железа (III). Отметить окраску образующегося осадка берлинской лазури.
Б. Налить в пробирку 3-4 капли раствора гексацианоферрата (III) калия K3[Fe(CN)6]. Добавить 2-3 капли раствора сульфата железа (II). Отметить окраску образующегося осадка («турнбулева синь»).
4.Ход работы
Уравнения реакций в молекулярной и ионной форме, результаты проведения реакций:
Опыт 1. Образование и разрушение амминокомплекса серебра
AgNO3+NaCl = AgCl↓+NaNO3– образование осадка белого цвета
Ag++Cl-→AgCl↓
AgCl+2NH4OH = [Ag(NH3)2]Cl+2H2O – растворение осадка
AgCl+NH4++OH-→[Ag(NH3)2]++Cl-+H2O
[Ag(NH3)2]Cl+2HNO3 = 2NH4NO3 + AgCl↓ –образование осадка белого цвета
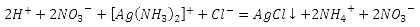
Опыт 2. Образование и реакции амминокомплекса никеля
2 NH4OH + 2 NiSO4 = (NH4)2SO4 + (NiOH)2SO4↓ – студенистый осадок
2Ni2++ SO42- + 2OH-→(NiOH)2SO4↓
(NiOH)2SO4 + 10NH4OH + (NH4)2SO4 = 2[Ni(NH3)6]SO4 + 12H2O – осадок растворился
[Ni(NH3)6]SO4+2KBr = [Ni(NH3)6]Br2↓+K2SO4 – осадок фиолетового цвета
[Ni(NH3)6]2+ +2Br-→[Ni(NH3)6]Br2↓
Опыт 6. Образование гидроксокомплекса цинка
ZnSO4+2NaOH→Zn(OH)2↓+Na2SO4 – студенистый осадок
Zn2++2OH-→Zn(OH)2↓
Zn(OH)2+NaOH(6N)→Na2[Zn(OH)4] – растворение осадка
Zn(OH)2+2OH-→[Zn(OH)4]2-
Опыт 7. Образование труднорастворимого гексацианоферрата (Ⅲ)
А.
3K4[Fe(CN)6]+4FeCl3=Fe4[Fe(CN)6]3+12KCl
Наблюдаем образование осадка темно-синего цвета («берлинская лазурь»). Реакция служит для обнаружения катионов Fe3+
4K++[Fe(CN)6]4-+Fe3++3Cl-→3K++3Cl-+ Fe[Fe(CN)6]↓
4K++[Fe(CN)6]4-+Fe3-→3K++ Fe[Fe(CN)6]↓
Б.
2K3[Fe(CN)6]+3FeSO4=Fe3[Fe(CN)6]2+3K2SO4
Наблюдаем образование осадка темно-синего цвета. Данная реакция служит для обнаружения катионов Fe2+
3K++[Fe(CN)6]3-+Fe2++SO42-→ Fe[Fe(CN)6]↓+2K++SO42-
+3K++[Fe(CN)6]3-+Fe2+-→ Fe[Fe(CN)6]↓+2K
Вывод:
В данной лабораторной работе я ознакомился с методами получения комплексных соединений и их свойствами, а также выяснил на практике как происходит их образование. |
|
|
 Скачать 44.6 Kb.
Скачать 44.6 Kb.
