получение этилена из этана. 1) ПОЛУЧЕНИЕ ЭТИЛЕНА ИЗ ЭТАНА. Материальный расчет
 Скачать 47.63 Kb. Скачать 47.63 Kb.
|
|
ПОЛУЧЕНИЕ ЭТИЛЕНА ИЗ ЭТАНА Пиролиз этана осуществляют в трубчатых печах в среде водяного пара при температуре 830-900°С и давлении, близком к атмосферному. МАТЕРИАЛЬНЫЙ РАСЧЕТ Исходные данные: годовая производительность установки по этилену 250000т; годовой фонд рабочего времени 8000ч; состав исходной этановой фракции(φi, %) :C2H4 – 0,73; C2H6 – 89,80; C3H6 – 4,69; C3H8 – 4,70; C4H8 – 0,08; массовое отношение водяной пар : этановая фракция = 0,4 : 1,0; температура процесса 845°С. Последовательность расчета: а) определяют степень конверсии этана в этилен по целевой реакций пиролиза; б) рассчитывают объемный расход компонентов этановой фракции на входе в трубчатую печь (основной аппарат пиролизной установки); в) определяют изменение состава газа в процессе пиролиза и состав газа на выходе из трубчатой печи. 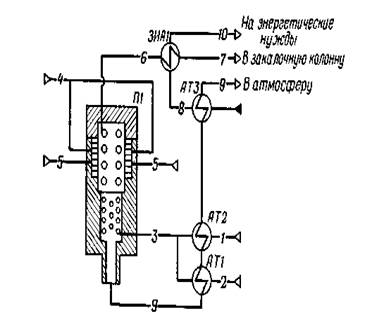 Схема потоков узла пиролиза приведена на рис.3 Схема потоков узла пиролиза приведена на рис.31- этановая фракция; 2- водяной пар; 3- парогазовая смесь; 4- топливный газ; 5- воздух; 6,7- пирогаз; 8- умягченная вода; 9- продукты сгорания; 10- пар высокого давления; П1- печь пиролиза; АТ1 — АТ3- теплообменники; ЗИА1- закалочно-испарительный аппарат Рис.3 Схема потоков узла пиролиза Кинетика основной реакции процесса пиролиза C2H6 ⇄ C2H4 + H2 удовлетворительно описывается уравнением первого порядка K = (2,303/τ) lg [a/ (a-x)] где K- константа скорости реакции, c-1; τ- время, прошедшее от начала реакции (оптимальной продолжительность пребывания реагентов в зоне высоких температур), с; а, x- количество реагента исходное и вступившее в реакцию соответственно, % Определяют степень конверсии этана: 3,5=(2,303/0,32) lg [100/ (100-x)]; x=67,3% Селективность процесса по основной реакции равна: β=α//α= 0,6/0,673=0,89 Часовая производительность установки в расчете на 100%-й этилена составит: 250000 * 1000/8000=31250 кг/ч или 31250/28= 1116,071 кмоль/ч Расход этана, находящегося в составе поступающей на пиролиз этановой фракций: 1116,071/0,6=1860,118 кмоль/ч Общий расход этановой фракции: 1860,118/0,898=2071,401 кмоль/ч Определяют состав этановой фракции (расчет см. Пример 4) на входе в трубчатую печь (табл.5). Количество водяного пара на входе в трубчатую печь (поток 2): 64684*0,4=25874 кг/ч или 1437,444 кмоль/ч Таблица 5. Состав этановой фракции (поток 1)
Количество парогазовой смеси на входе в трубчатую печь (поток 3): 64684 + 25874=90558 кг/ч По основной реакции C2H6 ⇄ C2H4 + H2 (1) расход этана составляет 1116,071 кмоль/ч или 33482 кг/ч; образуется: этилена: 1116,071 кмоль/ч или 31250 кг/ч водорода: 1116,071 кмоль/ч или 2232 кг/ч Всего конвертируется этана: 1860,118*0,673=1251,859 кмоль/ч По реакции образования метана C2H6 + H2⇄ 2CH4 (2) расходуется: этана: 1251,859 — 1116,071=135,788 кмоль/ч или 4074 кг/ч водорода: 135,788 кмоль/ч или 271 кг/ч образуется метана: 135,788 * 2=271,576 кмоль/ч или 4345 кг/ч Остается этана в составе пирогаза: 1860,118 – 1251,859= 608,259 кмоль/ч или 18248 кг/ч Пропилен в составе этановой фракции конвертируется по двум реакциям: C3H6 ⇄ C2H2 + CH4 (3) C3H6 + 3H2⇄ 3CH4 (4) По реакции 3, согласно экспериментального данным, расходуется 8,5% пропилена, что составляет: 97,149 * 0,085=8,258 кмоль/ч или 347 кг/ч; образуется: ацетилена: 8,258 кмоль/ч или 215 кг/ч; метана: 8,258 кмоль/ч или 132 кг/ч. По реакции 4 расходуется 26% пропилена, что составляет: 97,149 * 0,260 = 25,259 кмоль/ч или 1061 кг/ч; образуется метана: 25,259 * 3 = 75,777 кмоль/ч или 1212 кг/ч. Расход водорода составляет 75,777 кмоль/ч или 151 кг/ч. Остается пропилен в составе пирогаза: 97,149 – 8,258 – 25,259 = 63,632 кмоль/ч или 2672 кг/ч. Пропан в составе этановой фракции конвертируется по следующим реакциям: 2C3H8 ⇄ C4H6 + 2CH4 + H2 (5) 2C3H8 ⇄ C4H8 + 2CH4 (6) 2C3H8 ⇄ C5H10 + CH4 + H2 (7) 2C3H8 ⇄ C4H10 + C2H4 + H2 (8) C3H8 + 2H2 ⇄ 3CH4 (9) По реакции 5 расходуется 55,0% пропана, что составляет: 97,356 * 0,55 = 53,546 кмоль/ч или 2356кг/ч образуется: бутадиена: 53,546/2=26,773 кмоль/ч или 1446 кг/ч; метана: 53,546 кмоль/ч или 857 кг/ч; водорода: 26,773 кмоль/ч или 53 кг/ч; По реакции 6 расходуется 6,0% пропана, что составляет: 97,149*0,06=5,841 кмоль/ч или 257 кг/ч образуется: бутиленов: 5,841/2 = 2,920 кмоль/ч или 163 кг/ч метана: 5,841 кмоль/ч или 94 кг/ч Всего содержится бутиленов в пирогазе: 2,920 + 1,657=4,577 кмоль/ч или 256 кг/ч По реакции 7 расходуется 8,5% пропана, что составляет: 97,356 * 0,085 = 8,275 кмоль/ч или 364 кг/ч образуется: пентенов: 8,275/2 = 4,138 кмоль/ч или 290 кг/ч метана: 4,138 кмоль/ч или 66 кг/ч водорода: 4,138 кмоль/ч или 8 кг/ч По реакции 8 расходуется 10% пропана, что составляет: 97,356 * 0,1 = 9,736 кмоль/ч или 428 кг/ч образуется: бутана: 9,736/2 = 4,868 кмоль/ч или 283 кг/ч этилена: 4,868 кмоль/ч или 136 кг/ч водорода: 4,868 кмоль/ч или 9 кг/ч По реакции 9 расходуется 17,5% пропана, что составляет: 97,356 * 0,175 = 17,037 кмоль/ч или 750 кг/ч Расход водорода составляет: 17,037 * 2 = 34,074 кмоль/ч или 68 кг/ч Образуется метана: 17,037 * 3 = 51,111 кмоль/ч или 818 кг/ч Остается пропана в пирогазе: 97,356 – (53,546 + 5,841 + 8,275 + 9,736 + 17,037)= 2,921 кмоль/ч или 129 кг/ч Бутадиен взаимодействует с этиленом по реакции C4H6 + C2H4 ⇄ C6H6 + 2H2 (10) В эту реакцию вступает 23,5% образовавшегося бутадиена, что составляет: 26,773 * 0,235 = 6,292 кмоль/ч или 340 кг/ч Расход этилена составляет: 6,292 кмоль/ч или 176 кг/ч образуется: бензола: 6,292 кмоль/ч или 491 кг/ч; водорода: 6,292 * 2 = 12,584 кмоль/ч или 25 кг/ч; Остается бутадиена: 26,773 – 6,292 = 20,481 кмоль/ч или 1106 кг/ч Всего образуется метана по реакциям 2 — 7, 9: 271,576 + 8,258 + 75,777 + 53,546 + 5,841 + 4,138 + 51,111 = 470,247 кмоль/ч или 7524 кг/ч По реакции: CH4 + H2O ⇄ CO + 3H2 (11) конвертируется 2,6% метана, что составляет: 470,247 * 0,026 = 12,226 кмоль/ч или 195 кг/ч Расход водяного пара: 12,226 кмоль/ч или 220 кг/ч образуется: оксида углерода: 12,226 кмоль/ч или 342 кг/ч; водорода: 12,226 * 3 = 36,678 кмоль/ч или 73 кг/ч. Остается: метана: 470,247 – 12,226 = 458,021 кмоль/ч или 7329 кг/ч; водяного пара: 1437,444 – 12,226 = 1425,218 кмоль/ч или 25654 кг/ч. где 1437,444 – молярный поток водяного пара на входе в трубчатую печь (потока 2), кмоль/ч Образуется водорода по реакциям 1, 5, 7, 8, 10, 11: 1116,071 + 26,773 + 4,138 + 4,868 + 12,584 + 36,678=1201,112 кмоль/ч или 2402 кг/ч Расход водорода по реакциям 2, 4, 9: 135,788 + 75,777 + 34,074 = 245,639 кмоль/ч или 492 кг/ч Остается водорода в пирогазе: 1201,112 – 245,639 = 955,473 кмоль/ч или 1910 кг/ч Этилен в составе этановой фракции содержится 15,121 кмоль/ч (см. табл. 5), образуется по реакции 8 4,868 кмоль/ч, расходуется по реакции 10 6,292 кмоль/ч. Остаток 15,121 + 4,868 – 6,292 = 13,697 кмоль/ч представляет собой потери на стадии выделения этилена из пирогаза. В составе пирогаза (на выходе из трубчатой печи) содержится этилена: 1116,071 + 13,697 = 1129,768 кмоль/ч или 31633 кг/ч Таблица 6. Состав пирогаза (поток 6)
Потери этилена составляют: 13,697 * 100/1129,768 = 1,2% что соответствует оптимальному технологическому режиму. Коксообразованием в процессе пиролиза пренебрегают. По результатам расчета составляют табл 6. Необходимые округления при определении массовых потоков компонентов (в кг/ч) обусловлены точностью расчетов и необходимостью соблюдения закона сохранения масс. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
