кальцинированная сода. Методы производства кальцинированной соды. Характеристика сырья
 Скачать 86.81 Kb. Скачать 86.81 Kb.
|
|
Содержание:
Введение. Кальцинированная сода — Na2СО3 — представляет собой белый кристаллический порошок с температурой плавления 852°С, плотностью 2533 кг/м3. Насыпная плотность кальцинированной соды составляет от 500 до 700 кг/м3. Выпускается также специальный сорт соды — так называемая «тяжелая» сода. Насыпная плотность «тяжелой» соды — от 800 до 1000 кг/м3. Кальцинированная сода — гигроскопичная соль. Она хорошо растворяется в воде с выделением тепла. При нагревании раствора выше 32,5°С растворимость соды снижается. Кальцинированная сода широко применяется во многих отраслях промышленности, а также для бытовых нужд. До 25% кальцинированной соды применяется в химической промышленности для получения бикарбоната натрия, каустической соды и других солей натрия, стекла, в анилинокрасочном и лакокрасочном производствах. Основными потребителями кальцинированной соды являются цветная и черная металлургия, нефтяная, пищевая, целлюлознобумажная, текстильная и другие отрасли промышленности. В данном реферате более подробно рассмотрен способ приготовления соды, предложенный бельгийским инженером Эрнестом Сольве в семидесятых годах ΧΙΧ столетия. Этот способ произвел полный переворот в содовой технике. Сущность этого метода состояла в насыщении природных соляных растворов аммиаком и углекислым газом и переработке получающегося при этом осадка бикарбоната на кальцинированную соду посредством простого прокаливания. Методы производства кальцинированной соды. Производство соды в наши дни осуществляется четырьмя способами:
Главенство до сих пор принадлежит первому способу производства соды. Преимущества аммиачного способа производства соды: относительная дешевизна, широкая распространенность и доступность извлечения необходимого сырья; незначительность температур (до 100°С), при которых осуществляются основные реакции процесса; достаточная отлаженность способа производства соды; невысокая себестоимость кальцинированной соды. В XX в. в Японии этот метод был модернизирован, и предложенный в результате способ Асахи позволил экономить энергию на протяжении всего производственного цикла и снизить расход сырья. Характеристика сырья. Основным сырьем для производства кальцинированной соды являются мел или известняк и раствор поваренной соли. Кроме того, применяют еще ряд вспомогательных материалов — аммиак, воду, пар и электроэнергию. Карбонатное сырье. Для получения оксида углерода (IV) и извести на содовых заводах применяют известняк или мел, называемые, карбонатным сырьем. От качества карбонатного сырья в значительной мере зависит нормальная работа содового завода. Применение известняка более желательно, чем применение мела. При увеличении влажности мела возрастает расход топлива на его обжиг и, следовательно, расход воздуха на сжигание топлива. С увеличением расхода воздуха снижается концентрация СО2 в печном газе. Кроме того, прочность мела ниже, чем известняка. Содержание СаСО3 в известняке в соответствии с ОСТ 21-27—76 в пересчете на сухой продукт должно быть не менее 92%. Расход карбонатного сырья (100% СаСО3) на 1 т соды составляет 1,1—1,25 т. Содовые заводы обычно находятся вблизи месторождений карбонатного сырья. Поваренная соль широко распространена в природе как в твердом виде, так и в виде растворов. В производстве соды аммиачным способом применяют не твердую соль, а рассол, стоимость добычи которого путем выщелачивания соли во много раз ниже стоимости добычи твердой соли. На содовых заводах к рассолу предъявляются следующие требования: он должен быть насыщенным или близким к насыщению. Максимальная концентрация NaCl в воде при 15°С равна 317 г/л. В содовой промышленности концентрацию растворов принято выражать в так называемых нормальных делениях (н.д.). Одно нормальное деление соответствует содержанию 1/20 экв. вещества в 1 л раствора. На практике применяют рассол, содержащий 305—310 г/л NаСl, что соответствует 104,3 — 106,0 н.д. Увеличение концентрации NаСl благоприятно влияет на степень его использования, что ведет к уменьшению удельного расхода рассола, к снижению расхода аммиака, известняка, пара, воды, электроэнергии на 1 т соды. На производство 1 т кальцинированной соды расходуется около 1,5 т поваренной соли. Аммиак в производстве соды находится в замкнутом цикле: после регенерации в отделении дистилляции он возвращается обратно в производство. Для восполнения неизбежных потерь в цикл вводят аммиачную воду, содержащую до 25% г NH3. Аммиачная вода, поступающая с коксохимических заводов, содержит сульфид аммония, предохраняющий стальную аппаратуру и трубопроводы от коррозии. При использовании синтетической аммиачной воды в технологический процесс производства соды вместе с аммиачной водой вводят Nа2S. Промышленный аммиачный способ (способ Сольве) В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день. Способ основан на реакции взаимодействия гидрокарбоната аммония с хлоридом натрия, в результате которой получаются хлорид аммония и гидрокарбонат натрия. На практике процесс проводят, вводя в почти насыщенный раствор хлорида натрия эквимолярные количества газообразных сначала аммиака, а потом диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3. Гидрокарбонат натрия выпадает в осадок, когда диоксид углерода вводится в раствор: NaCl + H2O + NH3 + CO2 → NaHCO3 + NH4Cl. Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20° C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140-160° C, при этом он переходит в карбонат натрия: 2NaHCO3 → Na2CO3 + H2O + CO2, CaCO3 → CaO + CO2. Известь СаО, получаемую одновременно с СO2, действием на нее избытка воды превращают в известковое молоко Са(OH)2 которое используется для регенерации связанного аммиака из раствора хлористого аммония по реакции 2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O, и полученный NH3 также возвращают в производственный цикл. Таким образом, исходным сырьем для производства соды по аммиачному способу служат естественные или искусственно приготовленные растворы поваренной соли и известняк или мел. Аммиак, находящийся все время в круговороте, теоретически не должен расходоваться; неизбежные практические потери NH3 компенсируются вводом в процесс аммиачной воды. Единственным отходом производства является хлорид кальция, не имеющий широкого промышленного применения. Но и его можно переработать, подвергнув электролизу, и полученный кальций вернуть в производство, превратив назад в гашеную известь. До сих пор этот способ остается основным способом получения соды во всех странах. Производство соды кальцинированной по аммиачному способу на различных содовых заводах осуществляется почти по одной и той же технологии - схеме. Различны бывают конструкции, размеры и производительность отдельных групп аппаратов. Весь процесс производства соды является непрерывным, он делится на несколько операций; эти операции с соответствующей аппаратурой принято называть станциями. Технологическая схема производства кальцинированной соды. Производство кальцинированной соды по аммиачному способу включает восемь основных отделений:
Технологическая схема производства кальцинированной соды аммиач-ным способом представлена на рис.1. 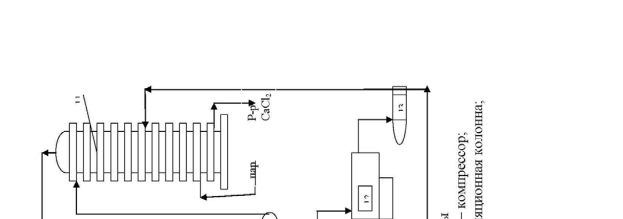 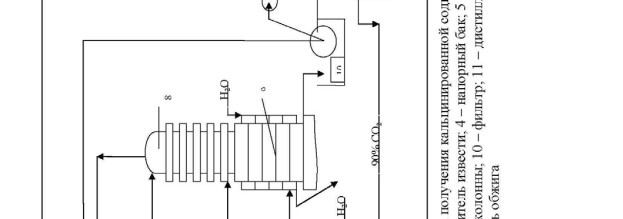 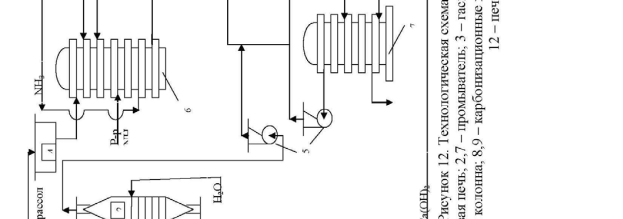 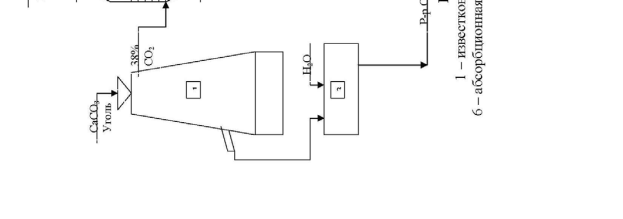 Для производства соды используют очищенный раствор хлорида натрия с концентрацией 270 г/л. Он поступает из напорного бака 4 в абсорбционную колонну барботажного типа 6, где происходит насыщение рассола аммиаком и частично углекислым газом. Для этого используют регенерированный аммиак из дистиляционной колонны 11, а также отходящие газы карбонизационных колонн 8 и фильтров 10, содержащие небольшое количество аммиака и углекислого газа. Абсорбция ведется последовательно в нескольких абсорберах. Для компенсации потерь аммиака в абсорберы вводится аммиачная вода (примерно 2,5 кг на 1 т воды). Затем аммонизированный рассол подается в карбонизационные колонны 8. В нижней части которых 9 расположены холодильники, в которых циркулирует холодная вода. В нижнюю и среднюю части колонны компрессорами 5 подается концентрированный углекислый газ из печи обжига 12 и слабый печной газ известковых печей 1. В результате карбонизации образуется бикарбонат натрия в виде твердой фазы. Бикарбонатная суспензия из колонны 9 подается на вакуум-фильтр барабанного типа 10, где суспензия делится на сырой бикарбонат и фильтровую жидкость. Сырой бикарбонат подается в печь обжига 12 , температура в которой составляет 140-1700С. Образовавшаяся сода удаляется из печи шнеком и транспортером 13 подается на упаковку. Газы кальцинации, содержащие водяные пары и 90 % СО2 в сухом газе удаляют с загрузочного конца печей и после охлаждения и промывки водой в промывателе 7 компрессором 5 подают на карбонизацию. Фильтровая жидкость с фильтра 10 подается на регенерацию аммиака в дистиляционную колонну 11. Туда же подается известковое молоко из гасителя 3. В нижнюю часть колонны подается пар. Из нижней части дистиляционной колонны отводится раствор хлорида кальция в шламовые бассейны, а газы дистилляции после охлаждения подаются в абсорбер 6. Известь и газ, содержащий 30-35 % СО2 производятся в известковых печах 1. Образующийся там печной газ очищают от пыли и охлаждают в промывателе 2 и компрессорами 5 подают на карбонизацию в колонну 8. Заключение. В семидесятых годах ΧΙΧ столетия выступил на сцену новый способ приготовления соды, предложенный бельгийским инженером Эрнестом Сольве. Этот способ произвел полный переворот в содовой технике. Сущность этого метода состояла в насыщении природных соляных растворов аммиаком и углекислым газом и переработке получающегося при этом осадка бикарбоната на кальцинированную соду посредством простого прокаливания. Отличительною особенностью разработанного Сольве способа фабрикации является непрерывность процесса во всех его стадиях. Изобретательности Сольве содовая техника обязана введением в практику знаменитых сольвеевских колонн для насыщения аммиачного рассола углекислым газом, для получения аммиачного рассола и для отгонки аммиака из маточных жидкостей при фильтрации бикарбоната. Наиболее важные области потребления каустической соды (перечислены в порядке уменьшения потребляемого количества) — химическое производство; переработка нефти; производство искусственного волокна и пленки, целлюлозы и бумаги, алюминия, моющих средств и мыла; обработка тканей; рафинирование растительного масла; регенерация резины. Список использованной литературы:
|
