|
|
«Разработка структуры и составление обзорно-повторительных таблиц по теме «Основы металлургического производства меди»». Отчёт медь готовый. Основы металлургического производства меди
Министерство просвещения Российской Федерации
Федеральное государственное автономное образовательное учреждение
высшего образования
«Российский государственный профессионально-педагогический университет»
Институт инженерно-педагогического образования
Кафедра инжиниринга и профессионального обучения в машиностроении и металлургии
ОТЧЁТ
о выполнении практической работы
«Разработка структуры и составление обзорно-повторительных таблиц
по теме «Основы металлургического производства меди»»
дисциплины «Технология конструкционных материалов и материаловедение»
образовательной программы профиля «Машиностроение и материалообработка (Инжиниринг обеспечения качества машиностроения)»
направления подготовки 44.03.04 Профессиональное обучение (по отраслям)
Вариант ___
Выполнил обучающийся группы
|
МС-302
|
|
|
|
шифр группы
|
|
Фамилия И.О. обучающегося
|
|
|
|
|
|
дата сдачи отчёта
|
|
|
Проверил
|
доцент
|
кафедры ИММ
|
|
Бухаленков В.В.
|
|
должность преподавателя
|
|
|
Фамилия И.О. преподавателя
|
Оценка
|
|
|
|
|
В.В. Бухаленков
|
|
оценка
|
|
дата
|
|
подпись преподавателя
|
Екатеринбург
2022
1.Основные технологические этапы производства меди
Последовательность технологических операций получения меди пирометаллургическим способом представлена на рисунке 1 в виде блок-схемы.

Рисунок 1 – Блок-схема пирометаллургического производства меди:
 – плавка концентрата без отжига, – плавка концентрата без отжига,
 – плавка непосредственно из руды. – плавка непосредственно из руды.
2. Обзорно-повторительные таблицы по теме «Основы металлургического производства стали»
2.1 Основные характеристики и свойства меди
Медь (Cu от лат. Cuprum) — элемент одиннадцатой группы четвёртого периода (побочной подгруппы первой группы птхэ Д. И. Менделеева, с атомным номером 29. Простое вещество медь — это пластичный переходный металл золотисто-розового цвета (красно-розового цвета при отсутствии оксидной плёнки).

 
Элементарная
ячейка кристал-
лической струк-
туры
Самородная медь
Свойства атома
|
Название, символ, номер
|
Медь/Cuprum (Cu), 29
|
Атомная масса (молярная масса)
|
63,546(3)[1] а. е. м. (г/моль)
|
Электронная конфигурация
|
[Ar] 3d10 4s1
|
Радиус атома
|
128 пм
|
Химические свойства
|
Ковалентный радиус
|
117 пм
|
Радиус иона
|
(+2e) 73 (+1e) 77 (K=6) пм
|
Степени окисления
|
3, 2, 1, 0
|
Термодинамические свойства простого вещества
|
Плотность (при н. у.)
|
8,92 г/см³
|
Температура плавления
|
1356,55 K (1083,4 °С)
|
Температура кипения
|
2 567 °С
|
Кристаллическая решётка простого вещества
|
Структура решётки
|
кубическая гранецентрированая
|
Параметры решётки
|
3,615 Å
|
Температура Дебая
|
315 K
|
Прочие характеристики
|
Теплопроводность
|
(300 K) 401 Вт/(м·К)
|
Основные методы получения меди — пирометаллургия, гидрометаллургия и электролиз.
3.2 Обзорно-повторительная таблица
«Процессы и соответствующее оборудование для производства меди»
Технологи-ческая операция
|
Разновидности технологичес-кой операции
|
Оборудование,
схема устройства
|
Исходные
материалы
|
Процессы, реакции
|
Продукт процесса, реакции
|
Химический состав
продукта
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
Добыча руды
|
Открытым (Карьер)
|
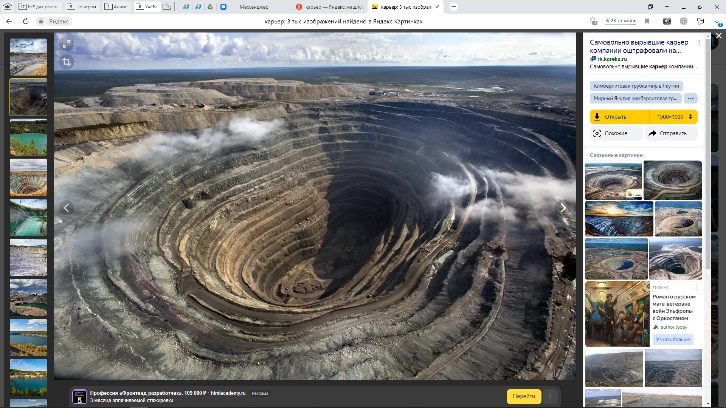
|
Руды содержащие 1-6% Cu
Отходы меди и её сплавов
|
_
|
_
|
Сернистые соединения (CuFeS2,Сu2S,СuS)
Окислов
(Cu2O,СuO)
Гидрокарбонатов
[СuCO3,Cu(OH)2]
Пустая порода состоит из пирита FeS2, кварца SiO2
|
Закрытым
(Шахта)
|
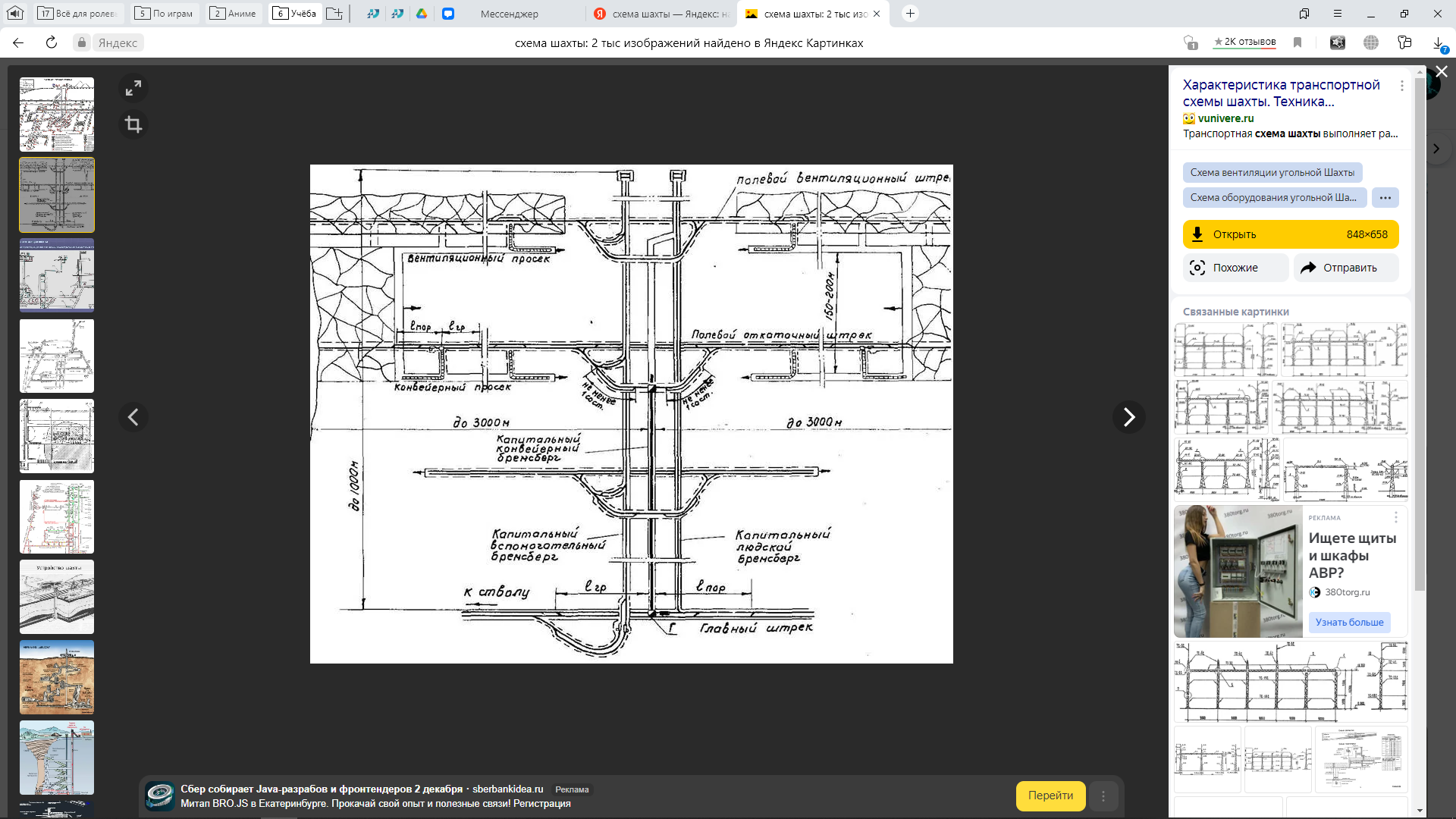
|
Флотация
обогащение
|
-
|

|
Пульпа- смесь твёрдых частиц и жидкости, негустая неоднородная система.
|
Аэрация
пульпы - процесс наполнения пульпы диспергированными пузырьками воздуха при флотации.
|
Медный концентрат
|
=
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
Окислительный обжиг
|
|

|
Концентрат медных руд
|
Обжиг концентрата в присутствии кислорода воздуха
|
Обжигают лишь бедные (8-25% Cu) богатые плавят без обжига
|
_
|
Плавка руды на штейн
|
|
В отражательных или электропечах

|
Концентрат медных руд
|
Восстановления окиси меди и высших окислов железа
(сульфиды меди и железа сплавляются и образуют первичный штейн) 1250-1300, °С
|
(Сu2O) реагируя с FeS
|
Cu2S(первичный штейн)
|
Конвертирование штейна(продувка воздухом)
|
|
В горизонтальных конверторах с боковым дутьём

|
Cu2S
|
Окисления сульфидов и железа
1100-1200, °С
Первичный период
|
2FeS+3O2 →
2Cu2S+3O2→
|
Первичный период
(получают белый штейн)
2FeO+2SO2+Q1
2Cu2O+2SO2+Q2
Железо связывается с SiO2 и удаляется в шлак
2FeO+SiO2=(FeO)2*SiO2
|
Вторичный
период из белого штейна образуют черновую медь
1250-1300, °С
|
Cu2S+3O2→
Закись меди взаимодействует с сульфидом меди
Сu2S+2Cu2O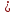
|
2Cu2O+2SO2
6Cu+SO2
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
Черновая медь
|
_
|
_
|
МК1
98,4-99,4%Cu
0,01-0,04%Fe
0,02-0,1%S
|
Сливают в ковш и разливают в стальные изложницы
|
_
|
_
|
Рафинирование
|
Огневое
|
Отражательные печи
Для рафинирования меди

|
98,4-99,4%Cu
0,01-0,04%Fe
0,02-
0,1% S
|
Окисление примесей, имеющих большее сродство к кислороду чем медь
(так же в этой реакции окисляются Al,Fe,Ni,Zn,и.тд
|
Кислород
соединяется с медью
4Cu+O2→
Закись меди реагирует с примесями
Me+Cu2O→
|
2Сu2O
MeO+2Cu
|
Электролитическое
|
Электролизные ванны для рафинирования

|
99-99,5%Сu
|
При пропускании постоянного тока анод растворяется, медь переходит в раствор, на катоде осаждаются чистая медь
|
Сu2++2e-
(Остальные примеси выпадают в осадок)
|
Cu (99,95%)
| |
|
|
 Скачать 2.38 Mb.
Скачать 2.38 Mb.
 – плавка концентрата без отжига,
– плавка концентрата без отжига, – плавка непосредственно из руды.
– плавка непосредственно из руды.