Исследование термодинамических циклов. Лэти Лаб9. Отчет по лабораторнопрактической работе 9 Исследование термодинамических циклов Выполнил Ковалев М. А
 Скачать 212.08 Kb. Скачать 212.08 Kb.
|
|
Санкт-Петербургский государственный электротехнический университет “ЛЭТИ” кафедра физики ОТЧЕТ по лабораторно-практической работе № 9 Исследование термодинамических циклов Выполнил Ковалев М.А. Факультет ЭА Группа № 3405 Преподаватель Титов Л.А.
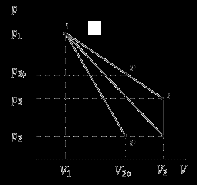
“Выполнено” “14” ноября 2013 Подпись преподавателя __________ ЛАБОРАТОРНАЯ РАБОТА № 9 ИССЛЕДОВАНИЕ ТЕРМОДИНАМИЧЕСКИХ ЦИКЛОВ ЦЕЛЬ РАБОТЫ: исследование политропно-изохорно-изотермического (nVT) и адиабатно-изохорно-изотермического (SVT) циклов. СХЕМА УСТАНОВКИ И МЕТОД ИЗМЕРЕНИЙ Приборы и принадлежности: баллон с воздухом, манометр, микрокомпрессор, лабораторные термометр и барометр. И 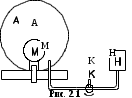 спользуемая в работе установка изображена на рис. 2.1. Баллон А объёмом V1 может сообщаться либо с насосом H, либо с атмосферой. Внутрь баллона помещён манометр М, измеряющий избыточное давление. Одно деление шкалы равно 4 мм вод. ст., что составляет 40 Па. Рабочим газом является воздух. В исходном состоянии параметры состояния воздуха следующие: давление p2 и температура T1. Диаграмма исследуемого цикла в координатах давления p и объёма V показана на рис. 2.2. 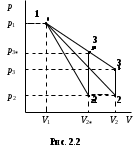 Исходным является состояние, в котором воздух имеет давление p2 и температуру T1. Насосом в баллон накачивают воздух до давления p1= p2 + p1 (состояние 1 (p1; V1)). При сжатии воздух нагревается, поэтому после закрытия крана необходимо выждать некоторое время, пока температура воздуха в баллоне не сравняется с температурой окружающей среды (при этом прекращается движение стрелки манометра). Затем воздух выпускают через кран К в атмосферу в течение нескольких секунд. Когда стрелка манометра приблизится к нулю, кран закрывают. В этот момент давление воздуха баллоне становится p2(состояние 2 (p2; V2). Изменение параметров состояния воздуха в процессе расширения отражает линия 12, которая является политропой. После закрытия крана охлаждённый при расширении воздух изохорически нагревается до температуры окружающей среды в результате теплообмена. Изменение параметров состояния воздуха отражает линия 23, которая является изохорой. Температура воздуха в баллоне становится равной температуре в точке 1 (T3 = T1), следовательно, точки 1 и 3 лежат на одной изотерме. После выравнивания температур давление в баллоне изменится на p3 и станет p3 = p2 + p3 (состояние 3 (p3; V2)). Таким образом, p1и p3 это изменения давления на участках 12 и 23. Участки 12 и 13 на диаграмме можно аппроксимировать прямыми, так как изменения параметров p, V, T в данной работе малы и много меньше абсолютных значений соответствующих величин. В работе изучаются политропно-изохорно-изотермический (nVT) и адиабатно-изохорно-изотермический (SVT) циклы путем их моделирования при значениях показателя адиабаты γ = 1,4 и показателя политропы n, полученным в результате измерений. ОСНОВНЫЕ РАСЧЕТНЫЕ ФОРМУЛЫ 1. Показатель политропы n при известных изменениях давлений Δp1, Δp3. Продифференцируем уравнения политропы (рVn = const) и изотермы (рV = const): рnV n1 dV + V n dр = 0 для политропы рdV + V dр = 0 для изотермы Преобразуем соотношения к виду 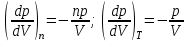 При относительно малых изменениях p и V угловые коэффициенты политропы и изотермы рассчитываются по формулам 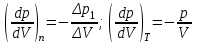 , где V = V2 V1. , где V = V2 V1.Из отношения приведенных уравнений получаем 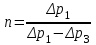 2. Холодильные коэффициенты ε для nVT и SVT- процессов при известных давлениях p2 и изменениях давлений Δp3, Δp3*. Холодильный коэффициент определяется как отношение теплоты, отнятой от охлаждаемого газа, к затраченной в цикле работе. Для SVT-цикла 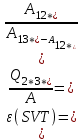 Для nVT-цикла 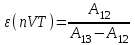 Перепишем выражения для , используя экспериментально измеренные величины давлений, для чего значения работы А12 и А12* определим графическим способом. В рV-координатах (рис. 2.2) они равны площадям трапеций, основания которых р1 и p2 = р2*, а высоты (V2 V1) и (V2* V1) соответственно. После преобразований получаем: 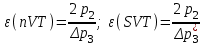 3. Холодильный коэффициент обратного цикла Карно εK при известных температурах нагревателя и холодильника T1, T2. КПД прямого цикла Карно по определению равен 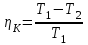 . .Холодильный коэффициент обратного цикла Карно 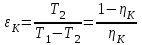 . .4. Число молей воздуха в сосуде по известным значениям p2, V1, T1: 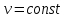 Запишем уравнение состояния идеального газа для процесса 1-2: 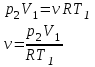 5. Изменения энтропии ΔS при известных давлениях Δp1 и p2, показателе политропы n и количестве молей газа ν. По определению 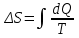 . .nVT: На участке 12 (политропический процесс) S12 = 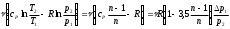 На участке 2-3 (изохорический процесс) S23 = 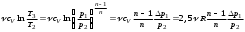 На участке 3-1 (изотермический процесс) S31 = 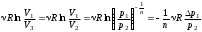 SVT: На участке 12* (адиабатический процесс) изменение энтропии равно нулю. Изменения энтропии на участках 2-3 (изохорический процесс) и 3-1 (изотермический) равны по величине, но различаются знаком: S3*1 = 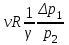 ОБРАБОТКА РЕЗУЛЬТАТОВ 1. а) Определение избыточных давлений Δp1 и Δp3 (прямые измерения): 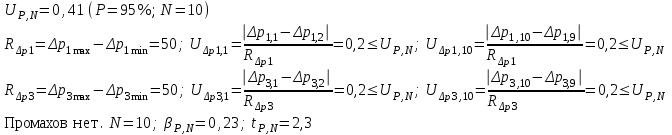 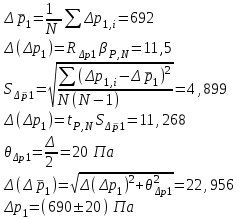 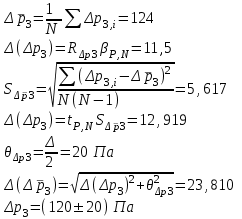 б) Определение показателя политропы n (перенос погрешностей.) 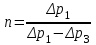 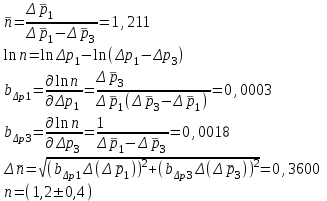 2. Определение параметров состояния (p, V, T) в точках 1, 2, 3, 1*, 2*, 3*. 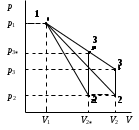 Cостояние 1 (совпадает с 1*): p1 = p2 + Δp1 = 102790 Па V1 = 22,4 л = 22,4∙10-3 м3 T1 = 294 K Состояние 2*: p2* = p2 = 102100 Па Уравнение адиабаты: 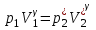 Газ двухатомный, i = 5. 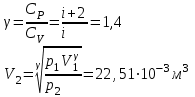 Уравнение состояния: 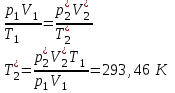 Cостояние 3*: T3* = T1 = 294 K Из уравнения изотермического процесса 1-3: 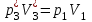 Процесс 2-3 изохорический, значит V3* = V2*. Тогда имеем 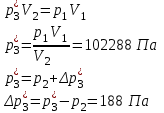 Уравнение состояния: 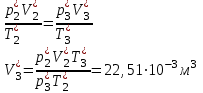 Состояние 2: p2 = 102100 Па Уравнение политропы: 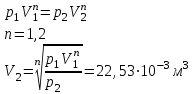 Уравнение состояния: 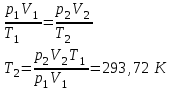 Cостояние 3: p3 = p2 + Δp3 = 102220 Па T3 = T1 = 294 K Уравнение состояния: 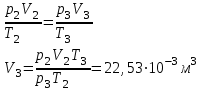 Графики циклов (начало координат сдвинуто): nVT (n = 1,2) 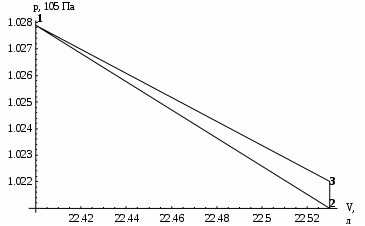 SVT (γ = 1,4) 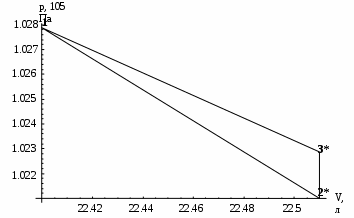 3. Расчет холодильных коэффициентов ε (вывод формул – стр. 3). Цикл nVT (1-2-3-1): 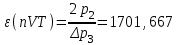 Цикл SVT (1-2*-3*-1): 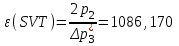 Так как Δp3* > Δp3, 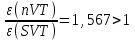 . .Обратный цикл Карно (идеальная холодильная машина): Для T1, T2: 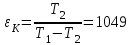 Для T1, T2*: 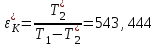 Так как T2* < T2, 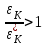 . .Холодильные коэффициенты циклов Карно меньше, чем холодильные коэффициенты рассматриваемых циклов в силу идеальности холодильной машины Карно. 4. Определение числа молей воздуха ν в сосуде (вывод формул – стр. 3). 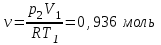 5. Изменение энтропии ΔS в циклах 1-2-3-1, 1-2*-3*-1 (вывод формул – стр. 4). Цикл nVT (1-2-3-1): Политропа 1-2 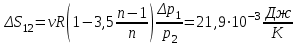 Изохора 2-3 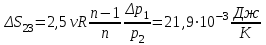 Изотерма 3-1 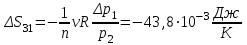 Изменение энтропии за цикл 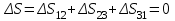 Цикл SVT (1-2*-3*-1): Адиабата 1-2* ΔS12 = 0 Изохора 2*-3* 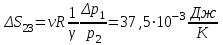 Изотерма 2*-3* 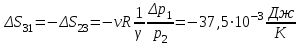 Изменение энтропии за цикл 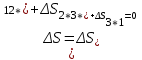 ИТОГИ
ВЫВОДЫ Выполнив данную лабораторную работу, я исследовал политропно-изохорно-изотермический (nVT) и адиабатно-изохорно-изотермический(SVT)циклы. Пользуясь экспериментально измеренными величинами избыточных давлений Δp1 и Δp3, я определил показатель политропного процесса n, нашел холодильные коэффициенты ε для nVT- и SVT-циклов. С помощью уравнения состояния идеального газа мной были вычислены параметры состояния (p, V, T). На основе полученных данных я построил графики nVT- и SVT-циклов в pV-координатах. Также были найдены изменения энтропии ΔS для каждого процесса nVT- и SVT-циклов. Результаты работы помещены на лист «Итоги» в табличной форме. Контрольные вопросы 1. Чему равны давление, объем и температура газа при нормальных условиях? Рассчитать величину газовой постоянной. 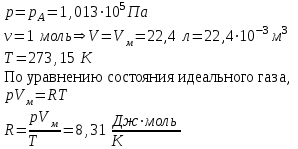 2. Что называется тепловой машиной? Чем характеризуется эффективность ее работы? Тепловой машиной называется периодически действующий двигатель, совершающий работу за счет получаемой извне теплоты. Эффективность работы тепловой машины характеризуется коэффициентом полезного действия 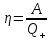 , где Q+ – количество теплоты, полученной тепловой машиной за цикл, A – работа, совершенная тепловой машиной за цикл. , где Q+ – количество теплоты, полученной тепловой машиной за цикл, A – работа, совершенная тепловой машиной за цикл.3. Что называется холодильной машиной? Чем характеризуется эффективность ее работы? Холодильной машиной называется машина, отбирающая за цикл от тела с некоторой температурой T2 количество теплоты Q2, и отдающая телу с более высокой температурой T1 теплоту Q1'. Эффективность работы холодильной машины характеризуется холодильным коэффициентом 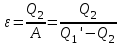 . .4. Может ли энтропия замкнутой системы уменьшаться? Нет. Второе начало термодинамики гласит: в замкнутых системах энтропия не уменьшается, 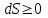 . .5. Какой физический смысл имеет площадь цикла в координатах nVT и SVT? Площадь замкнутого цикла равна работе газа за цикл. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

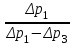 = (1,20,4)
= (1,20,4)