Пиримидиновые основания. Синтез пиримидиновых оснований
 Скачать 264.35 Kb. Скачать 264.35 Kb.
|
|
Пиримидиновые основания – производные пиримидина, входящие в состав нуклеиновых кислот: урацил, тимин, цитозин. Для оснований, содержащих группу –ОН, характерно подвижное равновесие структурных изомеров, обусловленное переносом протона от кислорода к азоту и наоборот: Синтез пиримидиновых оснований происходит во всех клетках организма. В реакциях синтеза участвует аспарагиновая кислота, глутамин, СО2, затрачивается 2 молекулы АТФ. В отличие от разветвленного синтеза пуринов этот синтез происходит линейно, т.е. пиримидиновые нуклеотиды образуются последовательно, друг за другом.Условно можно выделить 3 общих этапа синтеза и реакции синтеза УТФ и ЦТФ:
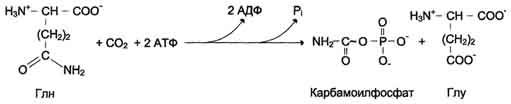
Образование дигидрооротата У млекопитающих ключевой, регуляторной реакцией в синтезе пирймидиновых нуклеотидов является синтез карбамоилфосфата из глутамина, СО2 и АТФ, в реакции катализируемой кар-бамоилфосфатсинтетазой II (КФС II), которая протекает в цитозоле клеток (рис. 10-12). В реакции NH2-гpyппa карбамоилфосфата образуется за счёт амидной группы глутамина, что отличает эту реакцию от реакции синтеза карбамоилфосфата в митохондриях в процессе синтеза мочевины из СО2, NH3 и АТФ с участием КФС I. Карбамоилфосфат, использующийся на образование пирймидиновых нуклеотидов, является продуктом полифункционального фермента, который наряду с активностью КФС II содержит
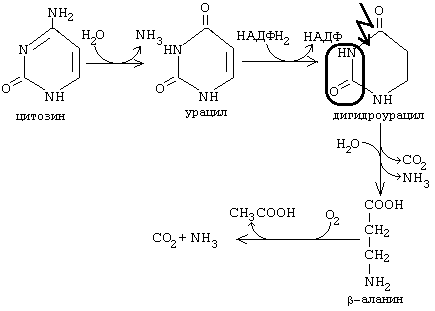
Рис. 10-12. Синтез карбамоилфосфата. каталитические центры аспартаттранскарбамоилазы и дигидрооротазы. Этот фермент назвали "КАД-фермент" - по начальным буквам ферментативных активностей, которыми обладают отдельные каталитические домены этого белка. Объединение первых трёх ферментов метаболического пути в единый полифункциональный комплекс позволяет использовать почти весь синтезированный в первой реакции карбамоилфос-фат на взаимодействие с аспартатом и образование карбамоиласпартата, от которого отщепляется вода и образуется циклический продукт - дигидрооротат (рис. 10-13). Отщепляясь от КАД-фермента, дигидрооротат подвергается дегидрированию NAD-зависимой дигидрооротатдегидрогеназой и превращается в свободное пиримидиновое основание - оротовую кислоту, или оротат. Оротовая ацидурия Оротовая кислота является межуточным продуктом обмена пиримидинов. При участии энзимов оротидилпирофосфатазы и оротидилдекарбоксилазы она превращается в рибософосфат. При дефиците обоих энзимов у пораженных лиц обнаруживается мегалобластическая анемия, не поддающаяся лечению витамином С, фолиевой кислотой или витамином В12, а также - и повышенная экскреция оротовой кислоты с мочой (1-2 г в сутки). Заболевание наследуется по аутосомно-рецессивному типу. У гетерозиготов активность обоих энзимов уменьшена приблизительно на 50%. Заболевание лечат успешно применением пиримидиновых нуклеотидов. Оротовая ацидурия I типа связана с утратой функции двух ферментов: оротатфосфорибозилтрансферазы, ОМФ-декарбоксилазы. наследуется.С мочой выделяется много оротовой кислоты.Недостаток пиримидиновых нуклеотидов. Лечат уридином. В детстве приводит к: отставанию в развитии, мегалобластической анемии, «оранжевой» кристаллоурии, подверженности инфекциям. Оротовая ацидурия II типа связана с недостатком ОМФ-декарбоксилазы. С мочой выделяются оротидин и оротовая кислота.   Пиримидиновые азотистые основания подвергаются тотальному разрушению до СО2, Н2О и NH3. Пуриновые азотистые основания сохраняют циклическую структуру пурина. Конечный продукт: мочевая кислота - вещество пуриновой природы. Аминогруппа азотистых оснований очень легко могут отщепляться гидролитическим путем. Аминогруппа может отщепляться, когда азотистое основание еще находится в составе нуклеозида, мононуклеотида и даже в составе нуклеиновой кислоты. Но поскольку в организме урацил не входит в состав ДНК, то дезаминирование цитозина и превращение его в урацил воспринимается клеткой как ошибка и исправляется.
b-аланин обычно разрушается до CO2, H2O и NH3, но иногда может использоваться для синтеза пептидов карнозина и ансерина в мышечной ткани. У микроорганизмов b-аланин используется и для синтеза HS-КоА. Конечным продуктов распада пиримидиновых азотистых оснований можно считать и мочевину, которая образуется из аммиака по известному механизму, изложенному в теме «Обмен простых белков». Тимин распадается подобно урацилу, но сохраняется CH3-группа, и вместо b-аланина образуется b-аминоизобутират (a-метил-b-аланин). Поскольку тимин встречается только в ДНК, то по уровню b-аминоизобутирата в моче судят об интенсивности распада ДНК. 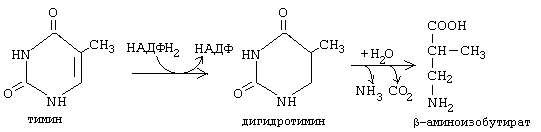 b-аминоизобутират выводится из организма и определение его количества в моче может использоваться для оценки катаболизма ДНК.  |