1. Гидролитические ферменты. Представители, роль в обмене веществ. Примеры катализируемых реакций. биохимия+. Содержание Гидролитические ферменты. Представители, роль в обмене веществ. Примеры катализируемых реакций стр. Способы осаждения белков из растворов.
 Скачать 83.5 Kb. Скачать 83.5 Kb.
|
|
Содержание Гидролитические ферменты. Представители, роль в обмене веществ. Примеры катализируемых реакций…………………………......................................................... 3 стр. Способы осаждения белков из растворов. Денатурация……………………………..5 стр. Полиненасыщенные жирные кислоты, строение, биологическая роль……………..7 стр. 1. Гидролитические ферменты. Представители, роль в обмене веществ. Примеры катализируемых реакций. Гидролазы - класс ферментов, катализирующих реакции расщепления органических соединений при участии воды (реакции гидролиза). Эти реакции протекают по следующей схеме: А‒В + Н2О → А‒Н + В‒ОН где А-В - сложное соединение, А-Н и В-ОН - продукты его гидролиза. Реакции этого типа активно протекают в организме; они идут с выделением энергии и, как правило, необратимы. Подклассы гидролаз формируются в зависимости от типа гидролизуемой связи. Наиболее важными являются следующие подклассы: Гидролазы, действующие на сложные эфиры (или эстеразы) гидролизуют сложные эфиры карбоновой, фосфорной, серной и других кислот. Широко распространённым ферментом этого подкласса являетсятриацилглицероллипаза (гидролаза эфиров глицерола, КФ 3.1.1.3). ускоряющая гидролиз ацилглицеролов: 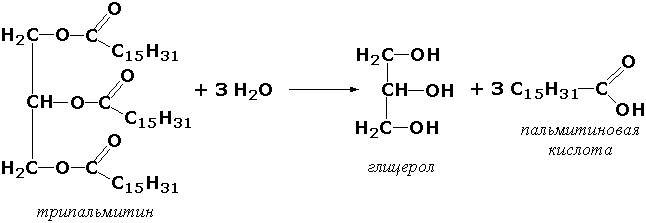 Другие представители эстераз расщепляют сложноэфирные связи в ацетилхолине (ацетилхолинэстераза), фосфолипидах (фосфолипазы), нуклеиновых кислотах (нуклеазы), фосфоорганических эфирах (фосфатазы). Гидролазы, действующие на гликозидные связи (гликозидазы) ускоряют реакции гидролиза олиго- и полисахаридов, а также других соединений, содержащих моносахаридные остатки (например, нуклеозидов). Характерным представителем являетсясахараза (β-D-фруктофуранозид-фруктогидролаза, КФ 3.2.1.26). катализирующая расщепление сахарозы: 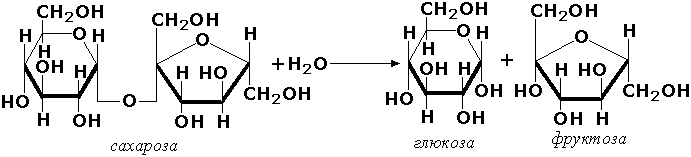 Гидролазы, действующие на пептидные связи (пептидазы), катализируют реакции гидролиза пептидных связей в белках и пептидах. К этой группе относятсяпепсин, трипсин, химотрипсин, катепсин и другие протеолитические ферменты. Гидролиз пептидных связей происходит по следующей схеме: 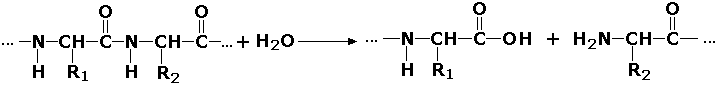 Гидролазы, действующие на C-N-связи, отличающиеся от пептидных, - ферменты, ускоряющие гидролиз амидов органических кислот. Представитель этого подкласса - глутаминаза(L-глутамил-амидогидролаза, КФ 3.5.1.2) - участвует в поддержании кислотно-основного состояния организма, катализируя в почках гидролиз глутамина: 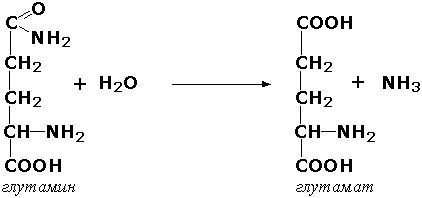 Гидролазы играют очень важную роль в обмене веществ микроорганизмов. По характеру действия они относятся к экзо-ферментам, выделяются клеткой во внешнюю среду и участвуют в расщеплении высокомолекулярных соединений вне клетки, тех, которые не способны проникнуть в клетку из-за малой величины пор в клеточной стенке и цитоплазматической мембране (белки, жиры, полисахариды и др.). Образовавшиеся в результате гидролиза низкомолекулярные вещества из внешней питательной среды могут проникать в клетку и затем подвергаться различным превращениям в ходе конструктивного и энергетического обменов. 2. Способы осаждения белков из растворов. Денатурация. Чтобы выделить белки из раствора или разделить белки по физико-химическим свойствам достаточно удалить один или оба фактора, обеспечивающих их растворимость - заряд и гидратную оболочку. Так как растворимость белков зависит только от них, то исчезновение одного или обоих этих факторов ведет к полному или частичному осаждению белка и, конечно, к потере его функций. Некоторые способы осаждения позволяют впоследствии восстановить нативные свойства и работоспособность белков. Обратимость осаждения белков обусловлена сохранением первичной структуры белка. Восстановление физико-химических и биологических свойств белка называется ренативация (ренатурация). Иногда для ренативации достаточно просто удалить повреждающий агент. Денатурация – необратимое осаждение белка из-за разрыва связей, стабилизирующих четвертичную, третичную, вторичную структуры белка, сопровождаемое изменением растворимости, вязкости, химической активности, снижением или полной потерей биологической функции. 1. Физическая денатурацияВызывается повышением температуры, ультрафиолетовым и микроволновым излучением, механическими воздействиями, ионизацией заряженными частицами. 2. Химическая денатурацияЗависит от природы денатурирующего реагента: - кислоты и щелочи образуют водородные связи с пептидными группами; - органические растворители образуют водородные связи и вызывают дегидратацию; - алкалоиды образуют связи с полярными группами и разрывают систему водородных и ионных связей; - тяжелые металлы взаимодействуют с заряженными радикалами, нейтрализуют отрицательные заряды и разрывают систему водородных и ионных связей. Высаливание – это добавление к раствору белка нейтральных солей (Na2SO4, (NH4)2SO4). Механизм высаливания заключается во взаимодействии анионов (SO42-) и катионов (Na+, NH4+) с зарядами белка (группы NH4+ и COO–). В результате заряд исчезает, и соответственно, исчезает взаимоотталкивание молекул. Одновременно резко уменьшается гидратная оболочка. Все это приводит к "слипанию" молекул и осаждению. Так как белки плазмы крови отличаются по размерам, заряду, строению, то можно подобрать такие количества соли, которые вызовут осаждение менее устойчивых белков, пока другие еще будут растворены. Осаждение водоотнимающими средствамиПри добавлении водоотнимающих средств (ацетон, этанол) происходит отнятие у белкагидратной оболочки, но не заряда. Растворимость несколько снижается, но денатурации не наступает. Например, в этом заключается антисептическое действие этанола. Изменение рНМягкое изменение рН до изоэлектрической точки белка ведет к исчезновению заряда, одновременному уменьшению гидратной оболочки и, как следствие, снижению растворимости молекулы. 3. Полиненасыщенные жирные кислоты, строение, биологическая роль. Полиненасыщенными жирными кислотами принято называть одноосновные жирные кислоты, в структуре которых присутствуют две и более двойных связей между атомами углерода. К полиненасыщенным жирным кислотам относятся в числе прочих и незаменимые жирные кислоты (эссенциальные жирные кислоты), получившие название витамина F, такие как линолевая (две двойные связи, положение первой – омега-6, то есть при шестом атоме углерода, отсчитывая от метильного конца) и линоленовая (три двойные связи, положение первой – омега-3, т. е. при третьем атоме углерода), эйкозапентаеновая (шесть двойных связей, положение первой – omega-3), идокозагексаеновая (пять двойных связей, положение первой – омега-3) кислоты.
Некоторые авторы также выделяют омега-9 кислоты, одной из которых является, например, олеиновая кислота (относится к мононенасыщенным жирным кислотам). Однако омега - 9 кислоты не относятся к эссенциальным, поскольку организм человека способен синтезировать их самостоятельно. Тем не менее, употребление в пищу оливкового масла, содержащего 65% олеиновой кислоты, положительно влияет на состояние сердечно-сосудистой системы, причем данный эффект усиливается высоким содержанием витамина Е в этом пищевом продукте. Источники полиненасыщенных жирных кислот (ПНЖК) достаточно многообразны. Интересно, что в противоположность общей тенденции, согласно которой мы ожидаем высокого содержания ненасыщенных жирных кислот преимущественно в растительных маслах, одним из важнейших источников полиненасыщенных жиров для человека является рыба и рыбопродукты (печень трески, лосось, макрель, сельдь, сардины, форель, тунец, моллюски и др.). В этой связи нельзя не упомянуть о такой полезнейшей добавке к взрослому и особенно детскому рациону, как рыбий жир. Он содержит комбинацию ПНЖК для развития мозга и сердечно-сосудистой системы ребенка и комплекс жирорастворимых витаминов (витамин A и витамин D) для всех систем организма, но особенно костной, иммунной и нервной. Кроме рыбы и рыбопродуктов, источниками полиненасыщенных жиров (особенно содержащих омега 3 ПНЖК) являются льняное, конопляное, соевое, рапсовое масла, масло канолы, грецкого ореха, тыквенных семечек и пр. Биологическая роль полиненасыщенных жирных кислот значительна: 1.Структурные компоненты липидов. Наличие полиненасыщенных жирных кислот определяет биологическую активность фосфолипидов, свойства биологических мембран. 2.Оказывают антиатеросклеротическое действие: а) увеличение выведение холестерина с калом; б) снижение образование липопротеидов низкой плотности; в) повышение эластичности и снижение проницаемости стенки сосудов. 2. Снижение синтеза жиров в организме. 3. Энергетическая функция. 4. Участие в обмене витаминов группы В. 5. Участие в процессах запоминания и поведенческих реакциях. 6.Являются субстратом для синтеза эйкозаноидов – биологически активных веществ, модулирующих метаболизм и активность как самой клетки, так и окружающих клеток. ТЕСТОВЫЕ МАТЕРИАЛЫ Тема 1. Молекулярное строение белков и пептидов 3. При денатурации белка не происходит: а) Распад белков до аминокислот б) Потеря биологической функции белка в) Разрушение вторичной и третичной структуры г) Выпадение осадка. Тема 2. Классификация, строение и биологические функции сложных белков. Обмен белков. 3. Какую валентность имеет железо в составе гемоглобина? а) 1 б) 2 в) 3 г) 6. Тема 3. Ферменты 3. Для чего служит каталитический центр фермента? а) Присоединение кофермента б) Превращение субстрата в) Связывание эффекторов г) Присоединение и ориентация субстрата. Тема 4. Активаторы и ингибиторы ферментов 3. Какие реакции ускоряют ферменты класса оксидоредуктаз а) Гидролитический распад органических молекул б)Реакции переноса функциональных групп в) Реакции изомерного превращения г) Окислительно-восстановительные реакции Тема 5. Незаменимые факторы питания 3. В каком виде витамин D оказывает свое биологическое действие? а) Эргокальциферол б) Дегидрохолестерин в) Кальцитриол г) Холекальциферол. Тема 6. Витамины 3. Какой структурный фрагмент лежит в основе никотинамида? а) Пиридиновый цикл б) Пуриновый фрагмент в) Изоаллоксазиновый фрагмент г) Остаток рибозы. Тема 7. Катаболизм и анаболизм. Первая стадия катаболизма. Тканевое дыхание и окислительное фосфорилирование 3. Что характерно для экзэргонических реакций? а) Выделение теплоты б) Поглощение теплоты в) Возрастание энтропии г) Уменьшение энтропии. . Тема 8. Обмен углеводов 3. Что такое гликоген? а) Резервный полисахарид клеток животных и грибов б) Компонент покровных тканей насекомых и ракообразных в) Структурный полисахарид растений г) Гормон. Тема 9. Энергетическое значение обмена углеводов 3. Какой из перечисленных сахаров относится к дисахаридам? а) Галактоза б) Глюкоза в) Сахароза г) Дезоксирибоза. Тема 10. Обмен липидов 3. Какое вещество является представителем стеринов? а) Холевая кислота б) Глицерин в) Пальмитиновая кислота г) Сфингозин. Тема 11. Фосфолипиды 3. Что лежит в основе строения стероидов? а) Изоаллоксазиновый фрагмент б) Пиримидиновый цикл в) Циклопентанпергидрофенантрен г) Пуриновый цикл. Тема 12. Структурная организация белков. 3. Выберите общий путь обмена аминокислот. а) Трансаминирование б) Метилирование в) Гидроксилирование г) Карбоксилирование. Тема 13. Обмен белков. 3. Из какого вещества образуется тирозин? а) Тироксин б) Тиреоглобулин в) Глутамин г) Фенилаланин |
