тесты хим. тест. бутадиен ацетилен этен пентан Этаналь содержит функциональную группу Карбонильную
 Скачать 116.42 Kb. Скачать 116.42 Kb.
|
|
К соединениям, содержащих сопряженную систему с открытой цепью относятся бензол = бутадиен ацетилен этен пентан Этаналь содержит функциональную группу =Карбонильную Карбоксильную Алкоскикарбоксильную Простую эфирную Аминогруппу положительный индуктивный эффект характерен для метаналя =глицерина формиата натрия гексана бутиндиена Из перечисленных молекул прохиральна пара-аминобензойная кислота (ПАБК) =ацетоуксусная кислота масляная кислота пропаналь бутаналь В молекуле местного анестетика лидокаина укажите центр протонирования 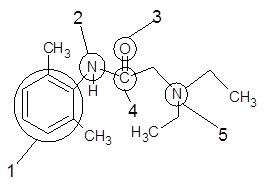 5 5Только ароматичен пиррол имидазол циклогексан =порфирин Пирролидин Приставкой обозначают насыщенность углеводородный радикал старшую группу =заместитель положение кратной связи Общая формула аренов CnH2n CnH2n+1 CnH2nO2 CnHn =CnH2n-6 Катализатор является веществом, ускоряющим реакцию и … поглощающим побочные продукты увеличивающим выход продукта не участвующим в реакции =не расходующимся в процессе реакции увеличивающим энергию активации Макроэрг для сопряжённых реакций в организме цГМФ ЛДГ ГЦ ФАД =ГТФ Если температурный коэффициент равен 3, то при повышении температуры на 20 градусов скорость реакции =увеличивается в 9 раз увеличивается в 20 раз уменьшается в 9 раз увеличивается в 3 раза уменьшается в 3 раза В методе ацидиметрии применяется индикатор =метилоранж любая щелочь любая кислота эриохром дихлорфенолиндофенолят натрия Как изменяется энтропия в случае протекания процессов катаболизма =увеличивается уменьшается не изменяется может как увеличиваться, так и уменьшаться равна нулю Скорость химической реакции в каждый момент времени пропорциональна концентрациям реагентов, возведенным в некоторые степени - это формулировка закона Гесса главного закона кинетики уравнения Аррениуса закона Вант#Гоффа =закона действующих масс Какие процессы называют эндэргоническими? ΔH< 0 ΔG < 0 ΔH> 0 =ΔG > 0 ΔG = 0 Укажите направление смещения равновесия системы Hb+O2↔ HbO2, если увеличить парциальное давление кислорода в системе в сторону прямой реакции равновесие не сместится = в сторону обратной реакции в сторону увеличения давления система находится в состоянии равновесия Молярная концентрация имеет размерность ... =моль/л моль/кг г/моль г/мл проценты (%) =7,3-7,8 7,1-7,15 7,0-7,1 10,0-11,0 0,86-0,94 Стерильный раствор изотонического раствора хлорида натрия выпускается в формах =флаконы по 200 и 400 мл; ампулы по 1,2,5,10 мл для приготовления растворов для инъекций флаконы по 200 и 400 мл ампулы по 1,2,5,10 мл для приготовления растворов для инъекций таблетки для приготовления раствора, флаконы по 200 и 400 мл; ампулы по 1,2,5,10 мл для приготовления растворов для инъекций таблетки покрытые пленочной оболочкой, флаконы по 200 и 400 мл; ампулы по 1,2,5,10 мл для приготовления растворов для инъекций Соли комплексонов называются… =комплексонатами; комплексными соединениями; комплексонами; комплексонными соединениями; комплексонотомами. Осмос это… процесс преимущественно двустороннего проникновения молекул через полунепроницаемую мембрану =процесс преимущественно одностороннего проникновения молекул через полупроницаемую мембрану процесс преимущественно одностороннего проникновения молекул через непроницаемую мембрану процесс преимущественно двустороннего проникновения молекул через проницаемую мембрану процесс преимущественно двустороннего проникновения молекул из раствора в раствор В элементе Якоби-Даниэля на медной пластинке протекает… полуреакция восстановления полуреакция окисления окислительно–восстановительная реакция реакция окисления =реакция восстановления Пример первичной диссоциации [Co(NH3)6](NO3)2 =[Co(NH3)6](NO3)2 = [Co(NH3)6]2+ +2NO3- [Co(NH3)6](NO3)2 = [Co(NH3)6]NO3+ +NO3- [Co(NH3)6](NO3)2 = Co[(NH3)6]+ +2NO3- [Co(NH3)6](NO3)2 = [Co]2+ + 6 NH3 +2 NO3- [Co(NH3)6](NO3)2 = Co2+ + (NH3)62+ +2 NO3- При образовании координационной связи комплексообразователь выступает в роли: донора электронной пары =акцептора электронной пары носителя отрицательного заряда источника неспаренных электронов нет верного ответа Для каких трех растворов характерны изображённые случаи? 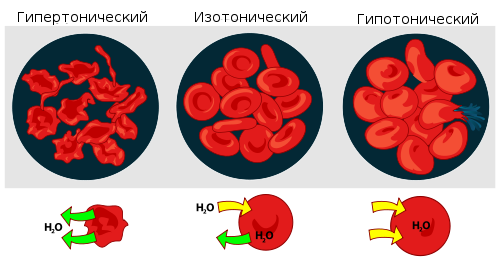 =0,9% NaCl =дистиллированная вода питьевая вода =15% CaCl2 нет верных ответов Азот содержит ароматический гетероцикл: пиран фуран тиофен =индол Оксиран Свойство молекулы не совмещаться в пространстве со своим зеркальным отражением называется Симметрия Изомерия Оптическая активность =Хиральность Энантиомерность Электронное строение атома углерода отражает формула 1s2 2s2 2p4 1s2 2s2 2p6 =1s2 2s2 2p2 1s2 2s2 2p3 3s1 1s2 2s1 2p1 Сопряженная система 1,4-диметилбензола содержит пи-электронов. 5 =6 7 8 12 Запахом зеленых яблок обладает формальдегид =ацетальдегид этилацетат амилацетат изовалерианбутират Способность вращать плоскость поляризации света называется =Оптической активностью Химическим потенциалом Стандартным состоянием Активностью компонентов Хиральностью Конденсированная гетероциклическая система пурин входит в состав: =мочевой кислоты урацила барбитуровой кислоты нафталина цитозина Сопряженная система этилбензола содержит пи-электронов. 1 =6 7 9 11 Макроэрг для сопряжённых реакций в организме цГМФ СДГ НАД ФАД =АТФ Процессы называют эндэргоническими, если ΔH<0 ΔG< 0 ΔH>0 =ΔG>0 ΔG=0 Чтобы рассчитать время наступления скорости реакции нужно ... 1/время появления признаков реакции (сек.) =время появления признаков реакции (сек.) / 2 1/время появления признаков реакции (сек.) + время появления признаков реакции (сек.)*0,5 время появления признаков реакции (сек.) * 2 2 время появления признаков реакции (сек.) Фактор эквивалентности соляной кислоты равен 1. Молярная масса эквивалента равна =36,5 г/моль 35,5 г/моль 37,5 г/моль 72 г/моль 71 г/моль Минимальный запас энергии частиц в момент столкновения, необходимый для протекания химической реакции, называется =энергией активации энтальпией реакции энергией ионизации тепловым эффектом энергией жизни элемента Действие биологических катализаторов сводится к а) изменению теплового эффекта реакции, б) снижению энергии активации, в) увеличению скорости прямой и обратной реакций, г) избирательности. а, б, в, г =б, в, г б, г а, б, г а, б, в Реакции, в которых продукт первой элементарной стадии вступает в реакцию второй стадии и т. д., пока не образуется конечный продукт, называются параллельными =последовательными сопряженными эндэргоническими каталитическими pH раствора щелочи с концентрацией 0,001 равен 3 14 13 =11 7 Число молекул, реагирующих в одном элементарном химическом акте называется: =молекулярностью реакции порядком реакции по веществу общим кинетическим порядком реакции стехиометрическим коэффициентом вещества молярной концентрацией реакции Чем больше электродный потенциал окислительно- восстановительной системы, тем большими окислительными свойствами обладает электрон протон =окислитель восстановитель ион На сколько частиц диссоциирует дигидрофосфат натрия это вещество неэлектролит 4 3 =2 1 Температура кипения это… температура при которой давление пара растворителя над раствором становится равным давлению пара над твердой фазой =температура при которой давление пара растворителя над раствором становится равным атмосферному давлению температура при которой давление пара растворителя над раствором становится равным давлению пара над жидкой фазой температура при которой давление пара растворителя над раствором становится равным гидравлическому давлению температура при которой давление пара растворителя над раствором становится неравным атмосферному давлению При добавлении к раствору [Pt(NH3)3Cl3]Cl нескольких капель AgNO3 с ним вступит во взаимодействие … хлорид-ионов 4 3 0 2 =1 Дентантность лиганды – это: =число двухэлектронных σ-связей, образованных ею с комплексообразователем численное значение величины ее заряда общее число атомов химических элементов, входящих в ее состав число атомов, выделяемых ею для образования координационных связей с комплексообразователем нет верного ответа Укажите место действия глюкозо-эфирной буферной системы: = клетка продолговатый мозг синцитий симпласт кости Строение комплексных соединений объясняется теорией кислот и оснований комплексных соединений =координационной электролитической диссоциации растворов сильных электролитов Ионом-комплексообразователем в соединении K2[Co(NH3)(NO2)5] является Co3+ NO2- =Co2+ Co1+ NH30 Растворы ВМС – это системы: а) гомогенные; б) гетерогенные; в) равновесные; г) образующиеся самопроизвольно; д) образующиеся не самопроизвольно, требуют стабилизатора. а,в,д; =а,в,г б,в,г б,г а,г Для регенерации анионита его промывают раствором кислоты = раствором щелочи раствором хлорида натрия водой ацетоном На рисунке изображена 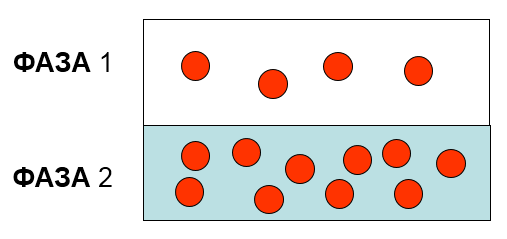 адсобрция =абсорбция сорбция гемосорбция хемосорбция Метод хроматографии предложил =М.С. Цвет Я.Х. Вант-Гофф Д.И. Менделеев А.М. Бутлеров А. Лавуазье 55. По принципу взаимодействия разделяемых компонентов смеси со структурными компонентами неподвижной фазы выделяют хроматографию: =Аффинную =Распределительную Тонкослойную =Адсорбционную =Осадочную |
