взаимозаменяемость. ответы на экзамен вопросы. 001 Металдарды кристалды рылысы. Металдарды кристалды торлары. Кристалдар асиеттеріні анизотропиясы
 Скачать 450.92 Kb. Скачать 450.92 Kb.
|
|
Бірінші блок 001 Металдардың кристалдық құрылысы. Металдардың кристалдық торлары. Кристалдар қасиеттерінің анизотропиясы Кристалдар (гр. krys-tallos – алғашқы мағынасы мұз) – атомдары мен молекулалары кристалдық тор түзетін қатты денелер. Кристалдар қатты денелердің тепе-теңдік күйі болып табылады. Белгілі бір термодинамикалық жағдайда (қысым, температура) кристалдық күйде болатын заттың нақты, тек өзіне тән кристалдық атомдық құрылымы болады. Бұл құрылым атомдардың орналасуына байланысты кристалдардың сыртқы симметриясын және олардың анизотропиялық қасиеттерін бейнелейді. Табиғатта және техникада кездесетін қатты материалдардың көпшілігі – поликристалдар. Олар ретсіз орналасқан ұсақ кристалдан (кристалиттерден) құралады. Бұған көптеген минералдар, металдар мен қорытпалар жатады. Кристалдың жеке ірі түрі монокристалл деп аталады. Табиғатта салмағы жүздеген килограммға жететін кварц, дала шпаты, флюорит кристалымен қатар мөлшері өте ұсақ алмас кристалы да кездеседі. Молекула-кинетикалық теориядағы термодинамикалық тепе-теңдік жағдайда өсірілген кристалдың пішіні белгілі бір симметриялы, дұрыс көпжақ түрінде болады. Олардың жақтары жазық болып келеді де, қырлары түзу сызық бойымен тұрақты бұрыш жасай қиылысады, яғни кристалдану кезінде кристалдың жақтары өзіне-өзі параллель жылжиды. Бұл заңдылық кристаллографияда бұрыштардың тұрақтылық заңы деп аталады. Барлық металдардың қалыпты жағдайда атомдары белгілі тәртіппен орналасып кристалл тор құрайды. Осыдан металдар атомдары бей-берекет орналасқан аморф денелерден ерекшеленеді. Жазықтықта металл атомдары белгілі тәртіппен орналасқан сүзгіні, ал кеңістікте атомдық кристалдық торды құрайды ###002 (номер вопроса) Материалдардың жіктелуі, жылу, электр, магниттік және оптикалық қасиеттерді зерттеу объектілері мен әдістері туралы ақпарат. ###003 (номер вопроса) Дислокация теориясы. Қосарланған және дискринация. Металдардың деформациясы кезіндегі процестерді түсіндіретін механизмдер. Ұзындық ақау - бұл құрылымның түзу сызықты болынуының бұзылуы (түзу сызықты болу міндетті емес) Кристалдың тұрақсыз, сызықты ақауларына нүктелі ақаулар тізбесі - бос орындар немесе түйін аралық атомдар жатады. Бұл ақаулар ұзақ уақыт бола алмайды. Атомдық жазықтардың дұрыс реттілігін бұзатын ерекше сызықтық ақаулар болатын дислокациялар кристалдарда тұрақты және стабильді болып келеді. Кристалдағы жақын ретті бұзатын нүктелік ақауларға қарағанда дислокациялар кристалдағы алыс реттерді бұзып, оның барлық құрылымын өзгертеді. Дислокацияның екі түрі болады: шеткі дислокациялары және бұрандалы дислокациялары. Кез -келген нақтылы дислокация өзімен бірге бұлардың екі түрін ұсынады. Дұрыс торлы кристалды паралельді атомдық жазықтықтардың тобы түрінде бейнелеуге болады (сур.2 а). егер бір кристал ішінде жазықтықтар қажалып жатса (сур.2 б), оның шеті шеткі дислокацияны құрайды. 2 суретте, дислокацияның басқа түрі көрсетілген - бұрамалық. Мұңда ешбір атомның жазықтығы кристалл ішінде аяқталмайды, бірақ жазықтықтың өздері тек шамалы параллельді және бір-бірімен сапқа тізіледі, не нақты кристал бұрамалык негіз ретінде жалғыз иілген атомдық жазықтықтан түзеледі. Шеткі дислокация экстражазықтық деп аталатын атом жазықтығының ажырасу нәтижесінде пайда болады, ол ішінде кристалдың жылжымалы бір бөлігінен басқа бағыттағы жылжу векторы r бір атомаралық қашқтықта болады. (3-сурет). Экстра жазықтық сына сияқты жұмыс атқарады, кристал ішіндегі өзінің төменгі шеттерін айнала кристалдық торды қатты бұзады. Кристалдың жоғарғы қабаты қысылған, ал төменгі жағы созылған, яғни экстра жазықтықтардың жоғарғы жағы атомаралық ара қашықтығы азырақ, ал төменгі жагы - бұрмаланбаған тордан көбірек. Түскен күштiң әсерінен дененің мөлшері мен сырт пішінінің өзгеруі д е ф о р м а ц и я деп аталады. Деформацияның тууына денеге түскен күштер немесе сол дененің бойында өтетін әртүрлі физикалық-механикалық процестер себепкер (мысалы, фазалық өзгеру процесінде кристалдың көлемінің өзгеруі) ###004 (номер вопроса) Аморфты материалдар туралы жалпы ақпарат. Аморфты материалдарды алу әдістері. Алғашқы адамзат танысқан кристалды емес құрылымды диэлектриктер – шынылар (әйнектер) жанартаулық негізді болған. Жанартаулық шыны немесе абсидиан сирек кездеседі. Бұрынғы ССРО-да оның біршама мол мөлшері Арменияда болған. Ол жақсы емес қара немесе сұр түсті және нашар өңделеді. Бұл жасанды шыныларды жасау қажеттілігіне әкеп соқты. Шыныларды жысау бес жарым мыңнан астам жыл бұрын игерілген. Сонау заманда египеттіктер тек күңгірт, мөлдір емес шыныларды, яғни әйнекейлерді (глазурлер) жасауды білген. Әйнекейлермен сазды құмыраларды су өткізбейтін, қолдануда ыңғайлырақ әрі көркемірек болу үшін қаптаған. Сосын әнекейлер мен тұрмыстық бұйымдарды әйнекейдің өзінен жасайтын болған. Негізінен шыны моншақтар, вазалар, құмыралар және т.б. Шыныдан жасалған бұйымдарды дайындау өте көп еңбекті талап ететіндіктен, Ежелгі Египетте мұндай бұйымдар өте сирек әрі асыл тастардан көп арзан болмаған. Аморфты және шынытәріздес заттар кристаллдық фазамен салыстырғанда құрамдары бірдей, энергия қорлары жоғары болады. Кристаллдық қатты дене балқығаннан кейін жақын реттердің барын сипаттайтын аймақтары құйманың құрылымдық көрінісі ретінде болып қала береді. Алайда, сұйық күйге ауысқан кезде 1-ші координациялық сферадан бастап құрылымдық өзгерістерге ұшырайды., жоғары температураларда еріген кезінде, әсіресе газдық фазада, ыдырау нәтижесінде ұсақ құрылымдық көріністер (фрагменттер) пайда болады. Алыс реттілік балқыған кезде жойылып кетеді. Егер кристаллизация және ұрық құру процесіне кедергі жасауына мүмкіндік болса, аморфты (шынытәріздес) қатты заттарды сұйық агрегаттық күйден (балқымадан немесе ерітіндіден) немесе газдық фазадан алуға болады. Балқыманың, ерітіндінің немесе газдық фазаның жоғары еркін энергиясы қатаю кезінде жарым-жартылай сақталады. Бұл жерде қатаю процесі туралы айтылып жатыр. Сонымен бірге кристаллдық қатты денелерге энергия берілген кезде сұйық пен газдық фазаларды өтіп аморфты(шынытәріздес ) күйге ауысуы мүмкін. Синтездің әртүрлі варианттарын жүйелеп диаграмма түрінде көрсетуге болады ###005 (номер вопроса) Материалдардағы иондық, ковалентті, металл және молекулалық байланыс. Кристалдық торлардың негізгі түрлері. Құрылымды зерттеу әдістері. Иондық байланыс деп – иондар арасындағы байланысты айтады. Металл мен бейметалл арасында түзіледі. Ион – бұл электрон беру немесе алу нәтижесінде түзілетін зарядталған бөлшек. Кристалдық тор – кристалл заттардағы атомдардың, иондардың, молекулалардың белгілі бір ретпен орналасуы. Кристалдық тор бір-біріне тығыз орналасқан параллелепипедтерден немесе кубтардан тұрады. Параллелепипед пен кубтар кристалдық тордың ұяшығы болып табылады. Атомдар, иондар немесе молекулалар орналасқан параллелепипедтің төбелері (бұрыштары) кристалдық тордың түйіндері, ал олар арқылы өтетін түзу сызықтары қатарлары деп аталады. Бір қатарда жатпайтын үш түйін арқылы өтетін жазықтықты жазық торап дейді. Элементар ұяшықтың үш бағыттағы сызықтық өлшемдері мен оның жақтарының аралық бұрыштары кристалдық тордың параметрлері болып табылады. Кристалдық тордың өлшемдері, атомдары мен молекулалардың орналасуы рентгенография, электронография, нейтронография көмегімен анықталады. Кристалдық тор статистикалық тұрғыдан тұрақсыз болады, атомдар мен иондар өзінің тепе-теңдік қалпынан белгілі бір амплитудада тербеліп тұрады. Температура өскен сайын бұл тербеліс артады, ал балқу температурасына жеткенде, кристалдық тор ыдырап, зат сұйықтыққа айналады. 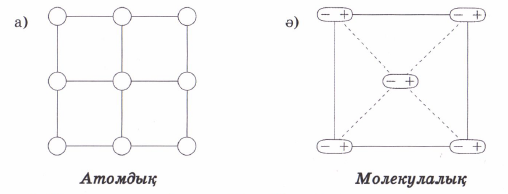 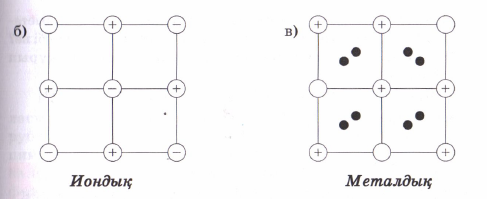 Атомдық кристалдық торлы заттарда (а) байланыс ковалентті, оны үзу үшін арнайы химиялық реакциялар жүргізу қажет. Қалыпты жағдайда олардың барлығы қатты, балқу температуралары жоғары, ерігіштігі өте нашар заттар. 2. Молекулалық кристалдық торлы заттар (ә) түйіндерінде молекулалар орналасқан, ал молекулааралық тартылыс күші өте аз болуына байланысты мұндай кристалдық торлы заттардың көпшілігі қалыпты жағдайда газ күйінде кездеседі. Оларды қыздырғанда оңай балқиды немесе температура әсерінен ыдырап кететін беріктігі нашар қосылыстарға жатады. . Ионды кристалдық тop (б) түйіндерінде иондар орналасқан, олар суда жақсы ериді, ерітінділері мен балқындылары электр тоғын жақсы өткізетін қатты заттар. 4. Металдық кристалдық тop (в); Металдарда металдық байланыстар болады, себебі кристалдық торларының түйіндерінде металл атомдары мен иондар орналасқан, ал металдың көлемінде электрон бұлттары (валенттілік электрондар оңай белініп шығады, өйткені олар ядромен нашар байланысқан) еркін қозғалып жүреді. Осы электрондар металдық қасиеттерді анықтайды: а) жоғары жылу және электрөткізгіштік ә) металдық, жылтыр б) созылғыштық, тапталғыштық ###006 (номер вопроса) Ұғымдар: компонент, фаза, құрылымдық компонент. Микро және макроанализ. Материалдарды зерттеудің физикалық әдістері туралы түсінік. ###007 (номер вопроса) Кристалл құрылымыныңақаулары. Ақаулардыңтүрлері, олардыңжіктелуі, қасиеттерінеәсері. Салқындату жылдамдығына байланысты қатты денелерді кристалдану (қатаю) кезінде аморфты және кристалды деп бөледі. Металдардың түрлі кристалдық торлары кездеседі. Солардың ішінде жиі кездесетін үш түрі болады (4.3 сурет): көлемге шоғырланған текше тор; жағына шоғырланған текше тор; тығыз гексагоналды кристалдық тор. Нақты кристалдарда әрқашан түрлі құрылымдық ақаулар байқалады. Олар кристалл торында атомдардың орналасу ретінің бүлінуінен түзіледі. Кристалл торының бүлінуінің түрі мен дәрежесіне қарай металдың қасиетіне әсері де әркелкі болады. Кристалдың құрылымдық ақаулары геометриялық белгілері бойынша нүктелік, сызықтық, беттік және көлемдік деп ажыратылады. Енді осылардың әрқайсысына тоқталып кетейік. Нүктелік ақауларға вакансиялар және түйінаралық атомдар жатады. Нүктелік ақаулардың өлшемдері бірнеше атом диаметрінен аспайды. Олар атомдардың жылу тербелістері, пластикалық деформация, металда зиянды қоспалардың пайда болуы нәтижесінде түзіледі. Түйінаралық ақаулар – атомның кристалл торының түйінінен түйіндер арасына өту нәтижесінде түзіледі. Ал кристалл торының түйінінен атом түйін арасына өтуінен вакансия түзіледі. Нүктелік ақаулардың болуы кристалл торының бұрмалануына себеп болады (4 ә сурет). Сызықтық ақаулар дислокация (5 сурет) деп аталады. Дислокацияның келесі түрлерін ажыратуға болады: шеткі, бұрама және аралас. Шеткі дислокация кристалл торының жергілікті бұрмалануы нәтижесінде түзілсе, ал бұрама дислокация кристалдың жазықтық бойымен толық емес жылжуы нәтижесінде түзіледі. Дислокациялар кристалдану процесі, термиялық және химия-термиялық өңдеулер, пластикалық деформация және қорытпалардың құрылымына ықпал ететін басқа да әсерлердің нәтижесінде түзіледі. Беттік ақаулар – түйіршіктердің арасындағы жазықтық, демек шекаралар. Түйіршіктер арасындағы шекараның ені 5-10 атом аралыққа тең. Техникалық металдардың шекараларында қоспалар шоғырланады. Түйіршік шекараларында атомдардың орналасуы оның ортасындағы атомдардың орналасуына қарағанда ретсіз болады. Көлемдік ақауларға қуыстар мен макрожарықшалар жатады. Аталған барлық ақаулардың металдар мен олардың қорытпаларының қасиеттеріне әсері мол. ###008 (номер вопроса) Нүктелік ақаулар. Нүктелік ақаулардың түрлері, диффузияның негізгі механизмі ретінде нүктелік ақаулардың ауысуы. Нүктелік ақауларға вакансиялар және түйінаралық атомдар жатады. Нүктелік ақаулардың өлшемдері бірнеше атом диаметрінен аспайды. Олар атомдардың жылу тербелістері, пластикалық деформация, металда зиянды қоспалардың пайда болуы нәтижесінде түзіледі. Атомдар кристалл торының түйінінде тербелмелі қозғалыста болатындығы белгілі, ал температураның өсуі тербелмелі қозғалыстың амплитудасын жоғарылатады. Металдың берілген кристалдық торындағы атомдардың энергиясы бірдей (орташа) болады, бірақ кейбір атомдардың энергиялары орташа шамадан жоғары болатындықтан бір жерден екінші жерге жылжуы мүмкін. Жылжып кеткен атомның босаған орнын – вакансия дейміз. Мұндай атомдар, әсіресе беткі қабатқа жақын орналасқан жазықтықтың бетіне шығып, ал олардың орнына беткі қабаттан алыс орналасқан келесі қабаттардың атомдары жылжып орын алады. Сонымен вакансия кристалдық торға терең ене береді. Нәтижесінде вакансия кристалдық торды бұрмалайды (4 а сурет). Температура көтерілген сайын және қысыммен өңдеуден кейін және басқа да өңдеу түрінен кейін вакансиялар саны көбейеді. Металдарда және олардың қорытпаларында диффузия процесі көбінесе вакансия механизмі бойынша өтеді. Диффузияның вакансия механизімі: вакансия орнына бірінші атом ауысады, ал бірінші атом орнына екінші атом, сөйтіп бірінің босаған орнын келесі атом толтыра береді. 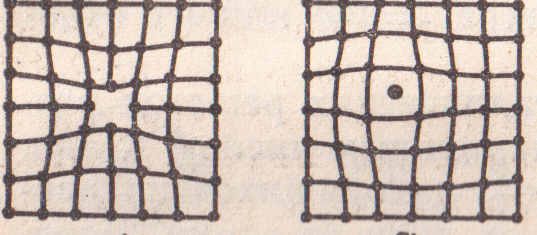 Кристалл торының нүктелік ақаулары: а — вакансия; б — түйінаралық атом ###009 (номер вопроса) Құрылымдық болаттар. Ыстыққа төзімді болаттар. Болатперлитті, мартенситтіжәне мартенсит-ферриттікластары. Ыстыққа төзімді болаттар дегеніміз - материалдың жоғары температурада пластикалық деформациялану және бұзылуына қарсылық көрсетер қабілеті. Қызуға берік материалдардан жоғары температурада пайдаланатын бұйымдар, бөлшектер ( бу және газ жіберетін құбырлар, қазан бөлшектері) дайындалады. Жоғары температурада дайындалатын материалдар құрылымындағы дара түйіршіктің бойында дислокациялардың өздігінен жылжу құбылысы кездеседі. Мұндай құбылыс материалдың істен шығуына әкеліп соғады. Сондықтан қызуға берік материалдар өндіруде осы құбылысты туғызатын факторлар есепке алынады. Мысалы, автомобильдің іштен жанатын двигателін жасайтын болат сильхром деп аталады. Сильхром- хромдыникельді болат, жұмыс атқару қабілеті 500... 600 0С-қа дейін жарамды. Жұмыс температурасы одан жоғары жағдайда 7000С-қа дейін хромдыникельді аустениттік болат пайдаланылады. Қызуға беріктігін көтеру мақсатымен аустенитті болаттар қосымша вольфрам, молибден, ванадий т.б. элементтермен легірленеді. Сильхром топты болаттардың кейбір маркалары: 4Х9С2, Х6С т.б. Перлит – аустениттің ыдырауынан туындаған өнім, феррит пен цементиттің механикалық қоспасы. Микроскопта күңгірт тілікше тәрізді болып көрінеді. Қаттылығы- HB 1200-1800 МПа. Құрамындағы көміртегі 0,8%. Болатты V ³ Vкр жылдамдығымен суытқанда аустениттің асыра суыну температурасында диффузия процесінің жүруі мүмкін емес. Мұндай жағдайда аустениттің полиморфты (g®a) өзгеруі диффузиясыз мартенситке өзгереді. Демек көміртегінің мөлшері бастапқы фазада (аустенитте) қандай болса соңғы фазада (мартенситте) сондай болады. Сондықтан мартенсит – көміртегінің a-Fe –дегі аса қаныққан қатты ерітіндісі. Сол себепті көміртегінің мөлшері 0,02 %C тұратын ферриттің (a-Fe) кристалдық торынан өзгешелігі мартенситтің кристалдық торының бір бойы созылған, тетрагональді (8.2,б – суреті). 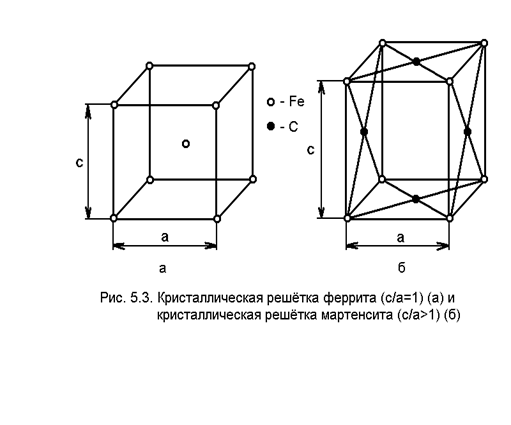 а) ферриттің кристалдық торы, с/а = 1: б) мартенситтің кристалдық торы с/а > 1 8.2 – сурет. Көміртегінің альфа-темірдегі ену қатты ерітінділері Мартенситтің қаттылығы HB600-650 (HRC62-66), созылымдылығы (d и y) және соққы тұтқырлығы (КС) нөлге жуық. Мартенситтің тығыздығы басқа құрылымдардың тығыздығынан төмен 7,75г/см3 болады. Мартенситтік өзгеріс кезінде болат құрылымының көлемі бірнеше пайызға дейін ұлғайады. Мартенсит алдымен бұйымның беткі қабатынан басталып түзіледі де, өзегіне қарай біртіндеп дамиды. Сонымен, болаттың көлденең қимасындағы температураның бірдей еместігінен құрылым кернеулері пайда болады. Сөйтіп, шынықтыру кернеулерін термиялық және құрылымдық кернеулер құрайды. ###010 (номер вопроса) Металдардың кристалдануының термодинамикалық негіздері, механизмі және кинетикасы Қатты заттар, кристалдық құрылысына байланысты, металдар, металл емес аморфты заттар болып екіге бөлінеді. Металдар мен металл қорытпаларының электр, жылу өткізгіштІк, пластикалық қасиеттері жоғары, металдық жарқылы бар. Олар қатты күйде кристалл торлардан құралады. Кристалл торлары белгілі заңдылықпен орналасқан атомдардан құралады. Атом электрондарыметалда газ молекулаларысияқтытәртіпсізқоз-ғалыстаболады. Металл злектрондарыатомдарменәлсіз бай-ланысқандықтанолардыжылу, электрөткізгіштікқасиеттері мен пластикалыққасиеттеріжоғарыболады. Қристаллденелердіңқаттыкүйденсұйықкүйгенемесесұйықкүйденқаттыкүйгеөтуібелгілібіртұрақтытемпературадаболады 3 Таза металл аbучастогындабіртіндепсуынып (1, а-сурет), bсучастогындабіразуақыттұрақтытемпературадаболады. Бұлучастоктаметалдыңтемпературасыbснүктесінесәйкесtктемпературасынажеткендеметалдыңкристалданупроцесі басталады.1-сурет. Суынуграфиктері: а -таза металдарүшін, б - корытындыларүшін, е - аморфтыденелерүшін.Металлтолықкристалданыпболғанша (bсучастогы) оныңтемпературасыезгермейді. Әйткенікристалданупроцесінде кристалл торларынбұзуғажұмсалғанжылу, жасырынбалқужылуытүріндеметалданбөлініп, оныңтемпературасынтұрактыжағдайдаұстайды. Металл сұйықкүйдентолыққаттыкүйгеайналып -болғансоң, температура сdсызығыбойыншабірқалыптытемендейді. Қорытпалардыңсуынупроцесі 1, б-суреттекөрсетілген. Қорытпалардыңкристалдануытұрақтытемпературадаемес, белгілі температура аралығындажүреді. Кристалданупроцесініңбасталуынасәйкестемператураныкристалданупроцесініңбастапқытемпературасы (tб), ал кристалданупроцесініңаяқталуынасәйкестемператураныкристал-данупроцесініңсоңғытемпературасыtсдепатайды. Аморфтыденелердіңбіркүйденекіншікүйгеөтуініңбелгілітемперату-расы болмайды (1, в-сурет).Сонымен, таза металдар мен қорытпалардыңсуынунемесеқыздыруграфигінде температура аялдамасыболады (b, сdучастоктары). ###011 (номер вопроса) Кристалдану параметрлері: кристалдану орталықтарының саны, орталықтардың өсу қарқыны. Кристалдану параметрлерінің гипотермия дәрежесіне (салқындату жылдамдығына) тәуелділігі және олардың астық мөлшері мен материалдардың қасиеттеріне әсері. Қорытпаның кристалдануы таза металдың кристалдану заңына сәйкес жүреді. Қорытпаның кристалдануында диффузиялық процестің атқаратын ролі үлкен. Себебі сұйық фазада бірбеткей орналасқан қорытпаны құраушы әртекті атомдардың қайтадан орын ауыстыруларын қамтамасыз ету керек. Бұдан басқа да қатты күйдегі қорытпада оны құраушы компоненттердің полиморфты өзгеруі немесе қатты ерітіндінің ыдырауынан туған қайта кристалдану процесі жүруі мүмкін. Мұндай өзгеру қорытпаның қатты күйіндегі фазаларының өзгеруі деп аталады. Диффузия арқылы жүретін бұл процесс температура төмендегенде баяулайды. Сол себепті кристалданған қорытпаның тепе-теңдік күйінен айырылуы жиі кездеседі. Қатты қорытпаның қайта кристалдану реті кристалдану орталықтарының пайда болып, температураның төмендеуіне қарай олардың өсіп дамуымен жүреді. Әдетте кристалдану орталықтары тор құрылысындағы ақауы бар жерлерге орналасады немесе жаңа кристалдар орталықтары болуға жарайтын кірмелер бар жерде ескі фазалардың түйіршіктері шекарасында пайда болады. Деформациялау температурасы мен қайта кристалдану температурасының ара қатынасына қарай деформация салқын және ыстық болып ажыратылады. Салқын деформация қайта кристалдану температурасынан төменгi температурада жүредi. Cондықтан салқын деформацияланған металдың берiктiгi артады. Қайта кристалдану температурасынан жоғары температурада жүретін деформация ыстық деформация деп аталады. Ыстық деформация кезінде металдың берiктiгi көтеріледi, бiрақ бұл температурада жүретін қайта кристалдану процесi оны жартылай немесе толығымен жойып отырады. Ыстық деформация температурасы қорытпаның құрамына қарай (0,7-0,75)Тпл өрнегiмен анықталынады. ###012 (номер вопроса) Металл қорытпаларындағы фазалар мен құрылымдар (қатты ерітінділер, химиялық қосылыстар, аралық фазалар, қоспалар) және олардың түзілу шарттары. Металл қорытпалары бойында металға тән механикалық және технологиялық қасиеті бар екі немесе одан көп элементтерді балқытып немесе басқа жолдармен біріктіру арқылы алынатын зат. Қорытпа құраушы компоненттердің бір-бірімен физикалық-химиялық әрекеттесуіне байланысты келесі фазалар: сұйық фаза, қатты ерітінді, химиялық қосылыс түзіледі. 3.1 Қатты ерітінді Көптеген қорытпалар кристалдану процесінде құрамындағы элементтердің атомдарының бірқалыпты орын ауыстыруын және бір - бірінде ерігіштік қабілетін сақтайды. Балқыған металл кристалданғанда қорытпаны құраушы компоненттердің біреуі өзінің алғашқы кристалдық торын сақтап, ал басқа компоненттердің атомы сол тордың бойына мөлшерін өзгертпей орналасса, мұндай фаза қатты ерітінді деп аталады. Екі немесе одан көп компоненттерден құрылған қатты ерітіндінің кристалдық торы бір типті болып, бір фазадан түрады. Атомдардың кристалдық торда орналасуына қарай ерітінділер ену қатты ерітіндісі (18,в суреті) және орын басу қатты ерітіндісі (18, б суреті) болып бөлінеді.  а) – таза металл; б) – орын басу қатты ерітіндісі; в) – ену қатты ерітіндісі. 18- сурет. Қатты ерітіндінің кристалдық торы. Орын басу қатты ерітіндісі еріткіш компоненттің кристалдық торындағы кейбір атомдардың орнын ерігіш компоненттің атомдарының басуы арқылы құрылады. Ену қатты ерітіндісі еріткіш компоненттің кристалдық торындағы түйінаралыққа ерігіш компоненттің атомдарының орналасуы арқылы құрылады. Ерігіш және еріткіш компоненттердің электрондық құрылысы және атомдарының мөлшері әртүрлі. Ену қатты ерітіндісі құрылғанда атомдардың мөлшеріне қарай кристалдық тор керіліп немесе сығылып құрылса, орын басу қатты ерітіндісі құрылғанда кристалдық тор периоды үлкейе бастайды. Ену қатты ерітіндісі құрылу үшін ерігіш компоненттің атомдық радиусы еріткіш компоненттің атомдық радиусынан кіші болу керек және ол орналасатын кеңістіктің мөлшеріне сәйкес келу керек. Мысалы, ену қатты ерітіндісінің темірде, молибденде, хромда т.б. металдарда құрылуына көміртегі (атом радиусы 0,077 нм), азот (0,071 нм), сутегі (0,046 нм) тағы сол сияқты ерігіш компоненттердің атомдық радиусы кішкене болуы қажет. Металдың қайсысы болса да қатты күйінде әртүрлі дәрежеде бір - бірінде еруі мүмкін. Мысалы, алюминийде мыстың 5,5 % ерісе, мыста мырыштың 39 %-ы олардың кристалдық тор типін өзгертпей ериді. Металдың бір - бірінде еру қарқынына қарай шексіз еритін және шектеулі еритін қатты ерітінді деп ажыратуға болады. Ену қатты ерітіндісі тек шектеулі болады, себебі негізгі металдың атомдары тор түйініндегі орындарын сақтап қалады да, ерігіш компоненттің атомдары тордың шектеулі бос орындарына орналасады. Орын басу қатты ерітіндісі шексіз еру үшін келесі шарттар орындалуы қажет: 1) компоненттердің кристалдық торларының бір типті болуы; 2) компоненттердің атомдарының мөлшерінің айырмашылығы 8-15%-дан аспауы керек; 3) компоненттер Д.И.Менделеев кестесі бойынша бір топта болуы немесе көршілес топқа жатуы керек, демек, атомдардың электрондық қоршауының құрылысы ұқсас болу керек. Тек сонда ғана қатты ерітіндінің концентрациясы өзгеріп, компоненттердің бір кристалдық тордан екінші кристалдық торға біртіндеп ауысуына мүмкіндік туады. Қатты ерітіндінің қасиеті металға жуық, қызған немесе суық күйінде де созымталдығы жоғары. Қатты ерітінділерді металтануда a, b, g т.б. грек әріптерімен белгілеу қабылданған. ###013 (номер вопроса) Екі компонентті қорытпалардағы тепе-теңдіктің термодинамикалық шарттары. Қорытпадағы фазалардың құрамы мен температурасына байланысты өзгеретіндігін «фазалық тепе-теңдік диаграммасы» арқылы көруге болады. Металл мен қорытпалардың өзгеру процесі фазалар ережесі немесе фазалық Гиббс ережесі деп аталатын тепе-теңдік заңына тәуелді. Фазалар ережесі жүйенің еркіндік дәрежесі және фазалардың, компоненттердің сандарының арасындағы қатынасын, оның бір-біріне тәуелділігін көрсететін физикалық-химиялық заңға негізделген. Жүйедегі фазаның күйі оның сыртқы (температура, қысым) және ішкі (концентрациясы, құрамы) факторлары арқылы анықталады. Фазаның бір күйден екінші күйге ауысуы жүйенің физикалық қасиеті мен ішкі құрылыстарының күрт өзгеруімен қатарласып жүреді. Фазалық өзгеру кристалдық торлардың толық бұзылуына (балқуы) немесе қайтадан кристалдық торлар құруына (кристалдану) немесе кристалдық тордың бір түрден екінші түрге ауысуына әкеліп соғады. Аталған өзгерістер жүру үшін белгіленген мөлшерде жылу әсерін тигізу керек. Мұндай жылу өзгерісі жасырын жылу деп аталады. Фазалар ережесі келесі математикалық теңдікпен өрнектеледі: с = к-ф+2, мұнда с – еркіндік дәреже саны, к – компоненттер саны, ф – жүйедегі тепе-теңдікте болатын фазалар саны, 2 – сыртқы әсерлер саны. Еркіндік дәреже санына жүйедегі фазалардың санын өзгертпей өздігінен өзгеретін факторлар (температура, қысым, концентрация) саны жатады. Сыртқы әсерлер санын атмосферадағы қысым тұрақты болғандықтан, бірлік санына теңеп, өрнекті с = к – ф + 1 деп қарастырады. Фазаларөзгеруініңкөптегенерекшеліктерінфазаларережесінесүйеніптүсіндіругеболады. ###014 (номер вопроса) Гиббс энергиясының қорытпаның күйіне тәуелділігі. Металдың сұйық күйден қатты күйге ауысуы кристалдану деп аталады. Кристалдану процесі жүру үшін сұйық фазаның Гиббс энергиясы (еркіндік энергиясы) кристалдың Гиббс энергиясынан жоғары болу керек, тек сонда ғана жүйе термодинамикалық тұрақты күйге жетіп, кристалдану жүреді. Еркіндік энергия (G) – жылу қозғалысымен қамтылған көп санды бөлшектерден (атомдар, молекулалар) тұратын, жүйенің энергетикалық күйін сипаттайтын термодинамикалық функция. Табиғатта өздігінен жүретін өзгерулерге (кристалдану, балқу) себепші. Еркіндік энергиясы жоғары жүйе тұрақсыз болғандықтан, қандай зат болса да мүмкіндігінше энергиясын аз жұмсайтын күйге ауысуға ұмтылады. 11- суретте металдың сұйық және қатты күйіндегі Гиббс энергиясының температураға байланысты өзгеруі көрсетілген. Егер түрлену кезінде көлемдік өзгеру шағын болса, онда G =E-TS, мұндағы E – толық энергия (фазаның ішкі энергиясы), T – абсолютті температура, S – энтропия. 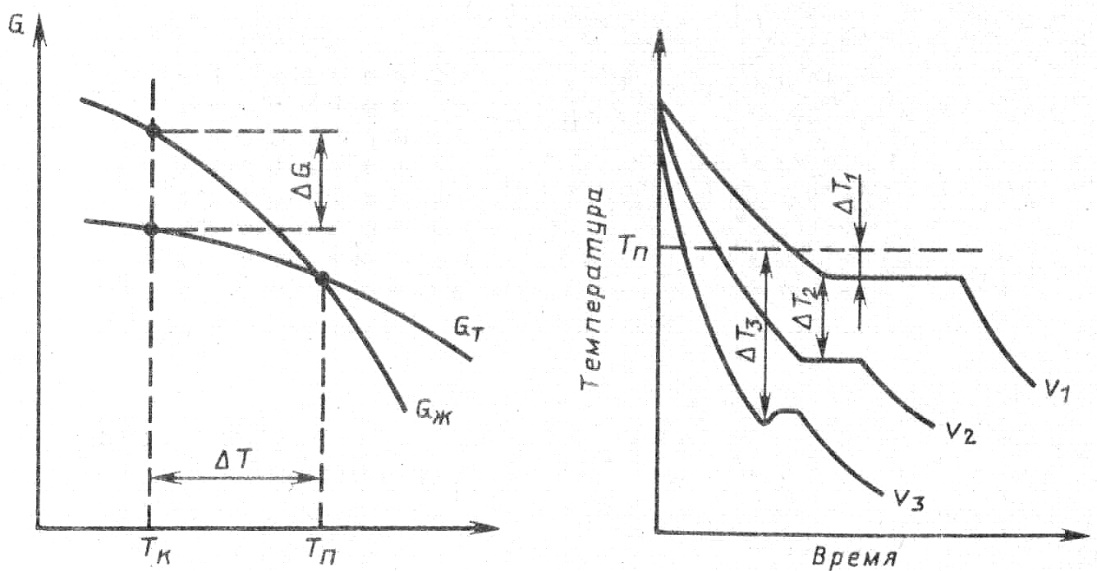
Тп температурасынан жоғары температурада сұйық тұрақты (еркіндік энергиясы төмен), ал одан төмен температурада қатты металл тұрақты болып келеді. Тптемпературасындасұйық металл мен қаттыметалдың Гиббс энергиясы тепе-тең. Бұл температура теориялықкристалдану (балқу) температурасыдепаталады. Кристалданупроцесібұлтемпературадабасталақоймайды. Кристалданупроцесіжүруүшінқатты металл мен сұйықтықтыңарасында Гиббс энергиясыныңайырмасыболуыкерек. Демек, кристалданупроцесіжүруүшінсуынутемпературасыжүйедегі тепе-теңдіктемпературасынанТптөмен. КристалданупроцесінқамтамасызететінТпжәнеТктемператураларыныңайырмасыD Т асырасуынудәрежесідепаталадыD Т =Тп-Тк. Әртүрліжылдамдықпенсуынған таза металдыңкристалданупроцесініңсипаттамасы 12 - суреттегітермиялықграфиктерарқылыкөрсетілген. ӨтебаяусуытукезіндеасырасуынудәрежесіD Т төменболады, сондықтанкристалданупроцесі тепе-теңдіктемпературасынаТптаяутемпературадажүреді (12 - сурет,V1). Суынуграфигіндегікристалданутемпературасыбойындағыкөлденеңалаң - суынупроцесіндебөлініпшыққанжылудыңорнынкристалданупроцесіндебөлініпшығатынжасырынжылументолтырылыпотырылуыныңкөрсеткіші. Суынужылдамдығыартқансайын (V2,V3 сызықтары) асырасуынудәрежесікөтеріліп, кристалданупроцесі тепе-теңдікТптемпературасынанәлдеқалайтөментемпературадаөтеді. Өте таза металдыңасырасуынудәрежесіD Т мейліншеүлкенболады, бірақ та 10-30 0С аспайды. Кристалданупроцесі кристалл өскіндері (кристалдануорталықтары) пайдаболуынанбасталады да, олардың саны көбейіп, мөлшеріөсуіменбіргеәріқарайжалғасады. 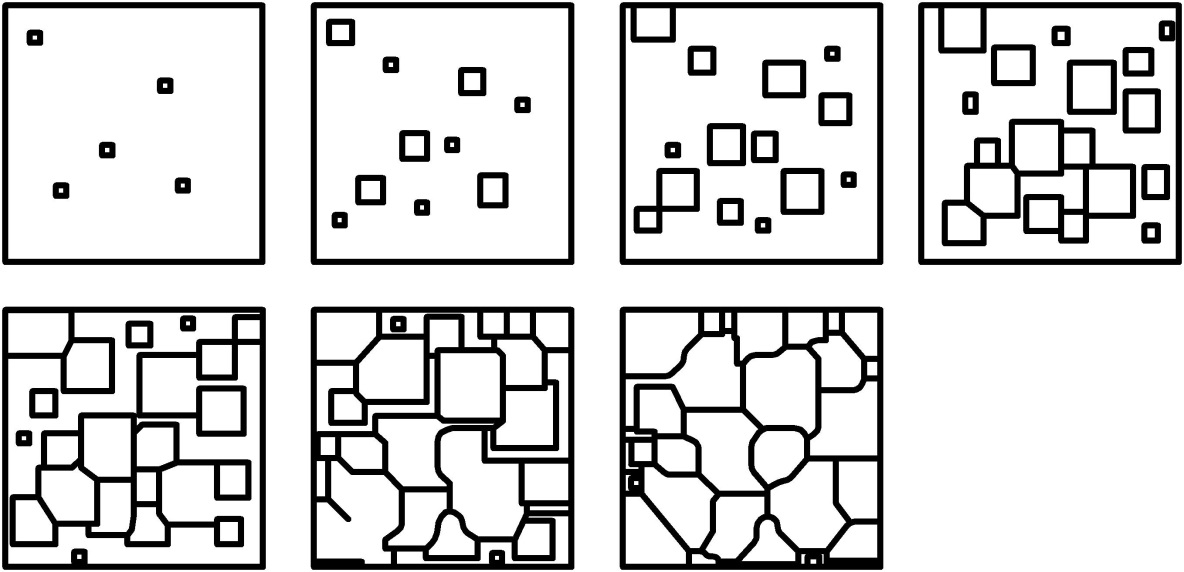 13 – сурет. Металдыңкристалданусұлбасы. ###015 (номер вопроса) Компоненттердің бір-біріне толық және толық емес ерігіштігі, компоненттердің шектеулі ерігіштігі кезінде эвтектикалық түзілу жағдайлары үшін фазалық тепе-теңдік диаграммалары. Жүйелер гомогенді және гетерогенді болып екіге бөлінеді. Бірдей фазадан құралған жүйе гомогенді деп аталады. Бірнеше фазадан құралған жүйе гетерогенді дейді. Мысалы, бірнеше газдардың қоспасы бір фазадан, ал ішінде мұз түйіршігі бар салқын су немесе су мен бу екі фазадан тұрады. Компонент дегеніміз жүйеден бөліп алғанда өз қасиетін, құрамын ешбір өзгеріссіз ұзақ мерзімге дейін сақтайтын, біріңғай химиялық құрылымдағы бөлшек. Оған мысал ретінде мұз, су, буды алайық. Егер бір жабық ыдыста мұз, су, буды тепе-теңдік жағдайында ұстасақ, бірдн үш агрегаттық күйді байқаймыз. Мұндағы мұздың да, судың да, будың да химиялық құрамы бірдей, демек жүйе бір компонентті. Фазалық түрлену немесе фазалық ауысу деп заттардың бір фазадан екінші фазаға ауысуын айтады. Фазалық ауысу 2 класқа бөлінеді. Бірінші текті фазалық ауысуға булану, возгонка және балқу жатады.Бұл ауысу кезінде жылу бөлінеді немесе сіңірледі және фазалардың көлемі өзгереді. 2 ретті фазалық ауысу мұндай қасиеттерді көрсетпейді. Тепе-теңдік жағдайындағы гетерогендік жүйедегі температура (Т), қысым (р), химиялық потенциал (μ) және де басқа біріктірілген күштер жүйеде өзгермейді, ал энтропия (S), көлем (V), жылу сыйымдылығы (Ср,С V) фаза шекарасында секірмелі өзгереді. Химиялық термодинамикада жүйелердің еркіндік дәрежелерінің саны немесе варианттылығы деген түсініктердің орны ерекше. Құрамындағы тәуелсіз компоненттердің санына сәйкес термодинамикалық жүйелер бір компонентті, екі компонентті, үш компонентті т.б. болып бөлінеді. Мұндағы компонент саны кезкелген фазаның құрамын анықтауға болатын заттың ең аз мөлшерімен анықталады. Мысалы, мырыш нитратын суда ерітіп, енді осы ерітіндіден су мен мырыш нитратын әр түрлі әдістермен бөліп кристаллогидраттар алады. Әйтсе де бұл жүйе екі компонентті, өйткені су мен мырыш нитратынан бұл жүйенің кез келген кристаллогидратты фазасын алуға болады. Күрделі жүйенің тәуелсіз компоненттер санын осы заттардың концентрациялармен байланысқан теңдеу санын шегеру арқылы анықтайды. Ал тепе-теңдік жағдайында фаза саны шексіз болмайды. Мұндағы фазалар саны 1876 жылы Гиббс тұжырымдаған фазалар ережесінің көмегімен анықталады. Жүйеге мысалы, электрлік не магниттік өріс, гравитациялық күштер, температура, қысым сияқты тағы да басқа сыртқы күштер әсер етуі мүмкін. Жүйеге жоғарыда келтірілген факторлардың арасындағы қысым мен температурадан басқаларды ешбір әсер етпейтін болса, Гиббстің фазалар ережесін мынадай теңдеумен өрнектеуге болады: Ф + С = k +2 Ф-тепе-теңдік жағдайындағы гетерогенді жүйеде болатын фазалар саны; С- жүйедегі еркіндік дәреже саны немесе варианттылық; k- жүйедегі компоненттер саны. Тепе-теңдік гетерогенді жүйеге сыртқы факторлар арасынан тек қысым мен температура әсер еткенде, фазалар саны мен еркіндік дәреже санының қосындысы компонент санына екіні қосқанға тең. Мұндай Гиббстің фазалар ережесі немесе тек фазалар ережесі дейді Сонымен фазалар ережесін термиялық, механикалық және химиялық тепе-теңдік жағдайынан қорытып шығаруға болады. Мұндағы екі жағдай, атап айтқанда термиялық және механикалық жағдайлар тепе-теңдіктегі барлық фазалардың температура мен қысым тепе-теңдігін білдіреді, ал үшінші-барлық фазалардағы әрбір компоненттің химиялық потенциал тепе-теңдігін көрсетеді. Егер Ф фаза тепе-теңдікте болып, осы фазалар арасында k компоненті таралса, онда жоғарыдағы үшінші жағдайдан температура, қысым және құрамды байланыстыратын (Ф-1) k теңдеуі шығады, өйткені химиялық потенциал осы көрсетілген айнымалы шамаларға функционалды. Ал, егер қысым, температура және құрам алдын ала белгілі болса, онда әрбір фазаның күйі оңай табылады, себебі олардың құрамы компоненттердің концентрациялармен анықталады. Ендеше, тепе-теңдік жағдайындағы барлық фазалар күйін анықтау үшін қажет болатын жалпы айнымалы саны (k-1)ф+2. Ал, егер жүйені екіге бөлсек, онда екі бөліктегі тепе-теңдік жағдайдың өзінде қысым өзгеше болады. Мысалы, осмометрде тепе-теңдік орнағанның өзінде мембрананың екі жағындағы қысым әр түрлі. Мұндайда тепе-теңдіктегі барлық фаза күйін анықтауға қажетті айнымалы өлшемдер саны көбееді. Осмометрмен байланысты келтірілген мысалда ол (k-1)ф+3. өрнектегенге тең. Егер тәуелсіз айнымалы шамалар саны оларды өзара байланыстыратын теңдеу санына тең болса, онда осы теңдеу жүйенің әрбір айнымалының белгілі бір мәніне сәйкес келеді. Ал айнымалы теңдеуден артық болса, онда олардың айырмасы қалған айнымалыларды өзгерісссіз қалдырғандағы кез келген мәнге ие болады. 2 + (k-1)ф –k(ф -1) =c Бұл теңдеудегі жақшаны ашып, ұқсас мүшелерді біріктірсек, Гиббстің фазар ереже姮іне сәйкес теңдеу шығады. |
