колоквиум. 1. Липиды как класс органических веществ определение. В чем заключается биологическая роль жиров Каково их суточное потребление
 Скачать 0.73 Mb. Скачать 0.73 Mb.
|
|
5. Реакции синтеза триглицерида. Для синтеза нейтрального жира необходим глицерин в активной форме - глицерол-3-фосфат (фосфоглицерин). Глицерол-3-фосфат может быть получен двумя способами: Кроме глицерина, для синтеза нейтрального жира необходимы жирные кислоты в активной форме. Активная форма любой жирной кислоты – Ацил-КоА. Образуется при участии фермента ацил-КоА-синтазы. 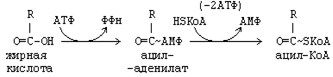 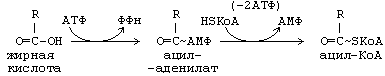 Следующим этапом на пути синтеза жира является реакция образования фосфатидной кислоты: Реакция катализируется ключевым ферментом липогенеза – глицерол-3-фосфатацилтрансферазой.  Билет 6 = 21 1.Какие этапы можно выделить в переваривании липидов в пищеварительном тракте? Каковы особенности переваривания триглицеридов у младенцев. Колипаза: в чем заключается ее участие в процессах пищеварения? Условно внешний обмен липидов можно подразделить на следующие этапы: 1. Эмульгирование жиров пищи - необходимо для того, чтобы ферменты ЖКТ смогли начать работу. 2. Гидролиз триацилглицеролов, фосфолипидов и эфиров ХС под влиянием ферментов ЖКТ. 3. Образование мицелл из продуктов переваривания (жирных кислот, МАГ, холестерола). 4. Всасывание образованных мицелл в эпителий кишечника. 5. Ресинтез триацилглицеролов, фосфолипидов и эфиров ХС в энтероцитах. После ресинтеза липидов в кишечнике они собираются в транспортные формы – хиломикроны (основные) и липопротеины высокой плотности (ЛПВП) (малое количество) – и разносятся по организму. Переваривание жиров, в свою очередь, можно разделить на следующие этапы: 1)переваривание в ротовой полости У взрослых в ротовой полости переваривание липидов не идет, хотя длительное пережевывание пищи способствует частичному эмульгированию жиров. 2)переваривание в желудке В желудке небольшая часть жиров гидролизуется под действием "липазы языка". Этот фермент синтезируется железами на дорсальной поверхности языка и относительно устойчив при кислых значениях рН желудочного сока. Поэтому он действует в течение 1-2 ч на жиры пищи в желудке. Однако вклад этой липазы в переваривание жиров у взрослых людей незначителен. 3)переваривание в кишечнике. Жиры - нерастворимые в воде соединения, они могут подвергаться действию ферментов, растворённых в воде только на границе раздела фаз вода/жир. Поэтому действию панкреатической липазы, гидролизующей жиры, предшествует эмульгирование жиров. Эмульгирование происходит в тонком кишечнике под действием солей жёлчных кислот. Жёлчные кислоты синтезируются в печени из холестерола и секретируются в жёлчный пузырь. Содержимое жёлчного пузыря – жёлчь, содержащая главным образом жёлчные кислоты; в небольшом количестве имеются фосфолипиды и холестерол. После приёма жирной пищи жёлчный пузырь сокращается и жёлчь изливается в просвет двенадцатиперстной кишки. Жёлчные кислоты располагаются на поверхности капель жира и снижают поверхностное натяжение. В результате крупные капли жира распадаются на множество мелких. Эмульгирование приводит к увеличению площади поверхности раздела фаз жир/вода, что ускоряет гидролиз жира панкреатической липазой. Эмульгированию способствует и перистальтика кишечника. Переваривание жиров - гидролиз жиров панкреатической липазой. Оптимальное значение рН для панкреатической липазы ≈8 достигается путём нейтрализации кислого содержимого, поступающего из желудка, бикарбонатом, выделяющимся в составе сока поджелудочной железы: Н+ + НСО3- → Н2СО3 → Н2О + СО2 ↑. Выделяющийся углекислый газ способствует дополнительному перемешиванию содержимого тонкой кишки. Панкреатическая липаза выделяется в полость тонкой кишки из поджелудочной железы вместе с белком колипазой. Колипаза – белок, вырабатываемый в поджелудочной железе, кторый при попадении в кишечник способен активировать панкреатическую липазу. Колипаза вырабатывается в виде неактивного предшественника – проколипазы, который активируется трипсином в кишечнике. Колипаза не является классическим активатором, она лишь связывает субстрат и приближает его к активному центру липазы. Переваривание жира у грудных детей: У грудных детей и детей младшего возраста основной пищей служит молоко. Молоко содержит жиры, в состав которых входят в основном жирные кислоты с короткой и средней длиной алифатических цепей (4-12 атомов углерода). Жиры в составе молока находятся уже в эмульгированном, смешанном с водой виде, поэтому они сразу же доступны для гидролиза ферментами. На жиры молока в желудке детей действует липаза, которая синтезируется в железах языка (липаза языка). Кроме того, в желудке детей грудного и младшего возраста вырабатывается желудочная липаза, которая активна при нейтральном значении рН, характерном для желудочного сока детей, и не активна у взрослых (рН желудочного сока -∼1,5). Эта липаза гидролизует жиры, отщепляя, в основном, жирные кислоты у третьего атома углерода глицерола. Далее гидролиз жиров молока продолжается в кишечнике под действием панкреатической липазы. Жирные кислоты с короткой цепью, как водорастворимые, всасываются частично уже в желудке. Остальные жирные кислоты всасываются в тонком кишечнике. Для детей грудного возраста основным источником энергии являются жиры, в то время как у взрослых людей при нормальном питании основным источником энергии служит глюкоза. Вследствие этого нарушение переваривания и всасывания жиров у детей более опасно, чем у взрослых. 3.Какие жирные кислоты являются незаменимым компонентом пищи? К незаменимым жирным кислотам относятся линолевая(С18:1 ) и линоленовая (С18:2) кислоты. Они не синтезируются в организме человека и поэтому должны поступать с пищей. Обычно организм не испытывает них недостатка, так как они содержатся в растительных продуктах (маслах), а также в рыбьем и курином жирах. В организме незаменимые жирные кислоты входят в состав клеточных мембран, а также являются предшественниками для синтеза биологически активных веществ, таких, как простагландины. Линолевая и линоленовая кислоты являются непосредственными предшественниками арахидоновой (С20:4) кислоты. Именно из арахидоновой кислоты синтезируются простагландины, тромбоксаны и лейкотриены. Простагландины действуют в тех клетках, где они синтезируются. Характер действия простагландина зависит от типа клетки. В этом заключается принципиальное отличие простагландинов от гормонов. Физиологические эффекты простагландинов: 1) простагландины усиливают воспалительные процессы; 2) регулируют приток крови к определенному органу; 3) моделируют синаптическую передачу. Лабильными продуктами превращения простагландинов являются тромбоксаны. Их функция заключается в том, что они участвуют в регуляции активности тромбоцитов. Являясь мощными стимуляторами образования тромбов, они способствуют агрегации тромбоцитов. Простациклины предотвращают агрегацию тромбоцитов. Лейкотриены - производные арахидоновой кислоты. Участвуют в иммунных процессах, воспалительных и аллергических реакциях, обладают спазмолитическим действием, влияют на артериальное давление и проницаемость сосудов. Билет 7= 22 1.Реакции активации жирных кислот. Жирные кислоты могут вступать в реакции только после активации. Активация жирных кислот принципиально отличается от активации углеводов. Реакция начинается с переноса от АТФ не фосфата, а АМФ, с образованием промежуточного продукта - ациладенилата. Затем с участием HS-KoA отщепляется АМФ, и образуется активная форма любой жирной кислоты – АЦИЛ-КоА. Образовавшийся АМФ не может превратиться в АТФ. Поэтому протекает еще одна реакция, и тоже – с затратой АТФ: АМФ + АТФ -------> 2 АДФ Распад 1 АТФ до АМФ энергетически равен распаду 2-х АТФ до 2-х АДФ. Поэтому затраты энергии на активацию жирной кислоты составляют 2 АТФ на одну молекулу жирной кислоты. 5. Какими реакциями синтезируется мевалоновая кислота? Ключевой фермент в биосинтезе холестерола. Где он локализован? Как осуществляется автономная саморегуляция? Ключевой фермент - ГМГ-КоА- редуктаза, который обнаруживается в эндоплазматическом ретикулуме всех клеток, обладающих способностью синтезировать холестерин . К ним относятся клетки печени , тонкого кишечника , надпочечников , половых желез . Регуляция происходит разными способами: 1.Фосфорилирование/дефосфорилирование ГМГ-КоА-редуктазы. При увеличении соотношения инеулин/глюкагон этот фермент дефосфорилируется и переходит в активное состояние. Действие инсулина осуществляется через 2 фермента: А)фосфатазу киназы ГМГ-КоА-редуктазы, которая превращает киназу в неактивное дефосфорилированное состояние; Б)фосфатазу ГМГ-КоА-редуктазы путём превращения её в дефосфорилированное активное состояние. Результатом этих реакций служит образование дефосфорилированной активной формы ГМГ-КоА-редуктазы. 2. Ингибирование синтеза ГМГ-КоА-редуктазы. Конечный продукт метаболического пути (холестерол) снижает скорость транскрипции гена ГМГ-КоА-редуктазы, подавляя таким образом собственный синтез. В печени активно идёт синтез жёлчных кислот из холестерола, поэтому и жёлчные кислоты (как конечные продукты синтеза) подавляют активность гена ГМГ-КоА-редуктазы. Так как молекула ГМГ-КоА-редуктазы существует около 3 ч после синтеза, то ингибирование синтеза этого фермента конечным продуктом метаболического пути (холестеролом) является эффективной регуляцией. 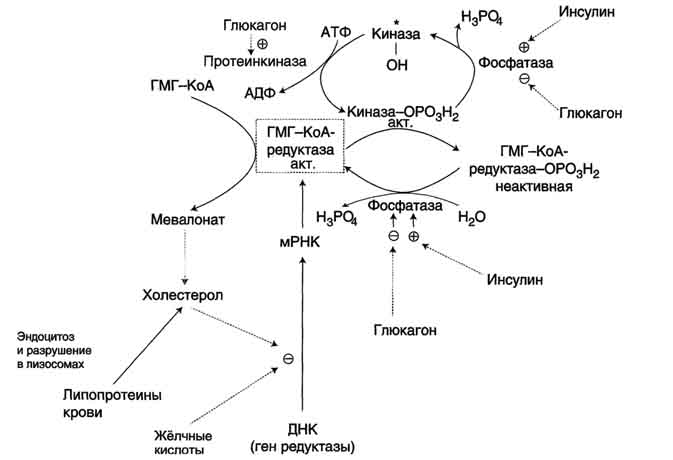 Билет 8 = 23 1.Назовите возможные пути синтеза глицерофосфолипидов. Представьте схему синтеа фосфотидилхолина. ГЛИЦЕРОФОСФОЛИПИДЫ (ГФЛ) - содержат спирт глицерин.Все они относятся к L-ряду. Есть асимметрический углеродный атом. Полярная группировка может быть представлена аминокислотой серином (фосфатидилсерин), холином (фосфатидилхолин, другое название – лецитин), этаноламином (фосфатидилэтаноламин), инозитолом (фосфатидилинозитол), глицерином (полиглицерофосфатиды).В природных фосфолипидах R1 и R2 - разные. R1 - насыщенная жирная кислота, R2.- ненасыщенная жирная кислота. Однако, есть и исключения: основным липидным компонентом легочного сурфактанта является ГФЛ, у которого и R1, и R2 – радикалы пальмитиновой кислоты, а полярная группировка – холин.  2.Для чего и как происходит перенос жирных кислот в матрикс митохондрий? β-Окисление жирных кислот, происходит в матриксе митохондрий, поэтому после активации жирные кислоты должны транспортироваться внутрь митохондрий. Жирные кислоты с длинной углеводородной цепью переносятся через плотную внутреннюю мембрану митохондрий с помощью карнитина. Карнитин поступает с пищей или синтезируется из незаменимых аминокислот лизина и метионина. В реакциях синтеза карнитина участвует витамин С (аскорбиновая кислота). В наружной мембране митохондрий находится фермент карнитинацилтрансфераза I, катализирующий реакцию с образованием ацилкарнитина. Образовавшийся ацилкарнитин проходит через межмембранное пространство к наружной стороне внутренней мембраны и транспортируется с помощью карнитинацилкарнитинтранс-локазы на внутреннюю поверхность внутренней мембраны митохондрий, где фермент карнитинацилтрансфераза II катализирует перенос ацила на внутримитохондриальный КоА. Таким образом, ацил-КоА становится доступным для ферментов β-окисления. Свободный карнитин возвращается на цитозольную сторону внутренней мембраны митохондрий той же транслоказой. На внутренней поверхности внутренней мембраны находится фермент карнитинацил трансфераза II, катализирующий обратный перенос ацила с карнитина на внутримитохондриальный КоА. После этого ацил-КоА включается в реакции β-окисления. 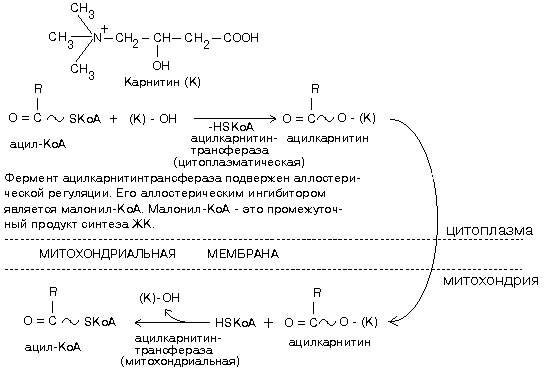 3.Реакции переваривания жира в кишечнике. Какие ферменты участвуют в этом процессе? 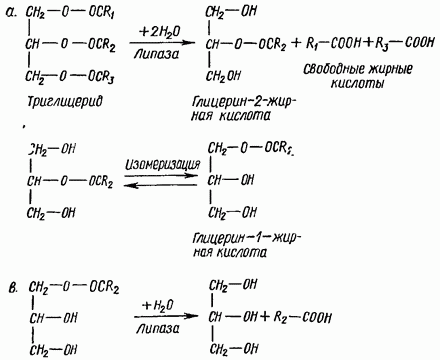 Ферменты: Язычная липаза. Вырабатывается клетками слизистой оболочки задней части языка. Действие этого фермента проявляется только в желудке (раньше считали, что это – желудочная липаза). Язычная липаза может переваривать уже эмульгированный жир. Ее pH-оптимум – 4-5. Поэтому в желудке взрослого человека язычная липаза неактивна. Реально жиры перевариваются язычной липазой только у младенцев. У взрослых людей переваривание жира идет только в кишечнике по схеме: «выделение желчи эмульгирование жира действие панкреатической липазы».
Образовавшиеся жирные кислоты и моноацилглицерины могут всасываться в кишечную стенку.
Таким образом, продуктами переваривания жира являются глицерин, жирные кислоты и моноацилглицерины. Всасываются продукты переваривания путем предварительного образования смешанных МИЦЕЛЛ с желчными кислотами. 5.Формула расчета прироста АТФ при распаде жирных кислот до СО2 и Н2О? 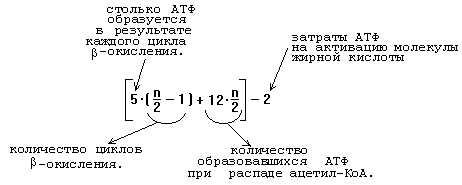 При распаде ненасыщенных жирных кислот образуется меньше АТФ. Каждая двойная связь в жирной кислоте - это потеря 2-х молекул АТФ. Билет 9 = 24 1. Формула фосфатидной кислоты 4. Гликолипиды, общая формула. Роль в составе мембран. Гликолипиды - Состоят из сфингозина, жирной кислоты и молекулы какого-либо углевода. Если в формулу СФЛ вместо фосфорной кислоты поставить какой-нибудь углевод, то получим формулу ГЛ. Гликолипиды тоже имеют гидрофильную "головку" и 2 гидрофобных "хвоста". Гликолипиды классифицируют в зависимости от строения углеводного компонента. Различают 2 группы гликолипидов: 1. ЦЕРЕБРОЗИДЫ. В качестве углеводного компонента содержат какой-либо моносахарид (глюкоза, галактоза), либо дисахарид, или нейтральный небольшой олигосахарид. 2. ГАНГЛИОЗИДЫ. Углеводным компонентом является олигосахарид, состоящий из разных мономеров, как самих моносахаридов, так и их производных. Этот олигосахарид обязательно кислый, в его состав обязательно входит сиаловая кислота. Благодаря определенной последовательности мономеров, олигосахариды в составе ганглиозида придают молекуле выраженные антигенные свойства. Функции: а) Участвуют в рецепции. б) Обеспечивают взаимодействие клеток друг с другом. в) Некоторые углеводные компоненты обеспечивают антигенную специфичность клеток. Например, эритроциты разных групп крови отличаются друг от друга по составу углеводных компонентов. 5. Избирательность фосфолипаз и их биологическое значение. Фосфолипаза — фермент, который гидролизует фосфолипиды. В зависимости от положения гидролизуемой связи в фосфолипиде различают 4 основных класса фосфолипаз: A, B, C и D. При образовании биологически активных веществ наибольшее значение имеют фосфолипазы "А2" и "С". Фосфолипаза А2 отщепляет ненасыщенные жирные кислоты, которые могут быть предшественниками биологически активных веществ. Фосфолипаза C - гидролизует связь между глицериновым остатком фосфолипида и полярной фосфатной группой, при этом образуются диацилглицерин и фосфат-содержащая полярная группа. Фосфолипаза D - гидролизует связь между фоасфатной группой и спиртовой группой, при этом высвобождаются фосфатидная кислота и спирт. Фосфолипаза A1 - отщепляет SN-1 ацильную цепь. Фермент не проявляет избирательности в отношении жирнокислотного состава фосфолипидов, но предпочтительно гидролизует отрицательно заряженные фосфолипиды (фосфатидную кислоту и фосфатидилглицерол). 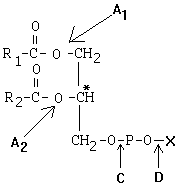 Билет 10 = 25 5.Какие липопротеины называются атерогенными? Формула холестерина. Липопротеины различаются и по участию в атерогенезе. Атерогенность липопротеинов частично зависит от размера частиц. Самые мелкие липопротеины, такие как ЛПВП, легко проникают в стенку сосуда, но также легко ее покидают, не вызывая атеросклероз. Богатые триглицеридами частицы – хиломикроны и крупные ЛПОНП, как полагают, не атерогенны, но их избыток может вызвать острый панкреатит. Что касается остатков липолиза богатых триглицеридами липопротеинов –липопротеинов промежуточной плотности, то они считаются атерогенными. ЛПНП, липопротеины промежуточной плотности и мелкие ЛПОНП достаточно малы, чтобы проникать в стенку сосуда, и в случае химической модификации (вследствие окисления) легко задерживаются в сосудистой стенке. ЛПОНП - образуются в печени, являются транспортной формой эндогенных ТАГ. Как и хиломикроны, являются субстратами липопротеинлипазы эндотелия капилляров. После гидролиза ТАГ, ЛПОНП превращаются в ЛПНП. ЛПНП - образуются в крови из ЛПОНП под действием липопротеинлипазы. Богаты холестеролом, транспортируют его во внепечёночные ткани. В результате взаимодействия ЛПНП с рецепторами на поверхности мембран холестерол из ЛПНП проникает внутрь клеток, где участвует в образовании клеточных структур и реакциях биосинтеза веществ (см.14.4.1). ЛПВП – образуются в печени, первоначально состоят преимущественно из белков и фосфолипидов и имеют форму дисков. При помощи фермента ЛХАТ липопротеины этого класса извлекают избыток холестерола из внепечёночных клеток и в форме эфиров доставляют его в печень. Увеличение содержания в крови ЛПНП и ЛПОНП и уменьшение содержания ЛПВП способствует развитию атеросклероза. Следовательно, ЛПОНП и ЛПНП –атерогенные липопротеины, ЛПВП –антиатерогенные липопротеины. Билет 11 = 26 2. В каком виде свободные жирные кислоты переносятся с током крови? Схема путей их утилизации в тканях. Жирные кислоты – алифатические карбоновые кислоты – в организме могут находиться в свободном состоянии (следовые количества в клетках и тканях) либо выполнять роль строительных блоков для большинства классов липидов. Местом депонирования жирных кислот является жировая ткань (адипоциты) в составе триглицеридов (этерифицированные жирные кислоты). Утилизация происходит в мышцах и печени, куда они транспортируются в форме свободных (неэтерифицированных) жирных кислот при помощи переносчика (альбумина). В печени большая часть НЭЖК подвергается реэтерификации (связыванию) с образованием триглицеридов и фосфолипидов. Свободные жирные кислоты, и особенно, олеиновая, пальмитиновая, линолевая накапливаются в жировой ткани в виде триглицеридов. Свободные жирные кислоты встречаются в очень небольшом количестве. В основном они находятся в составе других липидов. При этом они связаны с другими компонентами липидов сложноэфирной связью (эстерифицированы). 3. Напишите формулу арахидоновой кислоты. Представьте схему образования из нее биологически активных веществ. Назовите их, какие функции они выполняют. Арахидоновая кислота содержит 20 углеродных атомов и 4 двойные связи. В естественных условиях молекула арахидоновой кислоты имеет конфигурацию шпильки. 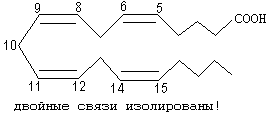 Арахидоновая кислота является субстратом для оксигеназ (ферменты, включающие кислород в состав субстрата). 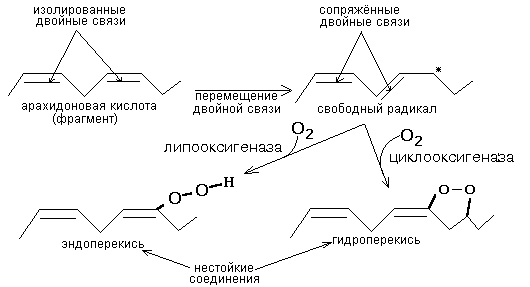 Перекисное окисление арахидоновой кислоты заключается в присоединении кислорода и образовании перекиси. Под действием активных форм кислорода происходит перемещение двойной связи и включение молекулы кислорода в молекулу арахидоновой кислоты. Перекисное окисление арахидоновой кислоты заключается в присоединении кислорода и образовании перекиси. Под действием активных форм кислорода происходит перемещение двойной связи и включение молекулы кислорода в молекулу арахидоновой кислоты.Перекиси – нестойкие быстро разрушающиеся вещества. В липиде появляются "ОН"-группы или кетогруппы. В тканях человека и животных имеются два фермента перекисного окисления: ЦИКЛООКСИГЕНАЗА и ЛИПООКСИГЕНАЗА. При окислении с участием циклооксигеназы одновременно с окислением происходит циклизация, при действии липооксигеназы окисление идет без циклизации. Продукт действия циклооксигеназы: гидроперекись простагландин G2 (ПГG2). Затем он преобразуется в другую гидроперекись - ПГН2. Далее в результате действия других окислительных ферментов из ПГН2 образуются другие простагландины. Из ПГН2 образуется ещё 2 тромбоксана (Тх). ПГ и Тх называются "ГОРМОНЫ МЕСТНОГО ДЕЙСТВИЯ". Регулирующий эффект оказывают там же, где образуются. Простагландины - влияют на проницаемость клеточных мембран. В частности, изменяют проницаемость кровеносных сосудов, влияют на тонус гладкомышечных клеток, на процессы реабсорбции в почках. Некоторые ПГ вызывают сокращение, а некоторые - расслабление мышечных элементов. 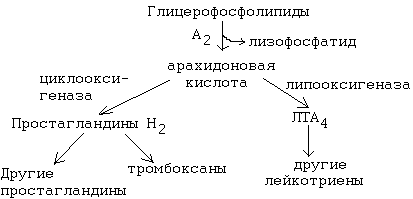 Тромбоксаны - регулируют функции тромбоцитов. Стимулируют агрегацию тромбоцитов. Тромбоксаны - регулируют функции тромбоцитов. Стимулируют агрегацию тромбоцитов.В результате действия липооксигеназы образуется лейкотриен А4 (ЛТА4). Это предшественник других лейкотриенов. Лейкотриены - продуцируются лейкоцитами и регулируют функции лейкоцитов. В частности, вызывают хемотаксис гранулоцитов, стимулируют фагоцитоз. Способны влиять на клеточную проницаемость и на тонус гладких мышц. При различных аллергических заболеваниях (например, при бронхиальной астме) важную роль играет не только выделение гистамина, но и лейкотриенов. Лейкотриены обладают очень длительным воздействием на клетку. 5. Какие нарушения липидного обмена наблюдаются при сахарном диабете? Сахарный диабет — заболевание, при котором наблюдается абсолютный или относительный дефицит инсулина. Нехватка этого пептидного гормона отражается главным образом на обмене углеводов и липидов 1.При сахарном диабете на липидный обмен влияет Инсулин в жировой ткани: он стимулирует синтез жирных кислот из глюкозы, что связано с активацией ацетил-КоА-карбоксилазы, и усиливает генерацию НАДФН + Н+ в ГМП . также инсулин тормозит расщепления жиров и деградации белков в мышцах. Таким образом, недостаточность инсулина ведет к глубоким нарушениям промежуточного метаболизма, что и наблюдается у больных сахарным диабетом. 2.Также при сахарном диабете наблюдается постоянное сильнейшее углеводное голодание, из-за плохого проникновения глюкозы в клетки. Наблюдается активация липолиза и повышается образование кетоновых тел. При тяжелых формах сахарного диабета концентрация кетоновых тел в крови может быть еще выше, и достигать опасных для жизни значений: до 20 ммоль/л и более. Билет 12 = 27 1. Написать реакции распада глицерина до ПВК. Сколько молекул АТФ может образоваться при распаде глицерола до СО2 и Н2О? Процесс окисления глицерина до СО2 и Н2О можно разбить на несколько этапов: 1.Превращение глицерина в 3-фосфоглицериновый альдегид. На этом этапе затрачивается АТФ на фосфорилирование глицерина. Далее фосфоглицерин окисляется фосфоглицеролдегидрогеназой, коферментом которой служит НАД, до фосфодиоксиацетона. Сопряженно с процессом окисления образуется 3 моль АТФ. Фосфодиоксиацетон изомеризуется в 3-фосфоглицериновый альдегид. 2.В превращении 3-фосфоглицериновый альдегид → пировиноградная кислота образуется 10 моль АТФ (см. второй этап гликолиза в аэробных условиях). 3.Окислительное декарбоксилирование ПВК - 3 моль АТФ. 4.Цикл Кребса - 12 моль АТФ. В сумме энергетические эффекты отдельных этапов превращения глицерина составляют 22 моль АТФ. 4. Схема путей утилизации глицерина в тканях. 5. Как происходит переваривание и всасывание жира в организме? Химическое название жиров - ацилглицерины, то есть жиры. Это сложные эфиры глицерина и высших жирных кислот. "Ацил-" - это означает "остаток жирных кислот. В зависимости от количества ацильных радикалов жиры разделяются на моно-, ди- и триглицериды. Если в составе молекулы 2 радикала жирных кислот, то жир называется ДИАЦИЛГЛИЦЕРИНОМ. Если в составе молекулы 1 радикал жирных кислот, то жир называется МОНОАЦИЛГЛИЦЕРИНОМ. В организме человека и животных преобладают ТРИАЦИЛГЛИЦЕРИНЫ (содержат три радикала жирных кислот). Источники жира в организме: 1. Пищевой жир (экзогенный) 2. Эндогенный жир, синтезируется в печени из углеводов. Переваривание экзогенного жира обязательно требует предварительного эмульгирования. Некоторые пищевые жиры поступают в организм уже в эмульгированной форме, например молочный жир. Для остальных необходимо эмульгирование с помощью специальных веществ - эмульгаторов (детергентов). Эмульгаторы – вещества амфифильной природы. Они снижают поверхностное натяжение и стабилизируют эмульсию. В организме человека эмульгаторами являются желчные кислоты. Это вещества стероидной природы. Синтезируются в печени из холестерина путем окисления по монооксигеназному типу в две первичные желчные кислоты: холевую и хенодезоксихолевую, которые затем связываются с аминокислотными остатками глицина и таурина. Собственно переваривание жиров – это гидролиз сложноэфирных связей. Существует три фермента: 1.Язычная липаза - Вырабатывается клетками слизистой оболочки задней части языка. Действие проявляется только в желудке, может переваривать уже эмульгированный жир. Ее pH-оптимум – 4-5. Поэтому в желудке взрослого человека язычная липаза неактивна. Реально жиры перевариваются язычной липазой только у младенцев. У взрослых людей переваривание жира идет только в кишечнике по схеме: «выделение желчи эмульгирование жира действие панкреатической липазы». 2.Панкреатическая липаза - фермент обладает очень низкой активностью. Но в поджелудочной железе вырабатывается белок, который, попадая в кишечник, способен активировать панкреатическую липазу это – «колипаза», она вырабатывается в виде неактивного предшественника – проколипазы, который активируется трипсином в кишечнике. Колипаза не является классическим активатором, она лишь связывает субстрат и приближает его к активному центру липазы. Образовавшиеся жирные кислоты и моноацилглицерины могут всасываться в кишечную стенку. 3. Эстераза липидов. Под действием этого фермента часть моноацилглицеринов может подвергаться гидролизу с образованием глицерина и жирных кислот. Всасываются продукты переваривания путем предварительного образования смешанных мицелл с желчными кислотами. Мицеллы попадают в энтероциты. Там из компонентов мицелл снова образуются триацилглицерины, а желчные кислоты по системе воротной вены возвращаются в печень, и могут снова поступать в желчь. Этот процесс называется рециркуляцией желчных кислот. Билет 13= 28 5. Каким производным холестерола присуща высокая биологическая активность? Синтез холестерина - протекает в основном в печени на мембранах эндоплазматического ретикулума гепатоцитов. Этот холестерин - эндогенный. Происходит постоянный транспорт холестерина из печени в ткани. Для построения мембран используется также пищевой (экзогенный) холестерин. Ключевой фермент биосинтеза холестерина - ГМГ-редуктаза (бета-гидрокси, бета-метил, глутарил-КоА редуктаза). Этот фермент ингибируется по принципу отрицательной обратной связи конечным продуктом - холестерином. Продукты холестерина, их роль, механизмы: Стероиды -группа физиологически активных в-в стероидной природы. Образуются стероидны в органах производящих гормоны(надпочечники,яичники,семенники и др.) Роль: регуляция беременности (гестагены), углеводного (глюкокортикоиды) и водно-солевого (минералокортикоиды) обмена, сперматогенеза (андро-гены) и овуляции (эстрогены) Механизм реакций: Биосинтез стероидных гормонов в организме происходит в органах, производящих гормоны (надпочечники, яичники, семенники и др.), откуда разносятся током крови к клеткам органов-мишеней, где вступают во взаимодействие со специфическими белковыми рецепторами, расположенными либо на клеточной мембране, либо в цитоплазме. Стероидные гормоны обратимо связываются с рецепторами за счет водородных связей и гидрофобных взаимодействий, образуя стероид-рецепторные комплексы, которые передают гормональный сигнал, либо оставаясь на месте (мембранные рецепторы), либо проникая в ядро клетки и вступая там во взаимодействие с генами. Эффективность гормонального сигнала определяется законом действующих масс, специфичностью и энергетикой стероид-рецепторного взаимодействия. Помимо прямого действия стероидные гормоны могут препятствовать действию др. гормонов, блокируя взаимодействие др.гормонов с их рецепторами. Таким образом, стероидные гормоны вследствие биотрансформации и мультифункциональности образуют в организме широкую сеть (или древо), каскадно исходящую из холестерина и регулирующую многочисленные стороны гомеостаза и адаптации. Билет 14 = 29 3. Роль и механизм десатуразных реакций. В состав клеточных мембран входят жирные кислоты и белки. «Разжижают» мембрану специальные ферменты — десатуразы. В цепях жирных кислот они образуют дополнительные двойные связи. Чем больше таких связей, тем выше текучесть мембраны. Включение двойных связей в радикалы ЖК называется десатурацией. Десатурация ЖК происходит в ЭПР в монооксигеназных реакциях, катализируемых десатуразами. Стеароил-КоА-десатураза – интегральный фермент, содержит негеминовое железо. Катализирует образование 1 двойной связи между 9 и 10 атомами углерода в ЖК. Стеароил-КоА-десатураза переносит электроны с цитохрома b5на 1 атом кислород, при участии протонов этот кислород образует воду. Второй атом кислорода включается стеариновую кислоту с образованием её оксиацила, который дегидрируется до олеиновой кислоты. 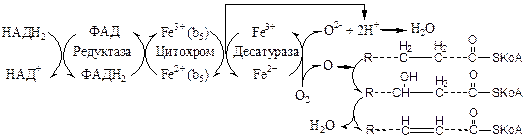 Десатуразы ЖК, имеющиеся в организме человека, не могут образовывать двойные связи в ЖК дистальнее девятого атома углерода, поэтому ЖК семейства ω-3 и ω-6 не синтезируются в организме, являются незаменимыми и обязательно должны поступать с пищей, так как выполняют важные регуляторные функции. Основные ЖК, образующиеся в организме человека в результате десатурации — пальмитоолеиновая и олеиновая. 4. Строение и роль желчных кислот. Желчь представляет собой сложную жидкость со щелочной реакцией. В ней выделяют сухой остаток - около 3% и воду - 97%. В сухом остатке обнаруживается две группы веществ: - попавшие сюда путем фильтрации из крови натрий, калий, бикарбонат-ионы, креатинин, холестерол (ХС), фосфатидилхолин (ФХ), - активно секретируемые гепатоцитами билирубин и желчные кислоты. В норме между основными компонентами желчи выдерживается соотношение Желчные кислоты : ФХ : ХС равное 65:12:5. Без желчи липиды не перевариваются. В сутки образуется около 10 мл желчи на кг массы тела, таким образом, у взрослого человека это составляет 500-700 мл. Желчеобразование идет непрерывно, хотя интенсивность на протяжении суток резко колеблется. Роль желчных кислот:1. Наряду с панкреатическим сокомнейтрализация кислого химуса, поступающего из желудка. При этом карбонаты взаимодействуют с НСl, выделяется углекислый газ и происходит разрыхление химуса, что облегчает переваривание. 2. Усиливает перистальтику кишечника. 3. Обеспечивает переваривание жиров: - эмульгирование для последующего воздействия липазой, необходима комбинация [желчные кислоты+жирные кислоты+моноацилглицеролы], - уменьшает поверхностное натяжение, что препятствует сливанию капель жира, - образование мицелл, способных всасываться. 4. Экскреция избытка ХС, желчных пигментов, креатинина, металлов Zn, Cu, Hg, лекарств. Для холестерина желчь - единственный путь выведения, с ней может выводиться 1-2 г/сут. Строение желчных кислот: 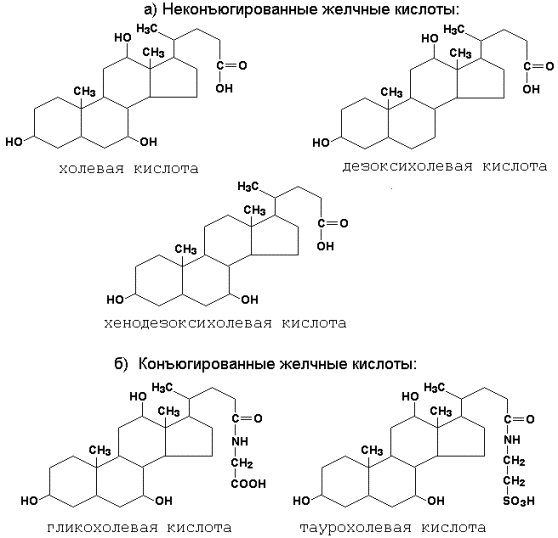 Билет 15 = 30 2. Назовите продукты липолиза. В каком виде осуществляется их транспорт из жировых депо в ткани? Составте схемы их утилизации в тканях. Продукты липолиза - глицерин и жирные кислоты выходят из жировой клетки, попадают в кровь и поступают в клетки других тканей. Глицерин как вещество гидрофильное растворяется в плазме крови. Жирные кислоты - гидрофобные вещества. Поэтому для транспорта в кровяном русле для них необходимы переносчики. Транспорт жирных кислот обеспечивают белки плазмы крови альбумины, образующие с ними комплексы. Такие комплексы образуются путем формирования слабых типов связей: гидрофобного взаимодействия радикалов жирных кислот и ионных связей СООН-групп жирных кислот с радикалами лизина молекулы альбумина. Следовательно, жирные кислоты в составе комплекса являются химически свободными. Жирные кислоты, находящиеся в комплексе с альбуминами, обозначаются термином НЕЭСТЕРИФИЦИРОВАННЫЕ ЖИРНЫЕ КИСЛОТЫ (НЭЖК). Уровень НЭЖК в крови – показатель степени мобилизации жира: чем больше в плазме крови НЭЖК, тем интенсивнее идет липолиз. Липолиз происходит в ходе мышечной работы и при голодании, что сопоровождается повышением концентрации НЭЖК в крови. Глицерин и жирные кислоты в этой ситуации выступают как источники энергии. Утилизации в тканях ЖК: -β-окисление - специфический путь катаболизма ЖК, в результате которого образуется Ацетил-КоА -липогенез – процесс образования ЖК -ФЛ( входит в состав) -ГЛ (входит в состав) Утилизации в тканях активной формулы глицерина: -Глюконеогенез( синтез глюкозы из продуктов неуглеводного обмена) – в печени, почках, слизичтой кишечника -Синтез глицерофосфолипидов - Липогенез - СО2 + Н2О + 2АТФ ( ГБФ путь) |
