Физика. Задачи. 1. Определите сколько А1(ОН) 3 выделилось из 100 кг щелоч ноалюминатного раствора, содержащего 9,4 масс. Na
 Скачать 22.89 Kb. Скачать 22.89 Kb.
|
|
1. Определите сколько А1(ОН)3 выделилось из 100 кг щелоч- но-алюминатного раствора, содержащего 9,4 % масс. Na2O при к= 1,66 , если каустический модуль системы стал равным: а) 3,56; б) 8,16. 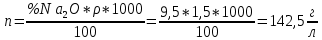 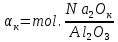 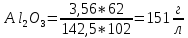 При растворении гидроокиси алюминия в щелочах образуются соли метаалюминиевой кислоты, которые носят название алюминатов, например Аl(ОН)3 + NaOH = NaAlO2 + 2Н2О. Алюминаты образуются также при нагревании смеси окиси или гидроокиси алюминия с соединениями щелочных или щелочноземельных металлов до температуры 800 °С и выше, например Al2O3 + Na2CO3 = 2NaA1О2 + CO2. Согласно реакции необходимо в два раза больше Al(OH)3 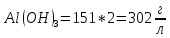 2. Рассчитать объем оборотной воды на разбавление 1 м3 пульпы после выщелачивания боксита, если концентрация глинозёма в жидкой фазе снизи- лась с 304 г/л до 165 г/л. Концентрация глинозёма в оборотной воде равна 40 г/л. Плотность твердой фазы равна 3080 кг/м3, содержание твердой фазы 300 г/л. 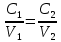 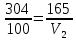 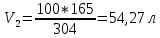 3. Определить теоретический и практический выходы глинозема при переработке боксита следующего состава (% масс.): Al2O3 – 52,3; SiO2 - 3,8; CaO - 3,1. CaO связывается в следующее нерастворимое соединение: 3CaO· Al2O3·6Ha2O 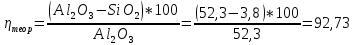 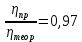 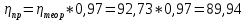 4. В алюминатном растворе, поступающем на выкручивание, содер- жится 1923,7 кг Al2O3; 904,5 кг Al2O3 остается в оборотном растворе; 11,5 кг - теряется. Остальное переходит в Al(OH)3. Определить выход глинозема и об- щий вес выделившегося в осадок гидроксида. 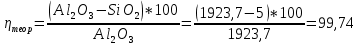 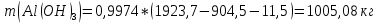  |
