Биотехнология. 1. Предмет и задачи биотехнологии. Основные этапы развития биотехнологии и биоиндустрии
 Скачать 0.65 Mb. Скачать 0.65 Mb.
|
|
1. Предмет и задачи биотехнологии. Основные этапы развития биотехнологии и биоиндустрии. Биотехнология - дисциплина, изучающая возможности использования живых организмов, их систем или продуктов их жизнедеятельности для решения технологических задач, а также возможности создания живых организмов с необходимыми свойствами методом генной инженерии. Задачи Биотехнологии: 1) создание новых ЛП и БАВ 2) создание микробиологических средств защиты растений, удобрений, а также создание новых гибридов методом генетич. и клет. инженерии. 4) технологии получения ценных продуктов для пищевой хим. и др. промышленности 5) технологии переработки отходов. Предмет: использование живых систем и их компонентов для создания и производства новых продуктов. Основные этапы развития биотехнологии и биоиндустрии: Первый этап – это развитие биотехнологии в разрезе исторического аспекта. При раскопках древних поселений в Месопотамии, в Египте, а также Греции были обнаружены остатки больших и малых пекарен и пивоварен. Известно, что уже шумеры умели делать пиво. На территории Древней Греции и Римской империи было активно развито виноделие и производство сыра. В конце 19 века развитие биотехнологии вступило во второй этап, она начала развиваться, как наука. Появились первые ученые генетики, микробиологи и вирусологи. В начале 20 века были созданы первичные установки по производству метана. Отходы сельскохозяйственного производства превращались в биологический газ и органическое удобрение. В середине 20 века начали производить антибиотики. В конце 20 века развилась генная и клеточная инженерия, что ознаменовало третий этап развития биотехнологии. 1972-ой год создание первой гибридной ДНК, в которую встроили чужеродные гены. 2. Общая схема технологического процесса. Характеристика и подготовка биообъектов в биотехнологии. Технологическая схема БТ процесса: Вспомогательные работы • ВР-1. Подготовка биообъекта микроуровня • ВР-2. Подготовка и стерилизация оборудования и коммуникаций • ВР-3. Подготовка и стерилизация питательной среды • ВР-4. Подготовка и стерилизация газового потока Основной технологический процесс • ТП-5. Стадия культивирования биообъекта • ТП-6. Выделение целевого продукта • ТП-7. Концентрирование/обезвоживание целевого продукта • ТП-8. Анализ целевого продукта Заключительные стадии • УМО-9. Фасовка, упаковка, маркировка лекарственной субстанции • ПО-10. Переработка отходов Биообъект - продуцент, синтезирующий нужный продукт 1) Клетки: микроорганизмов, животных, растений 2) Животные и растения (трансгенные) 3) Отдельные ферменты 4) Многокомпонентные ферментные системы Требования к биообъектам 1. Безвредность (GRAS –микроорганизмы считаются безопасными и приняты мировым сообществом). 2. Высокая скорость роста биомассы и синтеза целевого продукта 3. Направленная биосинтетическая активность при минимальных побочных продуктах. 4. Генетические однородность и стабильность в отношении к субстратам и условиям. 5. Отсутствие токсических веществ в целевом продукте. 6. Устойчивость к посторонней микрофлоре. 7. Способность расти на дешевых и доступных субстратах. Получение микроорганизмов для БТ 1) Классический подход - выделение нужного микроорганизма из природных условий: отбор проб материала посев в селективную среду выделение чистой культуры дифференциально диагностическое изучение изолированного микроорганизма определение его продукционной способности. 2) Выбор нужного вида из имеющихся коллекций хорошо изученных и охарактеризованных микроорганизмов 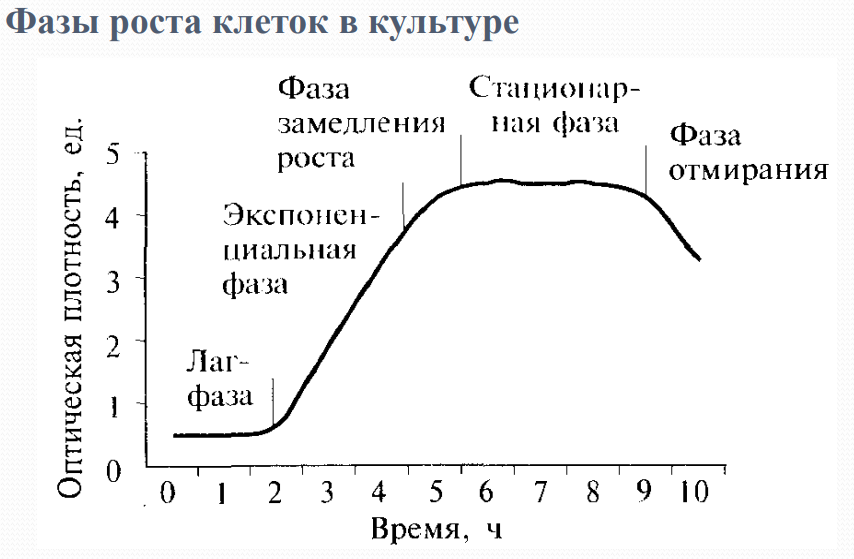 Лаг-фаза (адаптация клеток к новым условиям среды): синтез ферментов для переваривания субстрата, подготовка к клеточному делению. Экспоненциальная фаза (активное деление): синтез первичных метаболитов, которые нужны для роста и размножения микробов (аминокислоты, белки, нуклеиновые кислоты, витамины). Фаза замедления (исчерпание запасов питательной среды): исчерпание свободного места, накопление метаболитов, снижение клеточного деления, повышение синтеза вторичных метаболитов (не нужны для роста и размножения, но синтезируются в ответ на неблагоприятные условия: антибиотики, алкалоиды). Стационарная фаза (количество образованных равно количеству погибших микроорганизмов). Фаза отмирания (исчерпан запас питательных веществ, гибель). 3. Подготовительные операции в биотехнологическом процессе – подготовка и стерилизация оборудования, технологического воздуха и питательных сред. ВР-2. Подготовка и стерилизация оборудования и коммуникаций • Перед началом стерилизации оценивают степень герметичности оборудования и коммуникаций. • При выборе режима стерилизации особое внимание обращают на наличие в системе так называемых «слабых» точек (труднодоступные места). • Наиболее часто для стерилизации оборудования используется термический метод: обработка горячим паром при температуре 120-1400С, избыточным давлением 0,6 Мпа и в течении 4ч. Самоавтоклавирование – это очистка биореактора. ВР-3. Изготовление и стерилизация питательной среды • ВР-3.1. Выбор и реализация рецептуры питательной среды. • ВР-3.2. Растворение компонентов пит.среды. • ВР-3.3. Стерилизация питательной среды. • ВР-3.4. Охлаждение пит.среды до оптимальной температуры перед подачей и ферментатор. Питательная среда для культивирования должна обеспечивать: 1) жизнедеятельность микроорганизма, его рост и размножение; 2) эффективный синтез целевого продукта. Сложные питательные среды имеют непостоянный состав и включают биогенные добавки: мясной экстракт (бактерии) сыворотка крови (животные клетки) кукурузную муку морские водоросли Синтетические среды – среды, приготовленные из чистых химических соединений в заранее определенных соотношениях (выращивание стволовых клеток). Обычно для стерилизации питательных сред используют термический метод с применением насыщенного водяного пара повышенного давления. Процесс стерилизации длится от 2-20 мин. при температуре 120-140 С. Для обеспечения контроля за ходом стерилизации используют споры тест-микроорганизмов Bacillus stearothermophilus, которые помещают в автоклав (изменяют цвет при достижении нужной температуры). ВР-4. Подготовка и стерилизация технологического воздуха Технический воздухает поступает через систему аэрации и подвергается стерилизации (нагревание, облучение УФ, обработка ультразвуком, фильтрация). Чаще всего используют фильтрацию через волокнистые и пористые материалы: 1) Предварительная фильтрация – через стекловолокно, губчатый пенополиуретан, сетчатый винилпласт и т.д. 2) Тонкая очистка - фильтрующие материалы в виде картона, бумаги, мембран с диаметром волокон 0,4-1,5 мкм. 4. Культивирование биообъектов – типы биореакторов и процессов культивирования в биотехнологическом производстве. ТП-5. Культивирование биообъекта Культивирование биообъекта осуществляется в биореакторе и включает следующие операции: • ТП-5.1. Внесение питательной среды. • ТП-5.2. Подача газового потока. • ТП-5.3. Внесение биообъекта. • ТП-5.4. Рост биообъекта. • ТП-5.5. Внесение предшественников целевого продукта. • ТП-5.6. Биосинтез или биотрансформация. Современный биореактор должен обладать системами: 1) Система эффективного перемешивания пит.сред (для равномерного распределения среды) 2) Система аэрации 3) Система теплообмена 4) Система пеногашения 5) Система контроля и регулировки процесса Виды биореакторов: 1) Аппарат с мешалкой (интенсивное перемешивание среды, лопасти часто ломаются, клетки погибают) 2) Эрлифтный и Циркуляционный аппараты (насос обеспечивает ток среды и аэрацию) 4) Колонный аппарат (стерилизации газового потока, отсутствие застойных зон). Барботажная колонка (воздух циркулирует снизу вверх, интенсивная аэрация, но повышенное пенообразование и наличие застойных зон) Биотехнологические процессы: - Анаэробные процессы - Аэробные процессы: 1)Твердофазные процессы: • поверхностные - слой субстрата не превышает 3–7 см • глубинные процессы, идущие в не перемешиваемом слое • глубинные перемешиваемые процессы (кусочки субстрата с микробами, взвешенные в жидкости) 2) Газофазные - в аппаратах с твердым наполнителем, через которые пропускают газа 3) Жидкофазные – в жидких питательных средах (наиболее популярный) Культивирование: 1) Непрерывное (с подпиткой и выведение среды) – получение первичных метаболитов. 2) Полунепрерывное (отливаем и доливаем среду) 3) Периодическое (диализ, следим за фазой роста) – получение вторичных метаболитов. 4) Одностадийное - непрерывное культивирование в одном биореакторе. 5) Многостадийное – используем несколько культур и биореакторов 5. Внутриклеточные и внеклеточные метаболиты. Методы выделения и очистки целевых продуктов. ТП-6. Выделение целевого продукта ТП-6.1. Обработка культуры клеток ТП-6.2. Отделение биомассы от культуральной жидкости методами седиментации, флотации, фильтрования, центрифугирования. ТП 6.3. Разрушение клеток физическими, химическими и химико-ферментативными методами. ТП-6.4. Отделение экстракта от разрушенных клеток ТП-6.5. Выделение целевого продукта Методы грубого разделения (фракционирования): 1) Осаждение белков в изоэлектрической точке (белки выпадают в осадок из-за нейтрализации заряда). 2) Высаливание (путем добавления раствора солей щелочных и щелочноземельных металлов) из-за различной растворимости белков в концентрированных растворах. 3) Электрофорез (различное движение заряженных молекул с разной молекулярной массой) 4) Диализ (белки не проходят полупроницаемую мембрану в отличие от низкомолекулярных веществ) 5) Кристаллизация (создание пересыщенного раствора и резкое охлаждение для снижения растворимости, что приводит к росту кристаллов из чистых веществ) 6) Фильтрация с использованием специализированных мембран Хроматографические методы: 1) ВЭЖХ 2) Газовая хроматография 6. Совершенствование биообъектов методами мутагенеза и селекции. Виды мутаций, применяемые мутагены. Этот метод в наше время реже используется. Недостатки: мало предсказуем, длительно по времени, реверсия (возвращение к исходному генотипу и фенотипу у бактерий). Мутагенез – это метод получения продуцента с мутациями в геноме, которые отличаются в сторону увеличения биотехнологических свойств (увеличение синтеза целевого продукта). Мутации возникают спонтанно и обычно связаны с ошибкой в репликации ДНК и системы репарации не всегда помогают. У микробов такие мутации накапливаются в популяции, что приводит к развитию новых штаммов.   Миссенс-мутации (нарушение расположения 1 нуклеотида, которая приводит к синтезу некорректной аминокислоты в белке): обуславливает развитие заболеваний (БА), снижает активность ферментов, снижает вероятность ретроингибирования за счет мутации в аллостерическом центре. Нонсенс-мутации (замена 1 нуклеотида, которая приводит к синтезу стоп-кодона, что приведет к обрыву синтеза белка и изменению активности этого белка). Индуцированный мутагенез – это увеличение встречаемости признаков с очень высокой или наоборот очень низкой степенью выраженности по действием мутагенов (не селективное действие) 1. Химические мутагены: а) нитрозогуанидин б) нитрозометилмочевина в) акридиновые красители г) некоторые противоопухолевые антибиотики, которые являются ДНКтропными агентами. 2.Физические мутагены: а) УФ- облучение б) рентгеновское облучение в) ультразвук г) альфа-, бета-, гамма- излучения д) высокая температура 7. Создание новых биообъектов методами клеточной инженерии. Клеточная инженерия – это техника обмена фрагментами ДНК, участками хромосом у прокариот и любыми хромосомами у эукариот, независимо от удаленности организмов в эволюционном плане. Техника клеточной инженерии основана на получении протопластов (протопластирование). Протопласт – это клетка без клеточной стенки, окруженная цитоплазматической мембраной. Этапы генной инженерии: 1) Выбор биообъектов: Объект 1 с одними полезными свойствами + Объект 2 с другими полезными свойствами Например: бактерия, синтезирующая а/б + E.coli (хорошо растет) 2) Обработка клеточных клеток с помощью ферментов: Лизоцим действует на бактерии Улиточный фермент на грибы Целлюлаза и пектиназа на растения 3) Стабилизация протопласта (20% маннит или 10% натрия хлорид) Все следующие стадии проводят в гипертоническом растворе 4) Слияние протопластов (среда с полиэтиленгликолем): Кроме ПЭГ можно заранее протопласты сделать комплементарными (заморозка и оттаивание, обработка ферментами) 5) Восстановление клеточной стенки: гибрид засевают на плотную среду у бактерий образуются гаплоиды со смешанными генами 19. Экологические аспекты биотехнологии – утилизация твердых, жидких и газообразные отходов биотехнологического производства. Твердые отходы (к ним относят биомассу продуцента после отделения целевого продукта): Нужно учитывать, что они образуются в предприятиях в большом объеме и содержат остатки целевого продукта. Ликвидация путем переработки биомассы: перемешиванием с почвой и закапывание в ямы с бетонными подложками. Такую яму оставляют закрытой на несколько лет и за это время почвенные микроорганизмы расщепляют биомассу. А бетонная подложка защищает от попадания неразложившихся веществ в грунтовые воды. Попытки малоотходного производства: 1) Из мицелия актиномицет извлекают суммарную липидную фракцию и используют в качестве пеногасителя в следующем производственном цикле тетрациклинов. 2) Простерилизованную и перемолотую биомассу используют как добавку в корм скоту. 3) Добавляют в состав строительных материалов (керамзит, кирпич). Жидкие отходы (к ним относят сточная жидкость, т.е. это культуральная жидкость после отделения от нее биомассы продуцента и целевого продукта): В состав почти всех схем очистки входит очистка микроорганизмами. 1) Жидкость попадает в железобетонный отстойник, а снизу происходит удаление осадка с загрязнениями. 2) Далее происходит насыщение жидкости кислородом (способствует интенсивному протеканию окислительных процессов). 3) Жидкость проходит через активный ил (сообщество микроорганизмов, окисляющих органические вещества) и обычно в его состав входят микроорганизмы рода Pseudomonas, Bacterium, Bacillus и т.д. 4) Потом жидкость поступает в аэротенк для прохождения через биофильтры (пленки с микроорганизмами-деструкторами с наибольшей окислительной способностью, обычно получаемые методом генной инженерии) Газообразные отходы: Удаление органических неприятно пахнущих веществ проводят биологическими методами дезодорации, основанными на использовании микроорганизмов-деструкторов для очистки газов. В основе этого процесса лежит способность многих микробов окислять спирты, альдегиды, эфиры, азот и серосодержащие соединения. Обычно используют биоустановки, содержащие полимерный пористый материал с биопленкой на поверхности. При прохождении воздуха через установку микробы будут улавливать летучие вещества и расщеплять их. Ещё один метод очистки – это физический (термический метод) |
