ЭХО. 1. Разновидности электрохимической обработки Механизм процесса анодного растворения металла
 Скачать 3.87 Mb. Скачать 3.87 Mb.
|
|
Содержание Введение 1. Разновидности электрохимической обработки 2. Механизм процесса анодного растворения металла 3. Виды электрохимической обработки 4. Физико-химическая сущность метода 5. Методы размерной электрохимической обработки 5.1 Обработка с неподвижными электродами 5.2 Прошивание полостей и отверстий 5.2.1 Получение отверстий струйным методом 5.3 Точение наружных и внутренних поверхностей 5.4 Протягивание наружных и внутренних поверхностей в заготовках 5.5 Разрезание заготовок 5.6 Шлифование 6. Законы Фарадея и скорость электрохимического процесса 7. Электрохимический станок Заключение Библиографический список Введение В современном машиностроении возникают технологические проблемы, связанные с обработкой новых материалов и сплавов (например, жаро- и кислотостойкие, специальные никелевые стали, тугоплавкие сплавы, композиты, неметаллические материалы: алмазы, рубины, германий, кремний, порошковые тугоплавкие материалы и т.п.) форму и состояние поверхностного слоя которых трудно получить известными механическими методами. К таким проблемам относится обработка весьма прочных или весьма вязких материалов, хрупких и неметаллических материалов (керамика), тонкостенных нежестких деталей, а также пазов и отверстий, имеющих размеры в несколько МКМ; получение поверхностей деталей с малой шероховатостью, и очень малой толщиной дефектного поверхностного слоя. В этих условиях, когда возможность обработки резанием ограничены плохой обрабатываемостью материала изделия, сложностью формы обрабатываемой поверхности или обработка вообще невозможна, целесообразно применять электрофизические и электрохимические методы обработки. Их достоинства следующие: ) механические нагрузки либо отсутствуют, либо настолько малы, что практически не влияют на суммарную погрешность точности обработки; ) позволяют изменять форму обрабатываемой поверхности заготовки (детали); ) позволяют влиять и даже изменять состояние поверхностного слоя детали; ) не образуется наклеп обработанной поверхности; ) дефектный слой не образуется; ) удаляются прижоги поверхности, полученные при шлифовании; ) повышаются: износостойкость, коррозионная стойкость, прочность и другие эксплуатационные характеристики поверхностей деталей. Кинематика формообразования поверхностей деталей электрофизическими и электрофизическими методами обработки, как правило, проста, что обеспечивает точное регулирование процессов и их автоматизацию. Цель работы: доказать преимущества, а в некоторых случаях незаменимость электрохимической размерной обработки. Понять механизм действия методов электрохимической обработки. 1. Разновидности электрохимической обработкиВ основе электрохимической обработки (ЭХО) металлов и сплавов лежит принцип анодного растворения обрабатываемой заготовки в растворе электролита. Для осуществления процесса необходимо иметь два электрода, из которых один - заготовка (анод), другой - инструмент (катод), электролит между ними, а также источник питания. Совокупность двух электродов (анода, катода) и электролита между ними называется электролитической ячейкой. Электрохимическая обработка в стационарном электролите, к ним относятся: ü очистка поверхностей металлов от окислов, ржавчины, жировых пленок и других загрязнений; ü заострение и затачивание режущего инструмента; ü электрополирование; ü гравирование и маркирование по металлам и др. Отличительные особенности: обработка осуществляется при низких плотностях тока (не более 2 А/см); обеспечиваются сравнительно небольшие скорости растворения (10 - 10 мм/мин); общий объем удаляемого материала невелик; в межэлектродном пространстве отсутствуют (или имеется лишь малое количество) нерастворенных продуктов процесса; межэлектродное расстояние достаточно велико и может составлять сотни миллиметров. 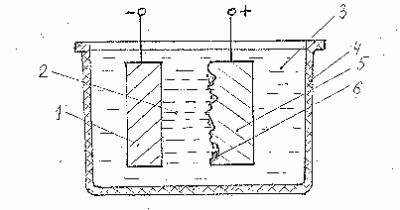 Рис. 1.1 Схема электролитического полирования (обработка в стационарном электролите): - катод, 2 - силовые линии тока, 3 - электролит, 4 - ванна, 5 - заготовка (анод), 6 - продукты растворения. 2. Механизм процесса анодного растворения металлаПротекание тока в электролитической ячейке осуществляется посредством движения ионов под действием приложенного внешнего электрического поля. Жидкие растворы, проводящие электрический ток за счет ионной проводимости, называются электролитами. В качестве электролитов используются водные растворы неорганических солей NaCl, NaNO3,Na2SO4 и др. реже кислот и щелочей. Удельная электропроводимость электролитов находится в пределах (0,1-0,4) см, а их температура в интервале (4-60) оС. При этом применяют так называемые сильные электролиты, в которых все молекулы растворенного вещества диссоциируют на анионы (Аn-) и катионы (Кn+). Например, водный раствор поваренной соли (NaCl) диссоциирует на Na+ (катион) иCl - (анион). Кроме этого сама вода содержит ион водорода Н+ и гидроксила (ОН) - . При отсутствии u1074 внешнего электрического поля (электроды разомкнуты) ионы движутся в электролите хаотически и электрического тока в нем не наблюдается. При этом на границе раздела твердой и жидкой фазы (металлического электрода и электролита) образуются два электрически заряженных слоя: поверхностный слой металла, заряженный положительно или отрицательно, и слой ионов, имеющий противоположный заряд. Между этими слоями устанавливается определенный потенциал, который называется равновесным (Φр). Этот потенциал измеряется относительно стандартного водородного электрода, потенциал которого при всех условиях принимается равным нулю. Подключение электродов ячейки к источнику напряжения сдвигает их потенциалы от равновесных: и вызывает протекание электродных процессов. На аноде происходит: ) основная реакция - растворение (окисление) металла с образованием гидрата окиси металла, выпадаемого в осадок при обработке в нейтральных и щелочных электролитах. (2.1) Ме - ne - > Men+; Men+ + n OH - >Me (OH) n где - валентность металла (Ме) или с образованием растворимой соли при обработке в кислотах (2.2) Men+ + n R - >Me (R) n ) возможна побочная реакция - образование кислорода, снижающая К.П.Д. процесса анодного растворения: (2.3) 2 OH - 2 e - > H2O +O; O+O->O2 На катоде происходит выделение водорода, процесс образования которого в зависимости от условий протекает по разному: а) в кислотах и при малых плотностях тока в нейтральных и слабо щелочных растворах восстановление водорода осуществляется по схеме: (2.4) H+ + e - > H; H+H->H2 б) в нейтральных растворах при больших плотностях тока и больших напряжениях на электродах образование молекулярного водорода может осуществляться за счет разложения молекул воды: (2.5) H2O + e - > H+ OH-; H+H->H2 Перечисленные уравнения отражают лишь конечный результат процесса анодного растворения, который представляет собой совокупность сложных взаимосвязанных процессов (диффузионных, миграции ионов, выделение тепла, гидродинамики электролита в зазоре, образование окисных пленок и др.). Характер электрохимических реакций и технологических показателей ЭХРО зависят от кислотности и щелочности электролита, который оценивают водородным показателем рН. При обработке значительного количества деталей в одном и том же электролите его рН повышается до 9-11, что ухудшает условия растворения металлов. Для сохранения постоянства шероховатости обработанной поверхности, скорости съема и энергоемкости процесса осуществляют стабилизацию рН электролита за счет буферирования раствора, например, борной кислотой в количестве 3-30 г/л. О характере протекания электродных процессов можно судить по поляризационным кривым, которые представляют собой зависимость между плотностью тока (i) и потенциалом на электроде (Φ), сравниваемым с потенциалом стандартного водородного электрода. 3. Виды электрохимической обработкиЭлектрохимическое объемное копирование - Электрохимическая обработка, при которой форма электрода-инструмента отображается в заготовке. Электрохимическое прошивание - Электрохимическая обработка, при которой электрод-инструмент, углубляясь в заготовку, образует отверстие постоянного сечения. Струйное электрохимическое прошивание - Электрохимическое прошивание с использованием сформированной струи электролита. Электрохимическое калибрование - Электрохимическая обработка поверхности с целью повышения ее точности. Электрохимическое точение - Электрохимическая обработка, при вращении заготовки и поступательном перемещении электрода-инструмента. Электрохимическая отрезка - Электрохимическая обработка, при которой заготовка разделывается на части. Электрохимическое удаление заусенцев (ЭХУЗ, Electrochemical debuting) - Электрохимическая обработка, при которой удаляются заусенцы заготовки. Электрохимическое маркирование Многоэлектродная электрохимическая обработка - Электрохимическая обработка осуществляемая электродами, подключенными к общему источнику питания электрическим током и находящимися во время обработки под одним потенциалом. Непрерывная электрохимическая обработка - Электрохимическая обработка при непрерывной подаче напряжения на электроды. Импульсная электрохимическая обработка - Электрохимическая обработка при периодической подаче напряжения на электроды. Циклическая электрохимическая обработка - Электрохимическая обработка, при которой один из электродов перемещается в соответствии с заданной циклограммой, а также другие смешанные виды электрофизикохимической обработки (ЭФХМО) включающие ЭХО: анодно-механическая обработка; - электрохимическая абразивная обработка; - электрохимическое шлифование; - электрохимическая доводка (ЭХД); - электрохимическое абразивное полирование; - электроэрозионнохимическая обработка (ЭЭХО); - электрохимическая ультразвуковая обработка и др. 4. Физико-химическая сущность методаМеханизм съема (растворения, удаления металла) при электрохимической обработке основан на процессе электролиза Особенностями электролиза являются пространственное окисление (растворение) анода и восстановление (осаждение) металла на поверхности катода. При ЭХО применяют такие электролиты, катионы которые не осаждаются при электролизе на поверхности катода. Этим обеспечивается основное достоинство ЭХО перед электроэрозионной обработкой Для стабилизации электродных процессов при ЭХО и удаления из межэлектродного промежутка (МЭЗ) продуктов растворения (шлама) применяют принудительную подачу в рабочую зону электролита, то есть прокачивают его с определенным давлением. 5. Методы размерной электрохимической обработки5.1 Обработка с неподвижными электродамиПо этой схеме получают местные облегчения в деталях, отверстия в листовых материалах, наносят информацию (порядковые номера, шифры изделий и др.), удаляют заусенцы. Требуемая форма углубления или отверстия получается за счет нанесения на заготовку 2 слоя диэлектрика 3. Электрод-инструмент 1 не перемещается к обрабатываемой поверхности - межэлектродный зазор по мере съема металла с заготовкой 2 возрастает, а скорость Схема обработки с неподвижными электродами:  Рисунок 1 1 - электрод - инструмент; - заготовка; - диэлектрик. 5.2 Прошивание полостей и отверстийПри такой схеме электрод-инструмент 1 имеет одно рабочее движение - поступательное движение со скоростью По этой схеме изготовляют рабочие полости ковочных штампов, пресс - форм, прошивают отверстия, пазы, перья лопаток турбин, вырезают заготовки различного профиля. [Схема прошивания полости показана на рисунке 2] Схема прошивания:  Рисунок 2 1 - электрод-инструмент; - заготовка. 5.2.1 Получение отверстий струйным методомЭлектрод-инструмент состоит из токопровода 1, омываемого потоком электролита. Токопровод находится внутри корпуса 3 из диэлектрика. Электролит создает токопроводящий канал между токопроводом 1 и заготовкой 2. [Схема прошивания струйным методом показана на рис] В месте контакта жидкости с обрабатываемой поверхностью материал заготовки растворяется и образуется углубление. Процесс идет достаточно быстро только при высоких напряжениях (до нескольких сотен вольт). Так получают отверстия диаметром 1,5…2,0 мм и вырезают контуры деталей сложной формы. Схема прошивания струйным методом:  Рисунок 2.1 1 - электрод-инструмент (токопровод); - заготовка; - диэлектрический корпус. 5.3 Точение наружных и внутренних поверхностейПо такой схеме электрод-инструмент 1 исполняет роль резца, без контакта. В зазор S прокачивается электролит со скоростью  Рисунок 3 Схема точения наружных поверхностей 1 - электрод-инструмент; - заготовка. При точении внутренней поверхности электрод-инструмент 1 перемещается вдоль заготовки 2 со скоростью Схема точения внутренних поверхностей:  Рисунок 3.1 1 - электрод - инструмент; - заготовка; - прокладки диэлектрические. 5.4 Протягивание наружных и внутренних поверхностей в заготовкахЗаготовки должны иметь предварительно обработанные поверхности, по которым можно базировать электрод-инструмент. Его устанавливают относительно заготовки с помощью диэлектрических прокладок. Электрод-инструмент продольно перемещается (иногда вращается). По такой схеме выполняют чистовую обработку цилиндрических отверстий, нарезание резьбы, шлицев, винтовых канавок. 5.5 Разрезание заготовокПри разрезании заготовок используется профилированный инструмент (вращающийся диск) или непрофилированный - проволока. [Схема разрезания профилированным инструментом показана на рисунке 4] При этой схеме зазор между инструментом-электродом и заготовкой должен быть постоянным. Для выполнения в заготовках различных фигурных пазов, щелей особенно в нежестких материалах применяется непрофилированный инструмент-электрод в виде проволоки из латуни, меди или вольфрама (рис.4.1). Для устранения влияния износа проволоки на точность обработки проволока непрерывно перематывается с катушки на катушку, что позволяет участвовать в работе все новым ее элементам. Схема разрезания профилированным инструментом:  Рисунок 4 1 - электрод - инструмент (диск); - заготовка. Схема разрезания непрофилированным инструментом:  Рисунок 4.1 1 - инструмент - электрод (проволока); - заготовка. 5.6 ШлифованиеПри этом используется вращающийся металлический инструмент цилиндрической формы, который поступательно движется вдоль заготовки 2 со скоростью При обработке недопустимы механические усилия. Применяется также для изготовления деталей из вязких и прочных сплавов. Схема шлифования:  Рисунок 5 1 - электрод - инструмент; - заготовка. 6. Законы Фарадея и скорость электрохимического процессаВыход по току. Применение закона Фарадея к расчету скорости обработки металлов. Электрохимические реакции - это гетерогенные химические реакции, протекающие на границе раздела различных фаз, сопровождающиеся переносом зарядов через эту границу. Все электрохимические реакции при своей записи должны содержать в левой или правой части электроны, потому что происходит их перенос при протекании реакции. Первое, что необходимо знать - это скорость реакции: m = d∆m/dt, (6.1) где Vm - количество вещества, перешедшее через границу в единицу времени. Обозначим через N число ионов, перешедших в раствор, а через Q - полный заряд иона, получающегося в результате реакции Ме Ме +n+n, (6. а) где - элементарный заряд, заряд электрона. Тогда = Q/ne. (6.2) Учитывая, что масса иона а равна атомной массе М, деленной на число Авогадро Na, получим: ∆m = aN =MQ/Na n (6.3) Произведение Na - это произведение двух фундаментальных постоянных (числа Авогадро и заряда электрона). Это произведение носит название константы Фарадея F = 96500 Кл/моль = 26,8 А·час/моль. Тогда: ∆m = Q = It, (6.4) где I - ток, t - время, Q - количество электричества. Уравнение (6.4) представляет собой т. н. объединенный закон Фарадея. Масса вещества, перешедшая в раствор (или выделившаяся на катоде) пропорциональна заряду, прошедшему через систему: ∆m = CQ (6.5) C = (6.6) Величина С носит название электрохимического эквивалента (размерность г/Кл; г/А час). Закон Фарадея является простым следствием атомарной природы вещества. Величие этого закона природы в том, что благодаря ему осуществляется связь между микромиром (заряд иона, единичный заряд) и макромиром (вес осадка на электроде, количество прореагировавшего вещества). Отношение носит название химического эквивалента. Скорость электрохимической обработки Из сотношения (6.4) можно определитьскорость электрохимической обработки: m = Δm/t (6.7) где Vm - массовая скорость обработки (размерность г/мин, мг/с и др.) Выход по току (обозначим его ε) представляет собой долю заряда, пошедшую на данную электрохимическую реакцию. Измеряется в процентах или в долях единицы. ε = ∆mэкс /∆mтеор ·100%, (6.8) где ∆mэкс полученное на практике количество прореагировавшего вещества (окисленного или восстановленного), ∆mтеор - количество прореагировавшего вещества, рассчитанное по закону Фарадея. Значение ε (ВТ) может быть как выше 100%, так и ниже. Последнее наблюдается тогда, когда на электроде протекает несколько электрохимических реакций и на исследуемую расходуется только часть заряда. Выход по току выше 100% наблюдается, когда: ) рассчитанная по закону Фарадея величина получена при большем значении n (числа перенесённых электронов), чем при протекании реакции; ) наряду с электрохимической реакцией на поверхности электрода протекает химическая реакция, не требующая потребления тока; ) при анодном растворении материал частично удаляется механическим путём (дезинтеграция - механическое разрушение металла). Электрохимический эквивалент сплава и практический электрохимический эквивалент. Электрохимической обработке часто подвергаются не чистые металлы, а их сплавы. В этом случае электрохимический эквивалент подсчитывается с использованием метода "сложения зарядов”: = (F xk nk/Mk) - 1, (6.9) где l - число компонентов в сплаве, а xk, nk, Mk - массовая доля, число переносимых электронов и атомная масса k - того компонента сплава. Например, для сплава, содержащего 20% хрома и 80% железа величина xFe = 0,8, а xCr = 0,2, MFe и MCr равны 59 и 52 соответственно (атомные массы железа и хрома), l = 2 (число компонентов сплава), величины nFe и nCr определяются степенью окисления железа и хрома в продуктах растворения. 7. Электрохимический станокТехнологические установки для реализации процесса ЭХО как правило являются узкоспециализированными под определенный технологический процесс, в связи с низкой производительностью (в сравнении с другими методами формообразования: механическая обработка, электроэрозионная обработка Широкое распространение электрохимические станки получили в авиационной промышленности. Распространены установки для получения рабочей поверхности пера лопатки турбореактивных двигателей Однако, распространены и универсальные электрохимические станки, выпускаемые серийно, как правило, это копировально-прошивочные станки, позволяющие обрабатывать широкую номенклатуру деталей прямым копированием. Данные станки обладают одной координатой Z (которая осуществляет формообразование) иногда снабжаются дополнительными координатами (X и Y) для настройки и базирования взаимного расположения электрода и обрабатываемой поверхности в заготовке. Данные станки широко применяются в инструментальной промышленности для обработки штампов, пуансонов и других твердосплавных формообразующих технологических элементов.  Копировально-прошивочный электрохимический станок ET 3000 электрохимическая размерная обработка станок ЗаключениеВ курсовой работе исследованы физико-химические процессы, протекающие при ЭХП меди, а также теория ЭХП в целом. Рассмотрено применение полирования металлов в технологии машиностроения. Описаны составы некоторых электролитов и режимы электрохимического полирования меди и их обоснование. Также дано обобщённое понятие о механизме и кинетике процесса согласно мнениям некоторых исследователей и в свете современных представлений. Однако следует заметить, что процесс ЭХП, несмотря на своё широкое применение, всё ещё недостаточно изучен и некоторые его положения всё ещё нуждаются в доработке и переосмыслении. Выполненная курсовая работа позволила выяснить важность физико-химического подхода при решении технологических проблем электрохимического полирования. Библиографический список1. Щиголев П.В. Электрохимическое и химическое полирование металлов. М., 1959. . Грилихес С.Я. Обезжиривание, травление и полирование металлов. Л.: Машиностроение, 1983. . Грилихес С.Я. Электрохимическое травление, полирование и оксидирование металлов. Машгиз, 1957. . Справочник по электрохимии. Под ред. Сухотина А.М. Л.: Химия, 1981. . Технология химической и электрохимической обработки поверхности металлов. Машгиз, 1961. |
