олимпиада. Олимпиадные задания по химии с решениями (8 класс). 1. в стратосфере на высоте 20 30 км находится слой озона О
 Скачать 33.58 Kb. Скачать 33.58 Kb.
|
|
8 класс 1. В стратосфере на высоте 20 – 30 км находится слой озона О3, защищающий Землю от мощного ультрафиолетового излучения Солнца. Если бы не «озоновый экран» в атмосфере, то фотоны с большей энергией достигли бы поверхности Земли и уничтожили на ней все живое. Подсчитано, что в среднем на каждого жителя Санкт- Петербурга в воздушном пространстве над городом (вплоть до верхней границы стратосферы) приходится по 150 моль озона. Сколько молекул О3 и какая масса озона приходится в среднем на одного петербуржца? Круговорот азота в природе включает: а) «биологическую фиксацию» при помощи клубеньковых бактерий и б) процессы окисления при атмосферных электрических разрядах. Во время грозы в воздухе образуется некоторое количество оксида азота неизвестного состава. Установлено, что абсолютная масса одной молекулы этого оксида азота составляет 4,99•10-23 г. Определите, какова формула этого вещества. Элементы Х и Y образуют с хлором соединения состава XYCl2 и XY2Cl2. Массовые доли хлора в этих соединениях равны соответственно 59,66 и 52,59%. Определите формулы неизвестных соединений. Антуан Лоран Лавуазье открыл природу горения различных веществ в кислороде после своего знаменитого двенадцатидневного опыта. В этом опыте он сначала длительное время нагревал в запаянной реторте навеску ртути, а позже (и при более высокой температуре) – образовавшийся на первом этапе опыта оксид ртути (II). При этом выделялся кислород, и Лавуазье стал вместе с Джозефом Пристли и Карлом Шееле первооткрывателями этого важнейшего химического элемента. Рассчитайте количество (моль) и объем кислорода (при н.у.), собранный при разложении 108,5 г HgO. Рассчитайте, какой объем водорода (н.у.) выделится при полном растворении в соляной кислоте 10 г простого вещества, в атоме которого находятся 26 протонов. Решения Решениезадачи№1 В решении задачи используется уравнение, связывающее между собой число частиц в данной порции вещества и постоянную Авогадро. N(O3) = (O3)N = 150 моль6,021023моль-1 = 9,031025 m(O3) = (O3)M(O3) = 150 моль48 г/моль = 7200 г = 7,2 кг Решениезадачи№2 Чтобы установить формулу оксида азота NxOy, который образуется во время грозы, достаточно узнать молярную массу этого соединения. Известные к настоящему времени оксиды азота состава N2O, NO, N2O3, NO2, N2O4, N2O5 имеют молярные массы, равные соответственно 44, 30, 76, 46, 92 и 108 г/моль. Напишем уравнение, связывающее между собой молярную массу вещества M(NxOy), абсолютную массу молекулы m(NxOy) и постоянную Авогадро N M(NxOy) = m(NxOy) N = 4,9910-23 г 6,021023моль-1 = 30 г/моль Решениезадачи№3 Пользуясь формулой для определения массовой доли элемента в соединении, вычислите молярные массы соединений XYCl2 и XY2Cl2:  ω(Cl в XYCl2) = 2𝑀(𝐶𝑙) ω(Cl в XYCl2) = 2𝑀(𝐶𝑙)𝑀(𝑋𝑌𝐶𝑙2) *100%, следовательно,  M(XYCl2) = 2𝑀(𝐶𝑙) M(XYCl2) = 2𝑀(𝐶𝑙)𝜔(𝐶𝑙 в 𝑋𝑌𝐶𝑙2) 100% = 235,5 г/моль 100% = 119 г/моль  59,66% 59,66%Аналогично для XY2Cl2:  M(XY2Cl2) = 2𝑀(𝐶𝑙) M(XY2Cl2) = 2𝑀(𝐶𝑙)𝜔(𝐶𝑙 в 𝑋𝑌2𝐶𝑙2) 100% = 235,5 г/моль 100% = 135 г/моль  52,59% 52,59%Найдем массы неизвестных элементов, входящих в состав второго и первого соединений: M(XY) = M(XYCl2) – 2M(Cl) = 119 г/моль – 235,5 г/моль = 48 г/моль M(XY2) = M(XY2Cl2) – 2M(Cl) = 135 г/моль – 235,5 г/моль = 64 г/моль Учитывая, что M(XY) = M(X) + M(Y), а M(XY2) = M(X) + 2M(Y), и обозначив M(X) и M(Y) соответственно как x и y, составим систему уравнений: 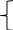 х + y = 48 х + y = 48х + 2y = 64, решая которую получим, что х = 32, y = 16. Значит, M(X) = 32 г/моль, M(Y) = 16 г/моль. Пользуясь Периодической системой элементов, определяем, что X – это сера, а Y – это кислород. Таким образом, формулы неизвестных соединений – SOCl2 SO2Cl2 . Решениезадачи№4 Запишем уравнение реакции: t° 2HgO = 2Hg + O2↑ Количество вещества кислорода, который выделяется при разложении оксида ртути (II), составляет: (O2) = 1\2(HgO) = (1\2m(HgO)) / M(HgO) = 108,5 г/(2172) г/моль = 0,25 моль ; а его объем при н.у.: V(O2) = (O2)Vm = 0,25 моль22,4л/моль = 5,6 л Решениезадачи№5 Простое вещество, содержащее 26 протонов (то есть соответствующее порядковому номеру элемента) – это железо. Запишем уравнение реакции железа с соляной кислотой: Fe + 2HCl = FeCl2 + H2↑ По уравнению реакции количество выделившегося газа (водорода) равно количеству вступившего в реакцию железа. Можем найти объем водорода при н.у.: (H2) = (Fe) = m(Fe)/M(Fe) = 10г/56 г/моль = 0,179 моль V(H2) = (H2) Vm = 0,179 моль 22,4 л/моль = 4 л |
