шпора фхонт. 12. Асимптотическая близость к критической точке это область. ТТкр(1 1) рркр. 7 3) область изменения свойств в окрестности критической точки Критическая точка это точка при температуре ниже которой газ никоем образом нельзя перевести в жидкое состояние (конец двухфазного состояния).
 Скачать 276 Kb. Скачать 276 Kb.
|
|
12. Асимптотическая близость к критической точке это область. Т=Ткр(1/1.1) р=ркр.(0.7/1.3) -область изменения свойств в окрестности критической точки Критическая точка- это точка при температуре ниже которой газ никоем образом нельзя перевести в жидкое состояние (конец двухфазного состояния). 16. Первая теория критических явлений связана с уравнением Ван-дер-Ваальса. В рамках этой теории увязываются значения критических параметров с индивидуальными Const a и b : Ркр., Ткр., Vкр.=(a,b,R). Уравнение Ван-дер-Ваальса качественно верно описывает однофазные состояния вещества, однако это уравнение неверно для двухфазного состояния на границе критического состояния. Уравнение Ван-дер-Ваальса относиться кпластическим теориям критических явлений. Критические явления не ограничевается около кристалическими состояниями в системе Ж+П. Туда относятся феромагнитный переход сигмето-электрика,в точке Кюри. 2)Теория среднего поля Вейсса. Согласно этой теории молекулы движуться в некотором среднем поле и в рамках этой теории критические индексы получаются точно такими же. В рамках класической теории есть модельные системы которые рассматривались на примере феромагнетик-это одномерная модель Изинга, двухмерная, трёхмерная, модель Гейзенберга, модель решёточного газа. модельные системы дают крит. индексы похожие на результаты уравнения Ван-дер-Ваальса. Трёхмерные модели дают значения которые ближе для значений реальных газов. 3) Обобщением для классических теорий крит. явлений, является теория Ландау. В этой теории свободная энергия термодинамической системы может быть разложена в ряд, по степеням параметра порядка. Теория Ландау даёт те же значения что и уравнение Ван-дер-Ваальса. альфа=0-0.1; бетта=1/2; гамма=1.2-1.4; сигма= 4.2/4.4. Билет 17.1.Модель Изинга --- математическая модель статистической физики, предназначенная для описания намагничивания материала.Одномерная модель Изинга позволяет получить весьма поучительные результаты при рассмотрении макромолекул - систем с сильными взаимодействиями вдоль цепи. Для рассмотрения ферромагнетиков одномерная модель непригодна. В самом деле, заменяя длину стрелки 1 магнитным моментом ц и внешнюю силу f напряженностью магнитного поля Н, мы получаем для намагничения формулу, не описывающую спонтанного намагничения и фазового перехода в точке Кюри.В теории ферромагнетизма необходима по крайней мере двумерная модель.Поэтому фазовые переходы в одномерной модели Изинга невозможны.Таким образом, хотя в одномерной модели Изинга фазовые переходы не происходят, в случае цепочки с в 0 существует критическое значение напряженности магнитного поля Нк ( е - е) / / д, вблизи которого осуществляется переход от состояния с чередующимися диполями первого и второго вида ( при Н: 7 / к) к полностью упорядоченному состоянию ( при Я ЯК), причем при Г-0 этот переход становится скачкообразным. Модель Изинга - простейшая математическая модель статистической физики,предназначенная для описания намагничивания материала. Двумерная модель Изинга описывается решеткой, в узлах которой расположены спины, принимающие только два значения: +1 или -1 (направление спина "вверх" или "вниз").Для описания ферромагнитного или антиферромагнитного упорядочивания в различных математических моделях обычно используют выражение энергии обменного взаимодействия спинов, предложенного Дираком, в котором энергия пропорциональна скалярному произведению операторовспинов s1 и s2 18. Среди теорий Крит явлен большое распространение получила теория, рассматривающая вещество в окрестности точки фазового перехода как систему флуктуирующих областей размера Rc. Она называется теорией масштабных преобразований (скейлинг-теорией). Скейлинг-теория не позволяет из свойств молекул, составляющих вещество, вычислить критические индексы, но даёт соотношение между индексами, которые позволяют вычислить их все, если известны какие-нибудь два из них. Соотношения между критическими индексами позволяют определить Уравнение состояния и вычислять затем различные термодинамические величины по сравнительно небольшому объёму экспериментального материала. Эта теория называется динамическим скейлингом в отличие от статического скейлинга, который относится только к термодинамическим свойствам материи. Метод ренормализационной группы в квантовой теории поля — итеративный метод перенормировки, в котором переход от областей с меньшей энергией к областям с большей вызван изменением масштаба рассмотрения системы. В теоретической физике метод ренормализационной группы относится к математическому аппарату, который позволяет систематическое исследование изменений физической системы при рассмотрении системы на разных пространственных масштабах 19. 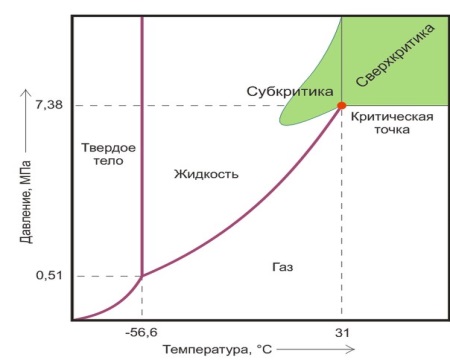 Субкритическое состояние-это состояние вещества в основном в жидком состоянии, с хорошей растворяющей способностью. Субкритические вещества обладают относительно высокой вязкостью. Сверхкритическое состояние- это состояние вещества которые обладают достоинствами газового состояния. Но по сравнению с субкритическим состоянием вязкость СК вещества относительно ниже примерно от 10 до 100 раз. вещества в СК состоянии имеют хорошую растворяющую способность. 20. СКФ Ряд физических свойств сверхкритических флюидов представляют собой нечто промежуточное между жидкостью и газом. Они могут сжиматься как газы (обычные жидкости практически несжимаемы) и, в тоже время, способны растворять твердые вещества, что газам не свойственно. Сверхкритический этанол (при температуре выше 234° С) очень легко растворяет некоторые неорганические соли (CoCl2, KBr, KI). Диоксид углерода, закись азота, этилен и некоторые другие газы в состоянии СКФ приобретают способность растворять многие органические вещества. Свойства сверхкритического CO2 как растворителя можно регулировать — при повышении давления его растворяющая способность резко увеличивается. СБКФ облодают высокой плотностью свойственной жидкостям, что определяет хорошую растворяющую способность. Вместе с тем эти среды облодают относительно высокой вязкостью, что определяет низкие маслообменные характеристики с их участием. преобладаю в жидком состоянии. 21. СКФ –сверкритические флюиды обладают достоинством в газообразном состоянии которых нету у жидкости. Вязкость СКФ от 10 до 100 раз меньше чем у органических жидкостей. Коэфициент дифузии от 10 до 100 раз больше, как следствие СКФ обеспечивает не только хорошую растворяющую способность но и высокие тепло- и масло обменные характеристики. 22. Анализ имеющихся на сегодняшний день данных по растворимости чистых веществ в СК-растворителях позволяет говорить о существовании кроссоверного давления прикотором изотерма на графике зависимости растворимости от давления сходятся или сближаются в данной точке. Ниже этого давления рост давления приводит к понижению растворимости, а выше-к её увеличению. 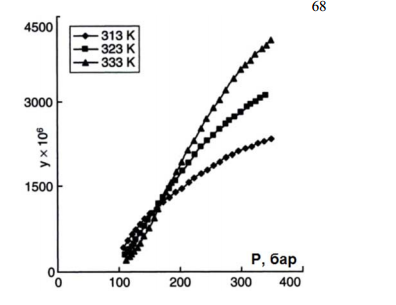 кросоверная точка на графике. С ростом температуры возрастает давление насыщенного пара растворённого вещества, при этом сверхкритического раство‐ рителя падает. Ниже кроссоверного давления, где сжимаемость вещества выше, большее влияние на растворимость оказывает плотность, а выше него большее влияние на раствори‐ мость оказывает давление насыщенного пара. Существующие методы измерения растворимости веществ в СКФ делятся по двум критериям. По способу получения насыщенного раствора на статические (равновесные), ре‐ циркуляционные и динамические (проточные). По способу анализа состава растворов – на спектроскопический, хроматографический, метод насыщения (испарения), метод точек росы и кипения. 25. При растворении молекулы или ионы вещества распределяются более или менее равномерно между молекулами растворителя.Полярный растворитель должен легко растворять только полярные вещества, а неполярный растворитель - только неполярные вещества. Это соответствует правилу: "Подобное растворяется в подобном". Растворимость зависит от природы растворяемого вещества и растворителя, температуры и давления. Ионные вещества растворяются в полярных растворителях и плохо в неполярных, а молекулярные вещества - наоборот. Влияние температуры. Если растворение вещества является экзотермическим процессом, то с повышением температуры его растворимость уменьшается (Например, Ca (OH) 2 в воде) и наоборот. Для большинства солей характерно увеличение растворимости при нагревании. Практически все газы растворяются с выделением тепла. Растворимость газов в жидкостях с повышением температуры уменьшается, а с понижением увеличивается. Влияние давления. С повышением давления растворимость газов в жидкостях увеличивается, а с понижением уменьшается. -Поскольку раствор вещества в СКФ являются разбавленными, то практический интерес, представляет зависимость растворимости вещества от Т,Р,р чистого растворителя, находящегося вблизи собств. крит. точки. Термодинамическое равновесие между конденсированной фазой и её насыщенным паром нарушается в случае наложения внешнего давления со стороны сверхкритического флюида. Это приводит к снижению концентрации молекул жидкости в паровой фазе. Для того чтобы вернуть систему в равновесное состояние, необходимо,чтобы некоторое количество молекул жидкости перешло в поровую фазу. Это означает рост давления насыщенных паров конденсированной фазы при данной температуре, что полностью отвечает правилу фаз Гиббса. Данный процесс называется эфект Пойтинга: Е=хР/Рv где Е- отношение парциального давления паров растворённого вещества в фазе 27)Природа СКФ-растворителей и использование сорастворителя. СКФ среда имеет два преимущественных фактора: 1) При соответ. Давлениях плость СК флюида может быть равна плотности жидкости, а стало быть растворяющая способность может быть равна растворяющей способности органических растворителей. 2) СК флюиды обладают достоинствами газообразного состояния которого нет в жидкостях. ИХ вязкость от 10 до 100 раз меньше вязкости орган. Жидкостей, а коэффициент диффузии 10-100 раз больше. Сорастворители используют для улучшения процесса растворения или для его осуществления(ссылка на 29 вопрос). В некоторых случаях использование свойст сорастворителя увеличивают растворимость до 100 раз. Сорастворители используют в количестве 3-5% к основному растворителю. 28)Основные процессы с использованием СКФ сред: 1)СКФ экстракция; 2)Сушка по СКФ пути; 3)СКФ импрегнационный процесс; 4)Диспергирование материалов с использованием СКФ сред(до 10^(-9)); 5)Реакции в СКФ средах; 6)СКФ хромотография. 29)СКф экстракциооный процесс. Существует несколько СКФ циклов экстракции: 1)Комперссорный цикл; 2)Изобарический цикл; 3) Метод реализации сеппарации адсорбированным методом. Экстракцию можно проводить при t=40-60’С. Но СО2 будучи неполярным веществом не способно экстрагировать полярные компоненты. Для решения этой задачи достаточно использовать полярный сорастворитель. Экстракция с исп СКФ растворителей более эконом. Выгоднее чем процессы с исп. Жидких растворителей. 30)Сушка по СКФ траектории. В традиционном исполнении это поверхностный переход жидкой фазы в парообразную. Изменение геометрических размеров жидкой фазы, с поверхности которой происходит испарение, определяет изменение величины поверхностных сил. Примером служит вода в объеме банки или стакана, в случае разрушения сосуда вода не в состоянии сохранить свою форму за счет поверхностных сил, но в случае меньших размеров, капля воды силой поверхностного напряжения позволяет сохранить эту форму, в случае же нано-размеров жидкой фазы, поверхностные напряжения еще более высоки, что в случае традиционной сушки приводит к разрушению внутренней структуры, Данную проблему можно решить если сушку производить по СК пути, не пересекая кривую насыщения. В этом случае жидкая фаза при переходе в СКФ состояние, мгновенно переходит в состояние плотных газов, что обеспечивает сохранность развитой поверх. аэрогелей. 31)Импрегнация с использованием СКФ сред.(пропитка) СКФ среды представляющие собой плотный газ имеет нулевое поверхностное натяжение ,в отличие от жидкости, и может легко проникать в любые пористые структуры, что является основанием для новых высокотехнологичных процессов. Все это предполагает предварительное растворение материала пропитки в СКФ растворителе. В СКФ средах не растворяются ни оксиды металлов, ни сами металлы. В этом случае предварительно формируется металлорганический комплекс на основе выбранного редкого метала с помощью добавления соответствующих комплексообразующих- Лигенда. Существует 2 метода пропитки: Динамический; Статический. 32)Метод диспергирования RESS- первоначально твердое вещество растворяется в сверхкритическом флюиде, затем расширяется в атмосферные условия через нагреваемое расширительное устройство. Основным параметром растворяющей способности СК флюида является плотность. При сбросе давления растворитель переходит в газообразное состояние, а вешество осаждается в виде мелкодисперсного аэрозоля. Так же этот метод применяется и для получения нано частиц. Для этого расширение производиться не в атмосферную среду, а в жидкую. Метод диспергирования SAS-Орг.метода SAS заключается,в том что процесс реализуется лишь в том случае когда диспергированый материал растворим в СКФ среде.Бывают случае что диспергированный материал плохо растворим в СКФ среде в этих случаях используют метод который лежит на основе принципа антирастворителя, такой метод наз метод SAS.В этом методе СК СО2 добавляемый в раствор диспергированного материала в орг. Растворителе снижает растворяющую способность жидкого орг. Растворителя,тем самым способствует осаждению дисперсного материала.(Дисперг материал+орг.растворитель)применяется когда диспергированный раствор не растворяется. 33)Реакции в СКФ средах. Многие физические и химические свойства СКФ находятся между таковыми для жидкости и газа. СКФ обладают также уникальной растворяющей способностью. Так компоненты, не растворимые в жидкости при нормальных условиях, становятся практически полностью растворимые в этой жидкости, находящейся в сверхкритических условиях. Многие газы, имеющие ограниченную растворимость в органических жидкостях, в условиях сверхкритического растворителя получают неограниченную растворимость в ней. Сверхкритические растворители привлекательны и для проведения гетерогенных каталитических реакций, так как вследствие высоких коэффициентов диффузии и растворимости реакционных компонентов предотвращается образование кокса и увеличивается скорость проникновения реагентов в поры зерна катализатора, увеличивая фактор эффективности катализатора. Практическое использование СКФ включает технологии утилизации и разложения отходов, процессы преобразования биомассы и угля, синтез новых материалов и многие другие. Так, технологии, использующие СКФ для преобразования твердых природных органических материалов, в частности угля, включают процессы ожижения и экстракции. Среди химических реакций, осуществляемых в СКФ, наибольшее практическое применение сегодня находят окислительные реакции. Еще к одному динамично развивающемуся направлению в использовании свойств сверхкритических растворителей следует отнести химические превращения моно- и политер-пеновых растительных соединений, к которым относятся скипидары хвойных деревьев, канифоль, а- и р-пинены, камфен и др. Среди известных и перспективных методов синтеза и модификации наночастиц наибольшее внимание в последнее время уделяется методам с использованием сверхкритических флюидов. Так, СКФ используются для получения наночастиц металлов (Pt, Pd, Rh, Au, Ag, композитов типа PtPd, PtRu и др), полимерных материалов, окислов металлов и их нитритов (ТЮ2, СГ2О3, C02N, C^N), синтеза наночастиц металлов типа L¡FeP04 и аналогичных соединений, микрокапсулирования наночастиц. 35)Плюсом СКФ растворителей- это то что регенерация экстрагента и выделение экстаркта может быть реализрвано простым сбросом давления. В случае компрессных циклов, понижение растворяющей способности экстрагента на этапе регенерации достигается за счет понижения давления существеющих циклов, в которых понижение растворяющей способности достигается за счет изменения температуры. Потребность таких циклов обусловлена что сброс давления после каждого цикла является энергозатратным. Метод сепаррации реализованный на адсорбционном методе. Как бы то ни было странно регенерация адсорбента может быть осуществлена тем же СО2, при других циклах и параметрах. 36) Некоторые типы мономеров, в особенности с мультaкрилатной и метaкрилатной функциональностью, исключительно трудно очищаются свыше 99% традиционными методами. Вместе с тем для большинства промышленно применяемых мономеров присутствие 1% остаточного растворителя, исходных материалов или побочных продуктов безвредно и они не нуждаются в дополнительной очистке. Однако существуют случаи, когда остающиеся в Мономерах компоненты могут придавать им, и впоследствии полимерам, некоторый нежелательный и подлежащий удалению запах или цвет. Сложность использования, например, метода дистилляции в этом случае заключается в том, что, как правило, эти МОНОмеры и нечистоты имеют низкие значения давления насыщенных паров. И достижение достаточных значений летучести компонентов посредством их нагревания Наталкивается на проблему термолабильности мономеров, требующую их обработки при умеренных температурных режимах. Выход из положения-использование процесса сверхкритического экстрагирования. Справедливости ради следует отметить, что сверхкритическая флюидная экстракция не является панацеей и должна применяться от случая к случаю. 37)Полимеризация в СКФ средах. Несмотря на высокие значения давления и соответствующие энергетические затраты этот метод продолжает функционировать благодаря такому достоинству, как растворение получаемого полиэтилена в сверкритическом этилене и легкому непрерывному транспортированию его в технологическом цикле. В случае полимеров синтезированных в суб- и сверх критическом СО2, то этот метод экологически безопасен и к тому же отсутствует необходимость в дорогостоящей сушке продукта и процессе удаления растворителя. 38)Кинетика кристаллического полимера в среде СКФ. В полимерах есть 2 фазы: кристаллическая, аморфная. При обычных температурных условиях образцы полиэтилена содержат 55-70%(высокого давления) и 80-90%(низкого давления) кристаллической фазы. При быстром охлаждении полимера(закалка) и относительно малой кристаллизации полимер затвердевает с большим содержанием аморфной фазы. Вблизи точки плавления, кристаллическая фаза полностью исчезает. Обнаружено, что время кристализации в СКФ случае снижается на порядок величины на каждую 1Мпа роста давления. Простая экстраполяция этих значений в областях более высоких давлений позволяет предположить что при некотором значении давления время кристализации будет значительно меньшим времени сорбции диоксида угларода полимерной пленкой. В следствии чего, среда сжатого СО2 может быть использована в целях управления кинетикой кристализации. 39) СКФ импрегнация полимерных материалов(пропитка). В процессе пропитки полимеров различными добавками находят большее применение именно сверхкритические, а не субкритические флюиды. Благодаря свойствам СКФ(низкая вязкость, высокая диффузионность, нулевое поверхностное натяжение и др), которые дополняются тем, что СКФ оказываются менее сильными агентами набухания полимеров(в отличие от органических жидкостей). На первом этапе матрица промывается СК раствором пропитки. На втором этапе осуществляется резкая декомпрессия, позволяющая пропитке осесть внутри матрицы в результате потери флюидом растворяющей способности и быстрого его исчезновения из полимера в газообразном состоянии. 40) Вспененные полимеры. Экстрагирование некоторых составляющих твердых материалов с помощью СКФ может в некоторых случаях привести к формированию пористой структуры со свойственными ей характеристиками. В частности, полимер представляющий собой смесь высоко- и низкомолекулярных цепей, может быть обработан СКФ, который в свою очередь при соответствующих условиях растворит лишь низкомолекулярные составляющие. Результаты исследований в этой области дают основание полагать о перспективности данного подхода к выработке мембран. 41)Диспергирование полимерных материалов в СКФ средах. Существует 2 принципиально разные функции СКФ: 1) растворителя(RESS); 2)Осадитель или антирастворитель(SAS, GAS и др.). В первом случае диспрегирование материала осуществляется благодаря быстрому расширению СКФ раствора диспергируемого материала. Во втором случае диспергируемый материал, предварительно растворенный в органическом растворителе, осаждается в результате введения в систему некоторого количества СКФ, в котором он не растворим. 42) Термодинамические основы методов RESS, SAS. RESS  На ТS диаграмме процес 1-2 соответствует адиабатному процессу сжатия СО2, процесс 2-3 соответствует процессу нагревания, процесс 3-4 соответствует изоэнтальпийному процессу расширения(расширение газа), процесс 4-5 соответствует испарению жидкой фазы и в процессу 5-1 диоксид углерода сжижается. SAS-Орг.метода SAS заключается,в том что процесс реализуется лишь в том случае когда диспергированый материал растворим в СКФ среде.Бывают случае что диспергированный материал плохо растворим в СКФ среде в этих случаях используют метод который лежит на основе принципа антирастворителя, такой метод наз метод SAS.В этом методе СК СО2 добавляемый в раствор диспергированного материала в орг. Растворителе снижает растворяющую способность жидкого орг. Растворителя,тем самым способствует осаждению дисперсного материала.(Дисперг материал+орг.растворитель)применяется когда диспергированный раствор не растворяется. 43)Биорезорбируемые полимеры (постепенно растворяющиеся в организме)- полимерные микрочастицы заданного химического состава, размера и внутренней структуры. К ним предъявляются высокие требования по токсичности и биосовместимости, а также по возможности контролируемого выхода из них биологически активных компонентов в кровь или определенные ткани человеческого организма. Все это до недавнего времени было труднореализуемо, но в 90гг. прошлого века когда для синтеза биорезорбируемых полимерных микрочастиц, начали использовть СКФ.(RESS,кр) 44)Покраска полимерных волокон и формирование порошковых покрытий. Применение СКФ покраски в значительной степени сокращает затраты поп причине неиспользования воды и отсутствия необходимости в последующей обработку окрашенного материала, и этот подход может решить задачу в принципе в случае тех полимерных волокон, которые вообще не могут быть покрашены обычными методами. Принцип покраски: СК СО2 растворяет в себе краситель в экстракторе; далее имеют место сепарация и выпадение красителя в сосуде покраски, и в том числе на окрашиваемые волокна. Длительность процесса определяется степенью достижения результата. Порошковые полимерные покрытия имеют много преимуществ. Прежде всего их применение не связано с использование органических растворителей. Технология приготовления порошковых красок весьма проста: исключается растворение, замешивание, диспергирование, фильтрование и многие другие трудоемкие операции. 47)Решение экологических проблем. 1)Очистка сточных вод(1.1 СКФ экстракционный прцоесс; 1.2 2-х стадийный процесс очистки сточных вод; 1.3 СК водное окисление), 2)Очистка почв(2.1Использование СКФ экстракционного процесса), 3)Утилизация бытовых и промышленных отходов(3.1Отработанные масла; 3.2Утилизация адсорбентов и катализаторов применяя СК СО2 экстракцию), 4)Решение экологических проблем благодаря выполнению условий зеленой химии в рамках СКФ технологии 48)12 принципов зеленой химии: 1. Лучше предотвратить потери, чем переработать и чистить остатки. 2.Методы синтеза надо выбирать таким образом, чтобы все использованные материалы в процессе были максимально переведены в конечный продукт. 3.Методы синтеза выбирают так, чтобы исп. и синтезирование вещества были как можно менее вредны для человека и окружающей среды. 4.Создавая новые химические продукты надо стараться сохранить эффективность работы, при этом точксичность должна быть минимальна. 5.Вспомогательные вещества при производстве лучше не использоватьЮ а если это невозможно, их использование должно быть безвредным. 6.Обязательно следует учитывать затраты и их влияние на окружающую среду. Синтез по возможности проводить при Т близкой к окружающей среде и атмосферном давлении. 7.Исходники, расходники должны быть восполнены, когда это технически и экономически выгодно. 8.При возможности надо избегать получения промежуточных продуктов. 9.Всегда следует отдавать предпочтения каталитическим процессам. 10.Химические продукты должны быть такими, чтобы после их использования он не оставался в окружающей среде, а разлагался на безопасные продукты. 11.Нужно развивать аналитические методы, для слежки в реальном времени за образование опасных продуктов. 12.Вещества и формы веществ нужно выбирать таким образом, чтобы риск химической опасности включая утечки, взрыв и пожар, были минимальны. 49)Это самими можно на шару придумать)))))) |
