Курсовая работа, расчет печи. Курсова_Печь. 1литературный обзор 2 1Принцип действия тепловых насосов 2
 Скачать 0.64 Mb. Скачать 0.64 Mb.
|
Теплоутилизатор-вентиляторТеплоутилизатор-вентилятор включает ротор с лопатками диаметром 0,6 м, собранными из термосифонов (рисунок 8). Ротор разделен перегородкой на две части, каждая из которых заключена в улиткообразный кожух, выполненный по аэродинамической схеме прямоточного вентилятора. Через клиноременную передачу ротор соединен с электродвигателем. Лопатки ротора обеспечивают раздельное перемещение приточного и удаляемого воздуха без смешения. В холодный период года теплота удаляемого воздуха затрачивается на испарение рабочего вещества в термосифоне. В парообразной фазе рабочее вещество поступает в ту часть ротора, где проходит холодный наружный воздух. При конденсации его через стенки трубок передается теплота на нагрев приточного воздуха. После этого рабочее вещество в жидкой фазе центробежными силами возвращается в зону кипения. Благодаря вращению ротора данный аппарат выполняет функции одновременно теплоутилизатора и вентилятора. При этом центробежные силы сбрасывают конденсат с наружной поверхности термосифонов, что предохраняет их от образования инея [7]. 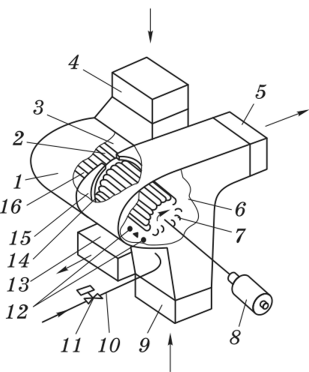 1 — кожух; 2 — сальниковое устройство между перегородкой в кожухе и разделительным диском; 3 — канал для прохода приточного воздуха; 4 — воздуховод забора наружного воздуха; 5 — воздуховод выброса; 6 — канал для прохода удаляемого воздуха; 7— лопатки из термосифонов; 8— электродвигатель; 9 — воздуховод удаляемого воздуха; 10 — присоединение водопровода; 11 — автоматический вентиль периодической подачи воды для промывки ротора; 12 — оросительные сопла; 13 — приточный воздуховод; 14 — разделительный диск; 15 — перегородка в кожухе; 16 — ротор Рисунок 8 – Принципиальная схема теплоутилизатора-вентилятора 2 Исходные данные Рассчитать трубчатую печь для нагрева и частичного испарения нефти при следующих исходных данных: Количество отбензиненной нефти – 3200 т/сут; начальная температура сырья Т1 = 447 К, конечная температура сырья Т2 = 620 К, плотность отбензиненной нефти 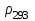 = 877 кг/м3, массовая доля отгона при температуре 620 К на выходе е = 0,60, плотность отгона при 293 К = 877 кг/м3, массовая доля отгона при температуре 620 К на выходе е = 0,60, плотность отгона при 293 К 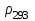 = 875 кг/м3, плотность остатка = 875 кг/м3, плотность остатка 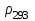 = 956 кг/м3, состав топливного газа (% об) CH4 = 54, C2H6 = 18, C3H8 = 16, н–C4H10 = 8,1, CO2 = 0,8, N2 = 3,7; плотность газа – 0,75 кг/м3 (при нормальных условиях). = 956 кг/м3, состав топливного газа (% об) CH4 = 54, C2H6 = 18, C3H8 = 16, н–C4H10 = 8,1, CO2 = 0,8, N2 = 3,7; плотность газа – 0,75 кг/м3 (при нормальных условиях). 3 Расчетная часть3.1 Расчет процесса горенияОпределим низшую теплоту сгорания топлива (в кДж/м3) по формуле: 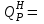 360,33·CH4 + 590,4·C2H4 + 631,8·C2H6 + 868,8·C3H6 + 913,8·C3H8 +, 360,33·CH4 + 590,4·C2H4 + 631,8·C2H6 + 868,8·C3H6 + 913,8·C3H8 +, + 1092,81·изо–C4H10 +1195·н–C4H10 + 1146·C4H8 + 1460,22· C5H12 + 251,2·H2, (3.1) где CH4, C2H4 и так далее – содержание соответствующих компонентов в топливе, объемные %. Получим: 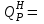 360,33·54 + 631,8·18+ 913,8·16+1195·8,1 = 55130,52 кДж/м3 360,33·54 + 631,8·18+ 913,8·16+1195·8,1 = 55130,52 кДж/м3или 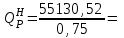 73507,36 кДж/кг. 73507,36 кДж/кг.Пересчитаем состав топлива в массовые проценты, результаты сведем в таблицу 1. Таблица 1 – Состав топлива в массовых процентах.
Определим элементарный состав топлива в массовых процентах. Содержание углерода в любом i–м компоненте топлива находим по соотношению: 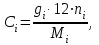 (3.2) (3.2)где ni – число атомов углерода в данном компоненте топлива. Содержание углерода: 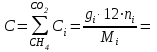 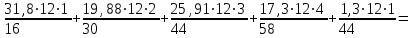 =75,625 масс. % =75,625 масс. %Содержание водорода: 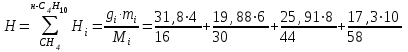 = 19,6197 масс. %, (3.3) = 19,6197 масс. %, (3.3)где mi – число атомов водорода в данном компоненте топлива. Содержание кислорода: 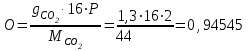 масс. %, (3.4) масс. %, (3.4)где Р – число атомов кислорода в молекуле СО2. Содержание азота: 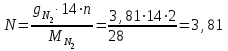 масс. %, (3.5) масс. %, (3.5)где n – число атомов азота в молекуле. Проверка: C + H + O + N = 75,625 + 19,6197 + 0,94545 + 3,81 = 100 масс. % (3.6) Определим теоретическое количество воздуха, необходимого для сжигания 1 кг газа, по формуле: 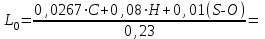 (3.7) (3.7)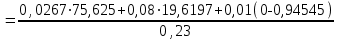 =15,56 кг/кг =15,56 кг/кгКоэффициент избытка воздуха 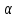 = 1,03 = 1,03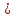 1,07. Принимаем 1,07. Принимаем 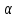 = 1,06. Тогда действительное количество воздуха: = 1,06. Тогда действительное количество воздуха:Lд = 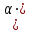 L0 = 1,06·15,56 = 16,49 кг/кг (3.8) L0 = 1,06·15,56 = 16,49 кг/кг (3.8)или 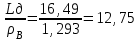 кг/кг, (3.9) кг/кг, (3.9)где 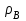 = 1,293 кг/м3 – плотность воздуха при нормальных условиях (273 К и = 1,293 кг/м3 – плотность воздуха при нормальных условиях (273 К и 0,1·106 Па). Определим количество продуктов сгорания, образующихся при сжигании 1 кг топлива: 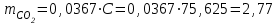 кг/кг; (3.10) кг/кг; (3.10)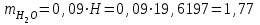 кг/кг; (3.11) кг/кг; (3.11) 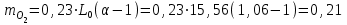 кг/кг; (3.12) кг/кг; (3.12)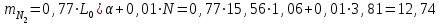 кг/кг (3.13) кг/кг (3.13)Суммарное количество продуктов сгорания: 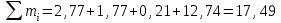 кг/кг (3.14) кг/кг (3.14)Проверка: 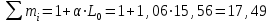 кг/кг (3.15) кг/кг (3.15)Содержанием влаги в воздухе пренебрегаем. Найдем объемное количество продуктов сгорания (в м3) на 1 кг топлива (при нормальных условиях): 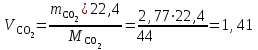 м3/кг; (3.16) м3/кг; (3.16)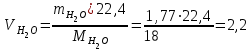 м3/кг; (3.17) м3/кг; (3.17)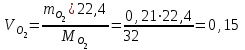 м3/кг; (3.18) м3/кг; (3.18)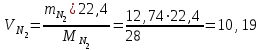 м3/кг. (3.19) м3/кг. (3.19)Суммарный объем продуктов сгорания: 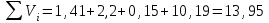 м3/кг (3.20) м3/кг (3.20)Плотность продуктов сгорания при 273 К и 0,1·106 Па: 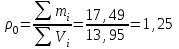 кг/м3 (3.21) кг/м3 (3.21)Определим энтальпию продуктов сгорания на 1 кг топлива при различных температурах по уравнению: 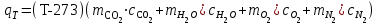 , (3.22) , (3.22)где Т – температура продуктов сгорания, К; 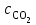 , , 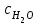 , , 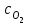 , , 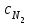 – средние массовые теплоемкости продуктов сгорания, определяемые из таблицы [8] (приложение 7), кДж/(кг·К). – средние массовые теплоемкости продуктов сгорания, определяемые из таблицы [8] (приложение 7), кДж/(кг·К).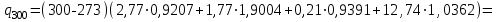 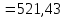 кДж/кг кДж/кгДалее рассчитываем аналогично, результаты расчетов сводим в таблицу 2. Таблица 2 – Значения энтальпии продуктов сгорания
По данным этой таблицы строим график q – Т (рисунок 1). 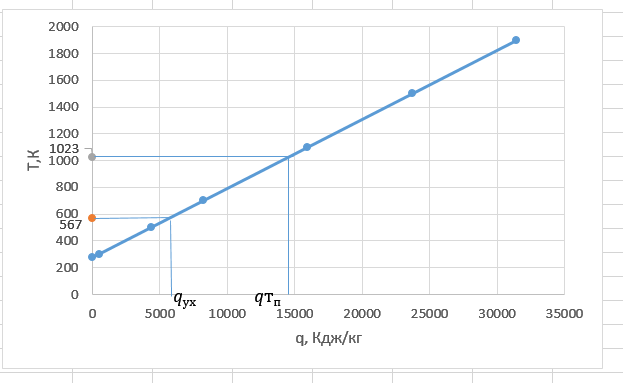 Рисунок 1 – График зависимости энтальпии от температуры |