Нуклеотиды Соснин. 2. Что такое нуклеотид, что такое нуклеозид. Нуклеотиды
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
|
2. Что такое «нуклеотид», что такое «нуклеозид». Нуклеотиды – это природные соединения, состоящие из 3-х химически различных компонента: гетероциклического азотистого основания, моносахарида (пентозы) и остатока фосфорной кислоты. Так же можно сказать, что нуклеотиды – фосфорные эфиры нуклеозидов. Остаток фосфорной кислоты присоединён к 5'-углеродному атому пентозы (5'-фосфоэфирная связь). В зависимости от числа имеющихся в молекуле остатков фосфорной кислоты различают нуклеозидмонофосфаты (НМФ), нуклеозиддифосфаты (НДФ), нуклео-зидтрифосфаты (НТФ). Они служат мономерными единицами полимеров нуклеиновых кислот. Пентозы в нуклеотидах представлены либо рибозой (в составе РНК), либо дезоксирибозой (в составе ДНК). Нуклеозиды – это соединения, состоящие из остатков нуклеинового основания и углевода, связанных β – N - гликозидной связью. В зависимости от того, какой моносахарид входит в состав нуклеозида, их подразделяют на два вида - рибозиды и дезоксирибозиды. Нуклеозиды являются промежуточными соединениями в синтезе нуклеотидов, и в клетке в иных метаболических процессах не участвуют. 3. Структурные формулы пуриновых и пиримидиновых азотистых оснований. Нуклеиновые кислоты по своему строению относят к классу линейных полимеров. Остов нуклеиновой кислоты имеет одинаковое строение по всей длине молекулы и состоит из чередующихся групп - пентоза-фосфат-пентоза- (рис. 4-5). Вариабельными группами в полинуклеотидных цепях служат азотистые основания - пурины и пиримидины. В молекулы РНК входят аденин (А), урацил (U), гуанин (G) и цитозин (С), в ДНК - аденин (А), тимин (Т), гуанин (G) и цитозин (С). П 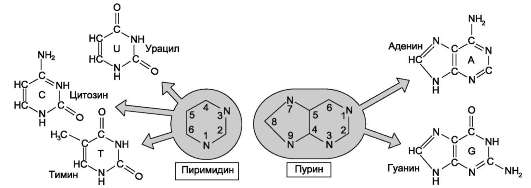 уриновые и пиримидиновые основания. уриновые и пиримидиновые основания.4 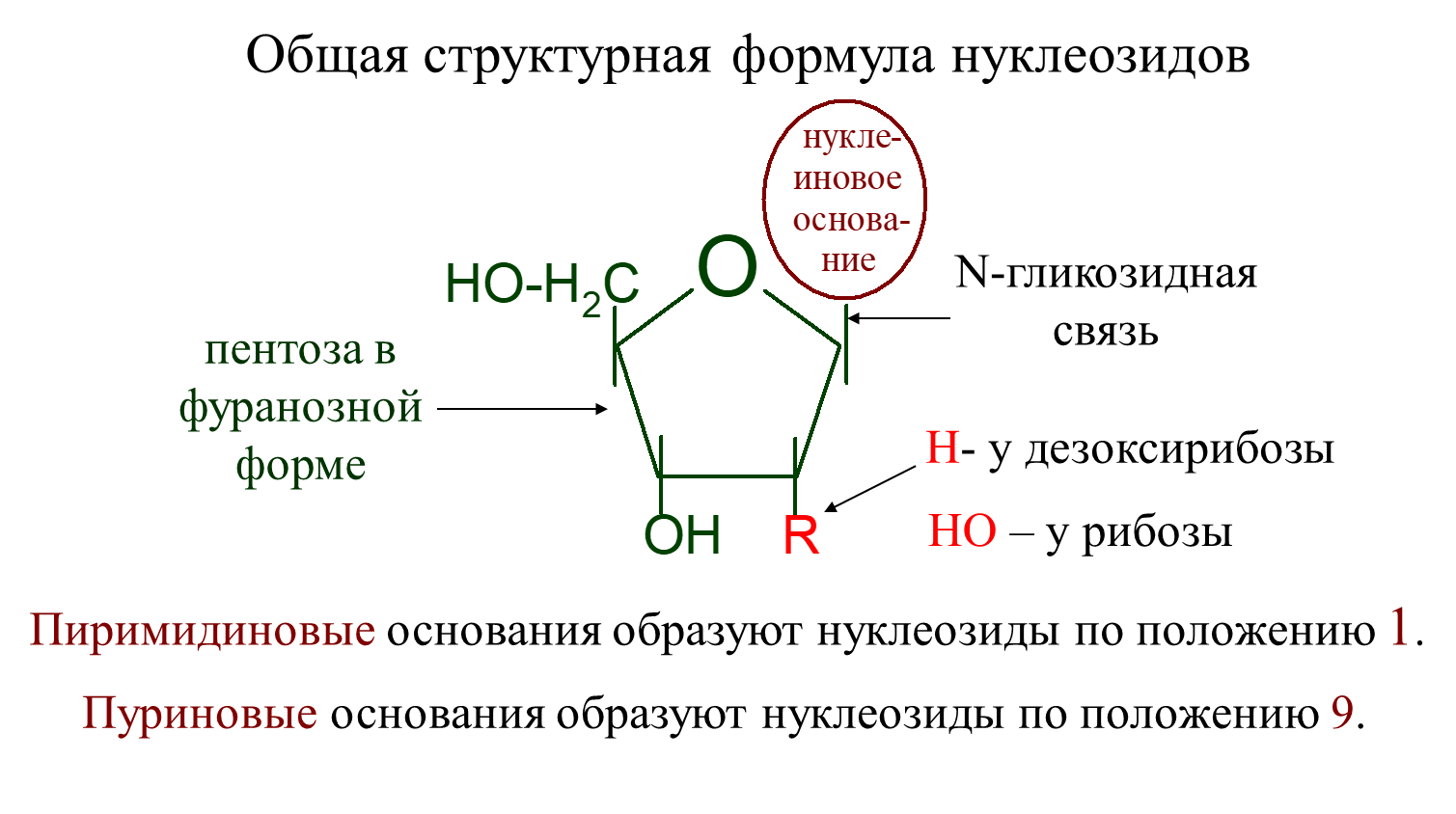 . Схема как происходит взаимодействие в структуре нуклеозида между атомами азотистого основания (пуриновым или пиримидиновым), пентозой, остатком фосфорной кислоты. . Схема как происходит взаимодействие в структуре нуклеозида между атомами азотистого основания (пуриновым или пиримидиновым), пентозой, остатком фосфорной кислоты. 5. Укажите роль свободных нуклеотидов. Свободные нуклеотиды (цамф и цгмф, атф, адф, фад, над) играют важную роль в энергетических и информационных внутриклеточных процессах, а также являются составляющими частями нуклеиновых кислот и многих коферментов. • Соединения цАМФ или цГМФ выполняют роль мессенджеров или вторых вестников в реализации клеткой внеклеточного регуляторного сигнала ( при действии глюкагона на гепатоциты в ускорении мобилизации гликогена играет существенную роль повышение концентрации цАМФ в этих клетках). • АТФ и ГТФ выступают в клетке как акумуляторы и переносчики энергии, высвобождающейся при биологическом окислении. • НАД+ , НАДФ+ , ФАД, ФМН являются переносчиками восстановительных эквивалентов в клетках ( промежуточными переносчиками протонов и электронов ). • Нуклеозидтрифосфаты (НТФ) используются в качестве субстратов синтеза ДНК и РНК, без которых невозможны образование белков и клеточная пролиферация. • Природа выбрала цикл АДФ-АТФ в качестве универсального механизма трансформации энергии окисления в энергию биосинтетических процессов. В некоторых биологических процессах и другие НТФ используются в качестве источника энергии. • Производные нуклеотидов служат донорами активных субстратов в синтезе гомо- и гетерополисахаридов, липидов и белков. Например: УДФ-глюкоза, УДФ-галактоза, ГДФ-манноза, УДФ-N-ацетилглюкозамин или ЦМФ-ацетилнейраминовая кислота принимают участие в синтезе гликогена и гликозаминогликанов; ЦДФ-холин - в синтезе фосфолипидов. • УДФ-глюкуроновая кислота, ФАФС, S-аденозилметионин - наиболее частые участники универсальной системы детоксикации, обеспечивающей последующее выведение ксенобиотиков (чужеродных веществ) и некоторых собственных метаболитов из организма. • АМФ входит в состав коферментов дегидрогеназ (NAD+, NADP+, FAD) и ацилирования (KoA). • С помощью циклических форм нуклеотидов (цAMФ, цГМФ) осуществляется передача в клетку сигналов гормонов, факторов роста, нейромедиаторов и некоторых других регуляторных молекул. 6. Представьте схему переваривания нуклеопротеинов в желудочно-кишечном тракте до продуктов, подлежащих всасыванию. Название ферментов. 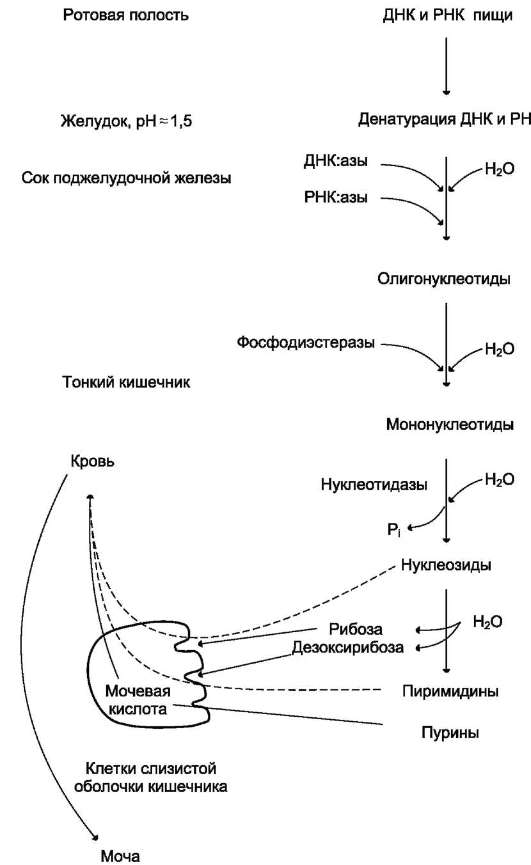      Неспецифические фосфатазы  Нуклеозидфосфорилаза    Ксантиноксидазы 7. Укажите пути использования в организме продуктов гидролиза нуклеопротеидов экзогенного и эндогенного происхождения. Пищевые пурины и пиримидины не являются незаменимыми пищевыми факторами и очень мало используются для синтеза нуклеиновых кислот тканей. Большая часть тех пуринов, что всосались, в энтероцитах под действием ксантиноксидазы - фермента, превращаются в мочевую кислоту, удаляющуюся с мочой. Пиримидиновые основания, не успевшие поступить в энтероциты, под действием микрофлоры кишечника расщепляются до NH3, CO2, β-аланина и β-аминоизобутирата. Введённые в кровь азотистые основания и нуклеозиды, а также основания и нуклеозиды, образующиеся в результате внутриклеточного разрушения нуклеиновых кислот, в небольшом количестве могут использоваться для повторного синтеза нуклеотидов по так называемым «запасным» путям. 8. Запишите в тетради схему: «Источники атома углерода и азота в ядре пурина» В формировании кольца принимают участие : СО2 Аминокислоты: Асп, Гли, Глн Два одноуглеродных производных тетрагидрофолата: метенилтетрагидрофолат и формил-тетрагидрофолат. 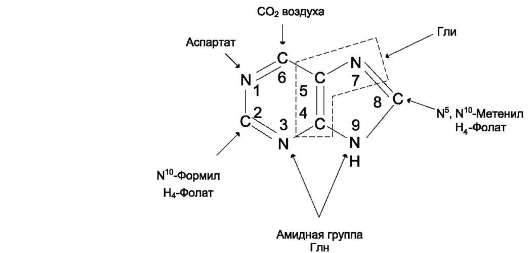 9. Запишите в тетради этапы биосинтеза пуриновых нуклеотидов de novo, укажите ключевые ферменты процесса, значение ФРДФ. Регуляция синтеза пуриновых нуклеотидов. Необходимой предпосылкой для биосинтеза нуклеотидов является синтез активной формы рибоза-5-фосфата. Источниками рибозо-5-фосфата могут быть: пентозофосфатный путь превращения глюкозы или катаболизм нуклеозидов, в ходе которого под действием нуклеозидфосфорилазы первоначально образуется рибозо-1-фосфат, а затем с помощью соответствующей мутазы фосфатный остаток переносится в 5-положение. З 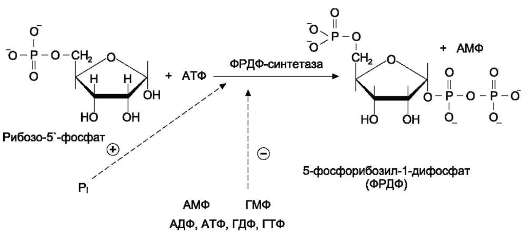 атем, за счёт переноса β,γ-пирофосфатного остатка ATФ на рибозо-5-фосфат в реакции, катализируемой ФРДФ-синтетазой, образуется Фосфорибозилдифосфат (ФРДФ). ФРДФ занимает центральное место в синтезе как пуриновых, так и пиримидиновых нуклеотидов, а также используется на образование пуриновых нуклеотидов по «запасному» пути и в синтезе нуклеотидных коферментов. атем, за счёт переноса β,γ-пирофосфатного остатка ATФ на рибозо-5-фосфат в реакции, катализируемой ФРДФ-синтетазой, образуется Фосфорибозилдифосфат (ФРДФ). ФРДФ занимает центральное место в синтезе как пуриновых, так и пиримидиновых нуклеотидов, а также используется на образование пуриновых нуклеотидов по «запасному» пути и в синтезе нуклеотидных коферментов.           П П ервая специфическая реакция образования пуриновых нуклеотидов - перенос амидной группы Глн на ФРДФ с образованием 5-фосфорибозил-1-амина (рис. 10-4). Эту реакцию катализирует фермент амидофосфорибозилтрансфераза. При этом формируется β-Ν-гликозидная связь. ервая специфическая реакция образования пуриновых нуклеотидов - перенос амидной группы Глн на ФРДФ с образованием 5-фосфорибозил-1-амина (рис. 10-4). Эту реакцию катализирует фермент амидофосфорибозилтрансфераза. При этом формируется β-Ν-гликозидная связь. 1 Ключевые ферменты процесса  2 Амидофосфорибозилтрансфераза  3 GAR – синтаза  4 Формилтрансфераза  5 FGAR - амидотрансфераза  6 FGAM – циклаза (AIR – синтетаза)  7 AIR – карбоксилаза  8 SAICAR – синтетаза  9 SAICAR – лиаза  10 Формилтрансфераза IMP – синтаза 10. Запишите в тетради значение резервного (запасного) пути синтеза пуриновых нуклеотидов, укажите ключевые ферменты процесса Огромные затраты энергии для синтеза пуриновых нуклеотидов denovo не способны полностью обеспечить субстратами синтез нуклеиновых кислот в период гаструляции и раннего роста ребёнка. Потребность в большом количестве нуклеотидов привела к развитию «запасных» путей синтеза этих «дорогих» молекул. Наибольшее значение в этом процессе имеют ферменты, осуществляющие превращение пуринов в мононуклеотиды с использованием ФРДФ как донора остатка фосфорибозы. ФРДФ-зависимое фосфорибозилирование пуринов катализируют 2 фермента. Аденинфосфорибозилтрансфераза, ответственная за образование АМФ. Гипоксантин-гуанинфосфорибозилтрансфераза, катализирующая образование ИМФ и ГМФ из гипоксантина и гуанина соответственно.  Однако в организме при любых ситуациях этот путь синтеза пуриновых нуклеотидов, получивший название «путь спасения», имеет вспомогательное значение. Однако в организме при любых ситуациях этот путь синтеза пуриновых нуклеотидов, получивший название «путь спасения», имеет вспомогательное значение.       1 1 1. Запишите в тетради схему катаболизма пуриновых нуклеотидов до мочевой кислоты, укажите промежуточные метаболиты, ферменты, конечный продукт. 1. Запишите в тетради схему катаболизма пуриновых нуклеотидов до мочевой кислоты, укажите промежуточные метаболиты, ферменты, конечный продукт. 12. Укажите нормальный показатель содержания мочевой кислоты в сыворотке крови человека и в моче. Что такое гиперурикемия и уратурия. Причины изменения содержания мочевой кислоты в биологических жидкостях. В сыворотке крови в норме содержание мочевой кислоты составляет 0,15-0,47 ммоль/л или 3-7 мг/дл. В моче 1,48 – 4,43 ммоль/сут или 250 – 750 мг/сут. Ежесуточно из организма выводится от 0,4 до 0,6 г мочевой кислоты и уратов. Когда в плазме крови концентрация мочевой кислоты превышает норму, то возникает гиперурикемия. Присутствие солей мочевой кислоты в моче носит название уратурия или мочекислый диатез. Появление уратов в моче является индикатором избытка в организме солей мочевой кислоты. Вследствие гиперурикемии может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов, или тофусов. Как правило, подагра генетически детерминирована и носит семейный характер. Она вызвана нарушениями в работе ФРДФ синтетазы или ферментов «запасного» пути: гипоксантин-гуанинили аденинфосфорибозил-трансфераз. Гипоксантин-гуанин фосфорибозилтрансфераза катализирует реакцию превращения гуанина и гипоксантина в соответствующие нуклеотиды. Обнаружены полиморфные варианты гипоксантин-гуанинфосфорибозил-трансферазы со сниженной ферментативной активностью, что: • уменьшает повторное использование пуриновых оснований, и они превращаются в мочевую кислоту; • увеличивает синтез пуриновых нуклеотидов de novo из-за слабого использования ФРДФ в реакциях реутилизации и увеличения его концентрации в клетке. Адениловые и гуаниловые нуклеотиды образуются в количествах, превышающих потребности клеток, а это способствует усилению их катаболизма, повышение продукции мочевой кислоты. Активность ФРДФ синтетазы, катализирующей образование ФРДФ, строго контролируется пуриновыми нуклеотидами. Мутации в гене ФРДФ синтетазы привели к появлению полиморфных вариантов фермента, которые характеризуются аномальным ответом на обычные регуляторные факторы: концентрацию рибозо-5-фосфата и пуриннуклеотидов. Как правило, наблюдается суперактивация фермента. Пуриновые нуклеотиды синтезируются со скоростью, почти независимой от нужд клетки. Это вызывает ингибирование запасных «путей спасения», усиление катаболизма избыточного количества нуклеотидов, повышение продукции мочевой кислоты. Одна из форм гликогеноза - болезнь Гирке (недостаточностью глюкозо-6-фосфатазы), сопутствующей ей патологией является подагра. Снижение способности печени секретировать глюкозу в кровь увеличивает использование глюкозо-6-фосфата в пентозофосфатном пути. Образуются большие количества рибозо-5-фосфата, которые могут стимулировать избыточный синтез, а следовательно, и катаболизм пуриновых нуклеотидов, повышение продукции мочевой кислоты. 13. Укажите причину развития и клинические проявления подагры и синдрома Леша-Нихена. Принципы лечения метаболических нарушений. Вследствие гиперурикемии может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов, или тофусов. Как правило, подагра генетически детерминирована и носит семейный характер. Она вызвана нарушениями в работе ФРДФ синтетазы или ферментов «запасного» пути: гипоксантин-гуанинили аденинфосфорибозил-трансфераз. Гипоксантин-гуанин фосфорибозилтрансфераза катализирует реакцию превращения гуанина и гипоксантина в соответствующие нуклеотиды. Обнаружены полиморфные варианты гипоксантин-гуанинфосфорибозил-трансферазы со сниженной ферментативной активностью, что: • уменьшает повторное использование пуриновых оснований, и они превращаются в мочевую кислоту; • увеличивает синтез пуриновых нуклеотидов de novo из-за слабого использования ФРДФ в реакциях реутилизации и увеличения его концентрации в клетке. Адениловые и гуаниловые нуклеотиды образуются в количествах, превышающих потребности клеток, а это способствует усилению их катаболизма, повышение продукции мочевой кислоты. Синдром Лёша-Нихена - тяжёлая форма гиперурикемии, которая наследуется как рецессивный признак, сцепленный с Х-хромосомой, и проявляется только у мальчиков. Болезнь вызвана полным отсутствием активности гипоксантин-гуанинфосфорибозилтрансферазы и сопровождается гиперурикемией с содержанием мочевой кислоты от 9 до 12 мг/дл, что превышает растворимость уратов при нормальном рН плазмы. Экскреция мочевой кислоты у больных с синдромом Лёша-Нихена превышает 600 мг/сут и требует для выведения этого количества продукта не менее 2700 мл мочи. Основным препаратом, используемым для лечения гиперурикемии, является аллопуринол - структурный аналог гипоксантина. Аллопуринол оказывает двоякое действие на обмен пуриновых нуклеотидов: • ингибирует ксантиноксидазу и останавливает катаболизм пуринов на стадии образования гипоксантина, растворимость которого почти в 10 раз выше, чем мочевой кислоты. Действие препарата на фермент объясняется тем, что сначала он, подобно гипоксантину, окисляется в гидроксипуринол, но при этом • остаётся прочно связанным с активным центром фермента, вызывая его инактивацию; с другой стороны, будучи псевдосубстратом, аллопуринол может превращаться в нуклеотид по «запасному» пути и ингибировать ФРДФ синтетазу и амидофосфорибозил-трансферазу, вызывая торможение синтеза пуринов denovo.При лечении аллопуринолом детей с синдромом Лёша-Нихена удаётся предотвратить развитие патологических изменений в суставах и почках, вызванных гиперпродукцией мочевой кислоты, но препарат не излечивает аномалии в поведении, неврологические и психические расстройства. 14. Запишите в тетради этапы биосинтеза пиримидиновых нуклеотидов de novo, укажите ключевые ферменты процесса, регуляция синтеза пиримидиновых нуклеотидов. В отличие от синтеза пуринов, где формирование гетероциклического основания осуществляется на остатке рибозо-5-фосфата, пиримидиновое кольцо синтезируется из простых предшественников: глутамина, СО2 и аспарагиновой кислоты и затем связывается с рибозо-5-фосфатом, полученным от ФРДФ. Процесс протекает в цитозоле клеток. Синтез ключевого пиримидинового нуклеотида - УМФ идёт с участием 3 ферментов, 2 из которых полифункциональны. У млекопитающих ключевой, регуляторной реакцией в синтезе пиримидиновых нуклеотидов является синтез карбамоилфосфата из глутамина, СО2 и АТФ, в реакции катализируемой карбамоилфосфатсинтетазой II (КФС II), которая протекает в цитозоле клеток.                             АДФ НДФ - киназа АДФ УТФ + АТФ НМФ - киназа УДФ АТФ + Регуляторным ферментом в синтезе пиримидиновых нуклеотидов является полифункциональный КАД-фермент. УМФ и УТФ аллостерически ингибируют, а ФРДФ активирует его карбамоилсинтетазную активность, тогда как активность аспартаттранскарбамоилазного домена ингибирует ЦТФ, но активирует АТФ. КАД-фермент катализирует реакции 1, 2, 3; дигидрооротатдегидрогеназа - реакцию 4; УМФ синтетаза - реакции 5 и 6; НМФ киназа - реакцию 7; НДФ киназа - реакцию 8; ЦТФ синтетаза - реацию 9.  Этот способ регуляции позволяет предотвратить избыточный синтез не только УМФ, но и всех других пиримидиновых нуклеотидов и обеспечить сбалансированное образование всех четырёх основных пуриновых и пиримидиновых нуклеотидов, необходимых для синтеза РНК.  15. Запишите в тетради значение резервного (запасного) пути синтеза пиримидиновых нуклеотидов, укажите ключевые ферменты процесса |
