бав ответы. 2. Рацемизация аминокислот, механизмы рацемизации (под действием оснований, кислот и по оксазолоновому механизму). Методы разделения рацематов аминокислот (механическое разделение, химические, ферментативные и хроматографические методы)
 Скачать 2.04 Mb. Скачать 2.04 Mb.
|
|
2. Рацемизация аминокислот, механизмы рацемизации (под действием оснований, кислот и по оксазолоновому механизму). Методы разделения рацематов аминокислот (механическое разделение, химические, ферментативные и хроматографические методы). Рацемизация-это химическая реакция, которая превращает аминокислоту в ее альтернативный энантиомер или зеркальную форму. Механизмы Прямая енолизация по оснОвному механизму (играет значительную роль) 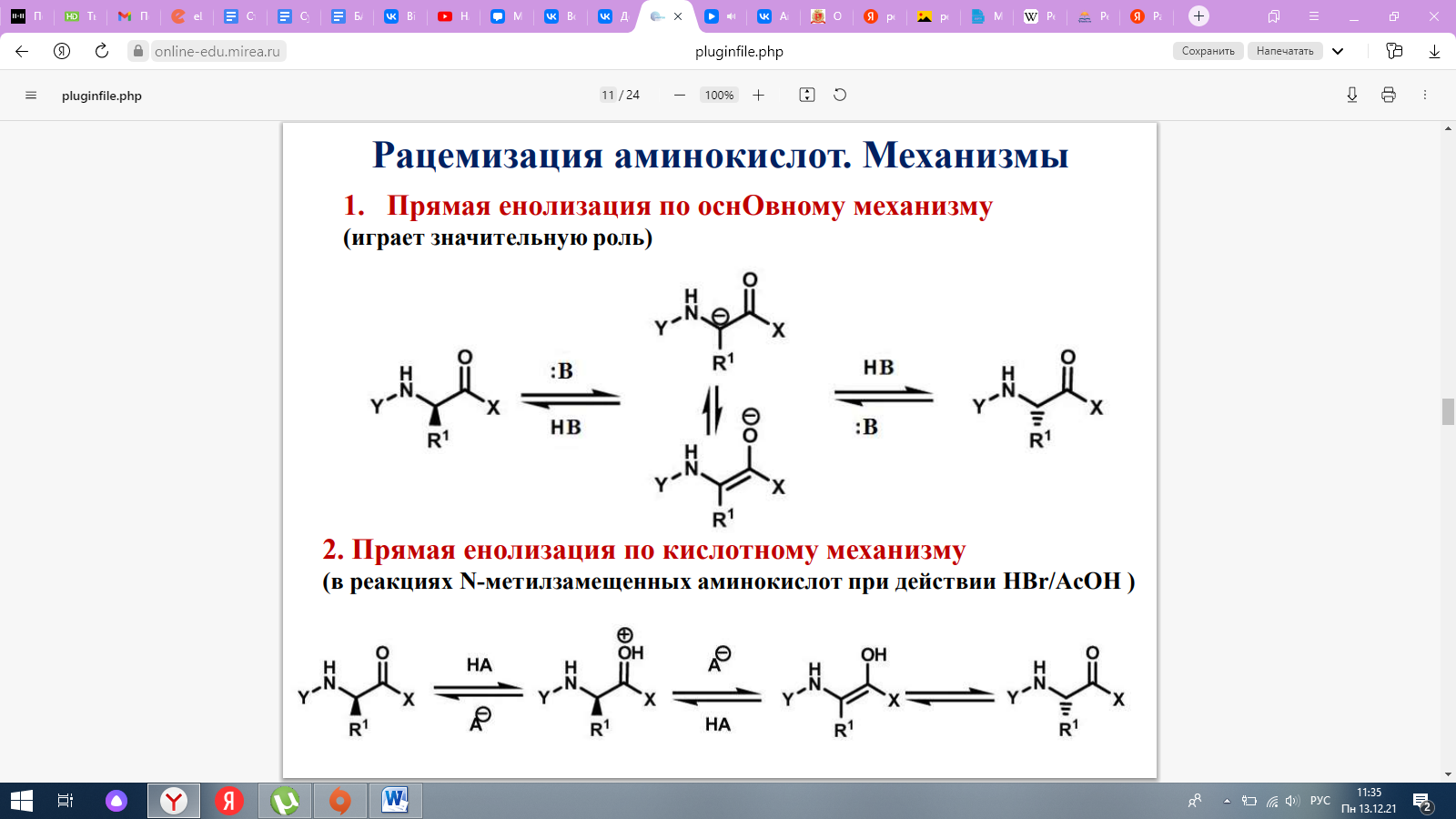 Прямая енолизация по кислотному механизму (в реакциях N-метилзамещенных аминокислот при действии HBr/AcOH ) 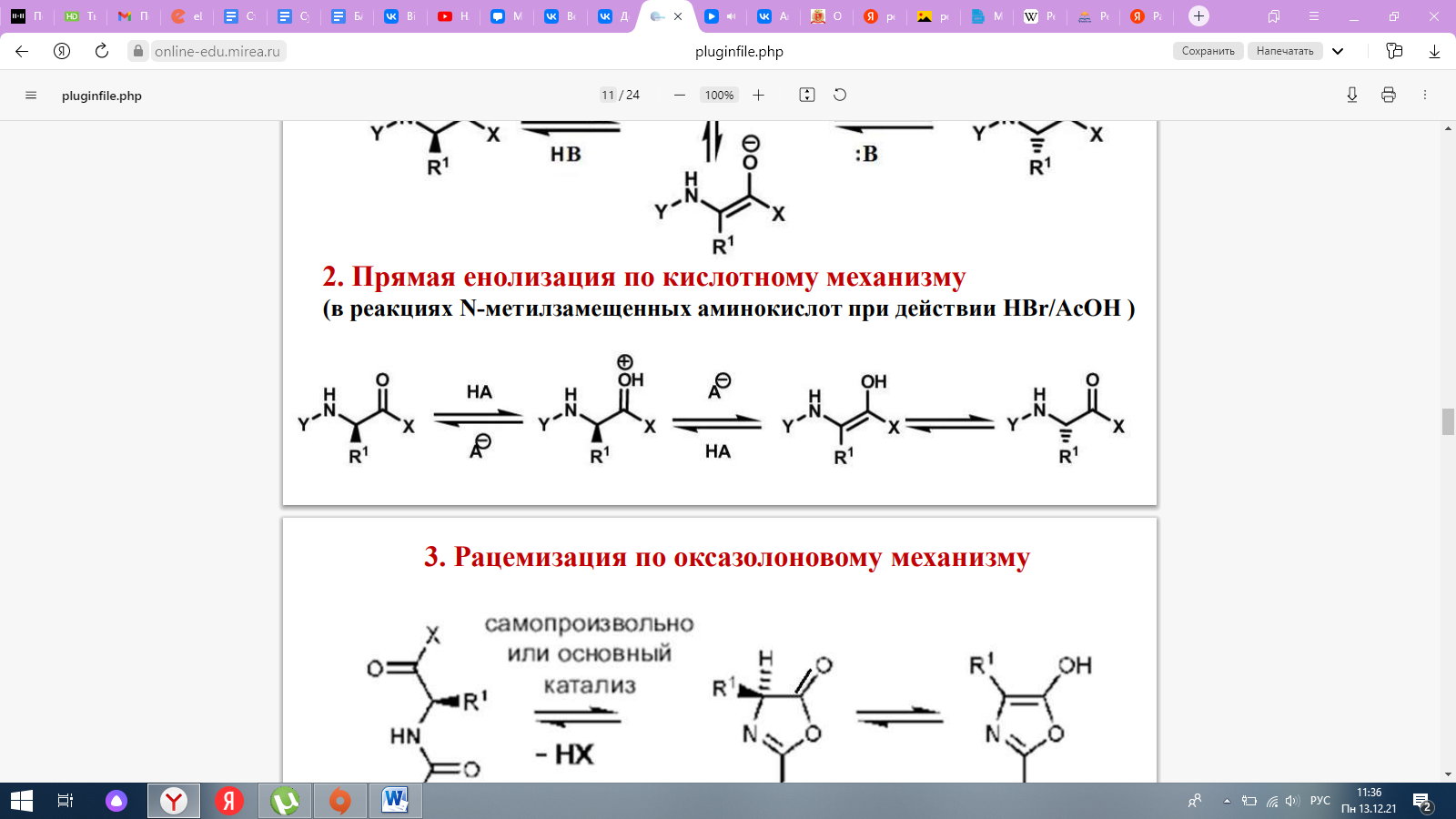 Рацемизация по оксазолоновому механизму 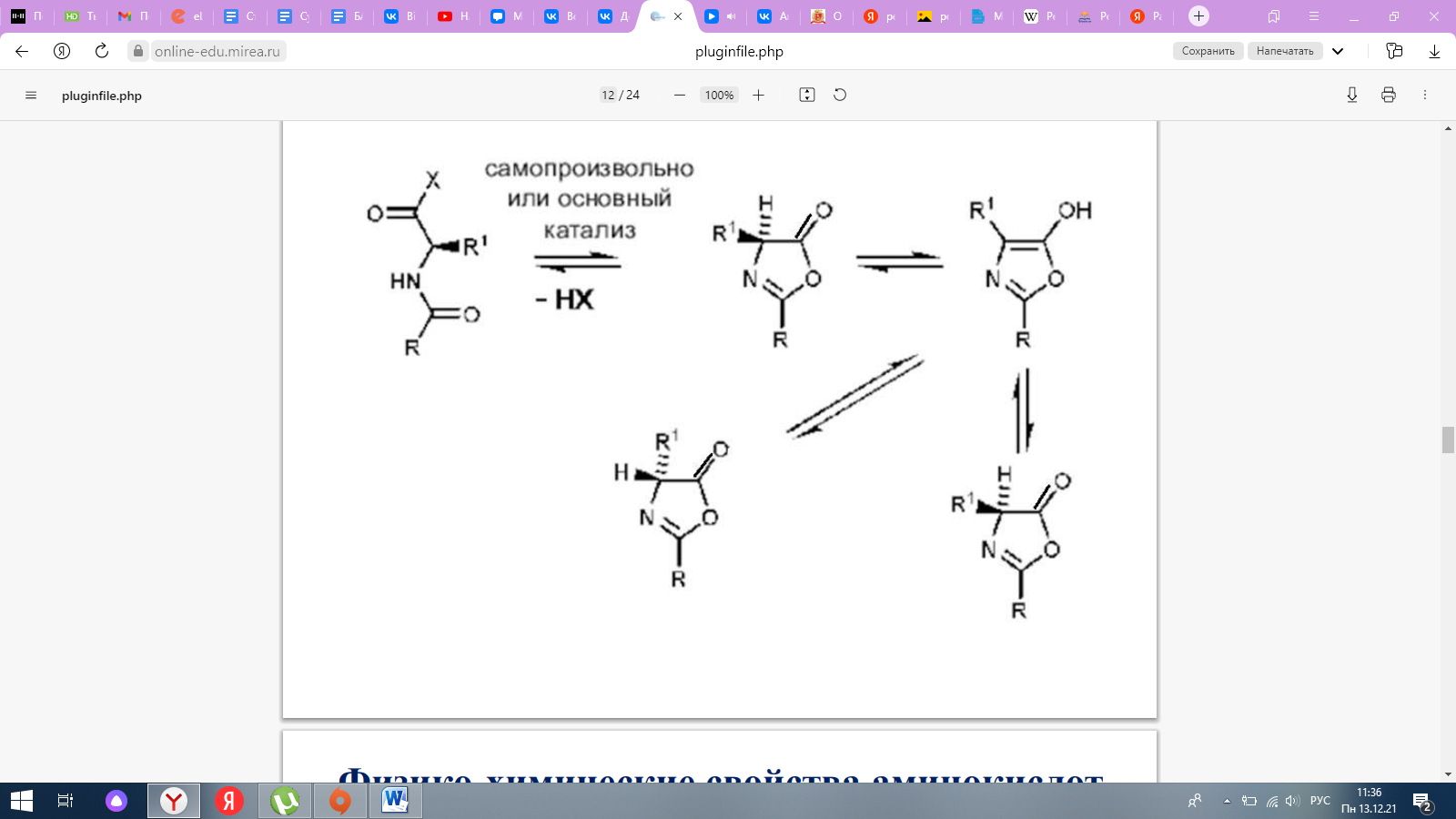 Методы разделения рацематов Механическое разделение. В некоторых случаях при кристаллизации из пересыщенных растворов образуются не смешанные кристаллы D,L-энантиомеров, а эвтектика из кристаллов D- и L-изомеров, так что энантиомеры можно отделить механическим отбором. В ряду аминокислот применение этого метода ограничено, так как только аспарагин, глутаминовая кислота и треонин выпадают в виде хорошо образованных кристаллов. Практическое значение имеет метод затравки: в пересыщенный раствор аминокислоты вводят кристаллы D- или L-энантиомера соответствующей аминокислоты. Выкристаллизовывающаяся аминокислота имеет такую же стереоконфигурацию, как добавленная затравка. Этот метод успешно применяется для разделения глутаминовой кислоты, гистидина, треонина, аспарагиновой кислоты, аспарагина и глутамина. Химические методы. Основаны на образовании диастереоизомерных солей с оптически активными вспомогательными веществами и разделении их фракционной кристаллизацией. Для образования солей с N-ацил(или N-алкил)- аминокислотами применяют алкалоиды α-фенилэтиламин, фенхиламин, хлорамфеникол. Для образования солей с такими производными аминокислот, как эфиры, амиды, нитрилы и гидразиды, в качестве оптически активных вспомогательных веществ используют винную кислоту, дибензоил-Dвинную кислоту и D-камфорсульфокислоту. Успех химического расщепления зависит от вида и количества применяемого растворителя, температуры кристаллизации и легкости отщепления вспомогательного вещества от диастереомерной соли. Ферментативные методы. Различают три направления: Селективное окисление или декарбоксилирование энантиомеров DLаминокислот специфическими ферментами. Применяется ограниченно для получения специфически меченных энантиомеров. Из экономических соображений вместо изолированных оксидаз и карбоксилаз вводят микроорганизмы, которые имеют необходимые системы ферментов и могут использовать в своем обмене только 1 антипод (обычно L-форму). Катализируемый ферментами асимметрический синтез производных аминокислот. Используют стереоспецифическое образование анилидов и фенилгидразидов N-ациламинокислот из N-ацил-DL-аминокислот и анилина или фенилгидразина, катализируемое папаином или пепсином. Метод применим для расщепления аминокислот с двумя центрами хиральности. Ферментативный гидролиз α-амино или α-карбоксизамещенных производных аминокислот. Благодаря использованию фиксированных на носителе микробных ферментов (в основном это системы аминоацилаза – ДЭАЭ-сефадекс) этот процесс был автоматизирован. Используется для промышленного получения ряда L-аминокислот: Phe, Val, Met, Trp. Хроматографические методы. Если рацемичеcкую смесь хроматографировать на колонке, заполненной хиральными веществами, энантиомеры должны проходить с разными скоростями и, следовательно, их можно разделить. Можно использовать бумажную, колоночную, газовую и жидкостную хроматографию. 28. Химико-ферментативный синтез ДНК.  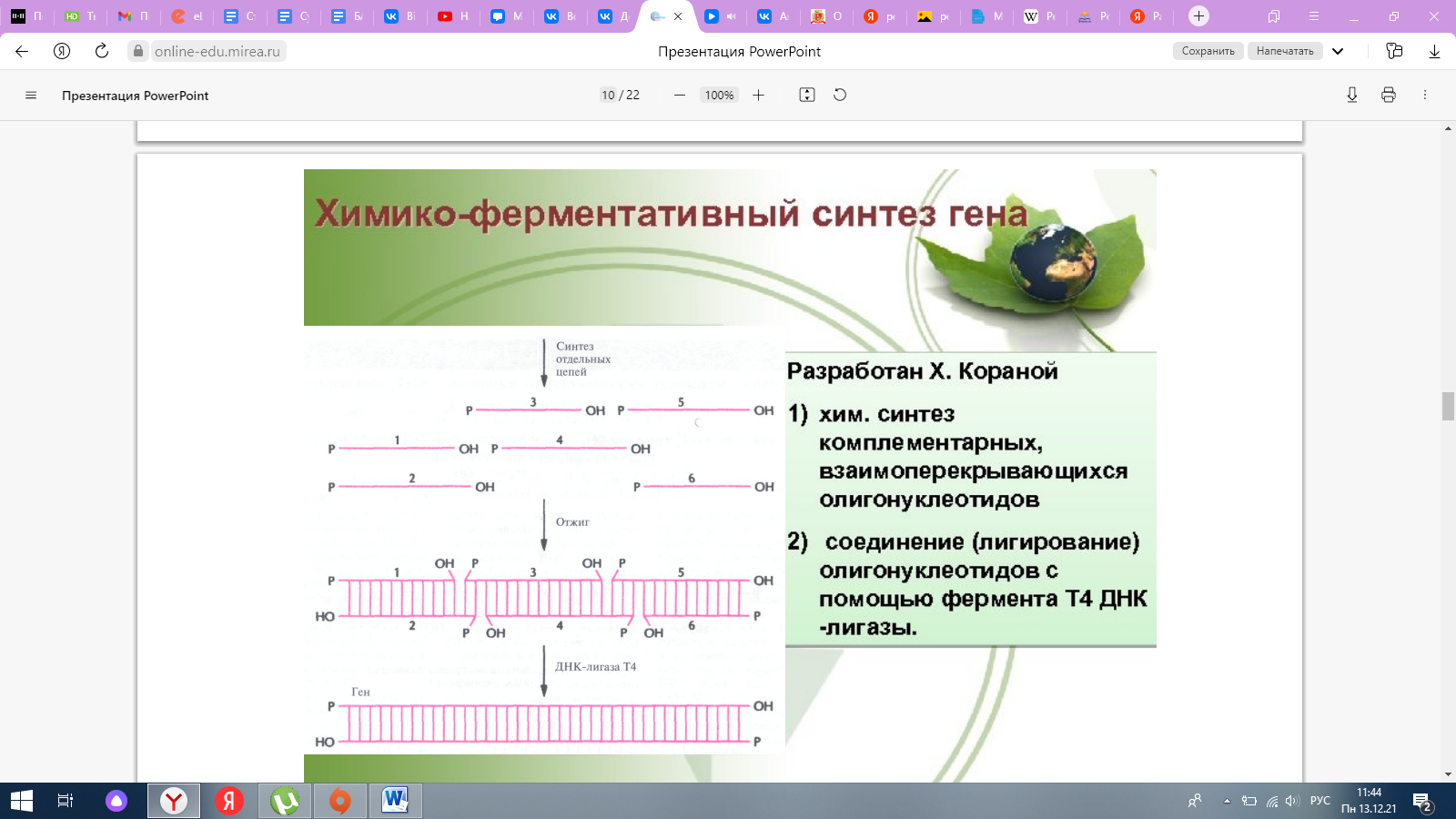 Химико-ферментативный синтез генов. Метод включает химический синтез коротких одноцепочечных фрагментов ДНК (олигонуклеотидов) за счет поэтапного образования эфирных связей между нуклеотидами и сшивку олигонуклеотидов посредством ДНК-лигазы с образованием двухцепочечных полинуклеотидов. Это позволяет избежать липких последовательностей в ДНК, а также получать разнообразные участки узнавания, регуляторные последовательности и т. д. Применимость метода ограничена недостатком информации о нуклеотидной последовательности генов. Такая последовательность воссоздается на основе знания о цепочке аминокислотных остатков в кодируемом белке. (из инета). |
