2. Строение и функции белков
 Скачать 0.73 Mb. Скачать 0.73 Mb.
|
|
Глюкозо-1-фосфат + УТФ < = > УДФ-глюкоза +Пирофосфат. На второй стадии – стадии образования гликогена – происходит перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена («затравочное» количество). При этом образуется α-(1–>4)-связь между первым атомом углерода добавляемого остатка глюкозы и 4-гидроксильной группой остатка глюкозы цепи. Этареакция катализируется ферментом гликогенсинтазой. Необходимо еще раз подчеркнуть, что реакция, катализируемая гликогенсинтазой, возможна только при условии, что полисахаридная цепь уже содержит более 4 остатков 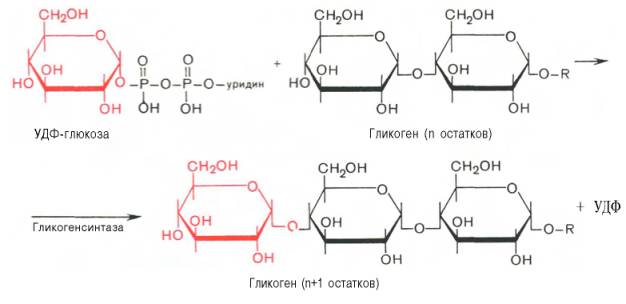 46. Влияние гормонов на синтез и распад гликогена. Метаболизм гликогена в печени, мышцах и других клетках регулируется несколькими гормонами, одни из которых активируют синтез гликогена, а другие – распад гликогена. При этом в одной клетке не могут идти одновременно синтез и распад гликогена – это противоположные процессы с совершенно с разными задачами. Синтез и распад исключают друг друга или, по-другому, они реципрокны. Активность ключевых ферментов метаболизма гликогена гликогенфосфорилазы игликогенсинтазы изменяется в зависимости наличия в составе фермента фосфорной кислоты – они активны либо в фосфорилированной, либо в дефосфорилированной форме. Присоединение фосфатов к ферменту производят протеинкиназы, источником фосфора является АТФ: фосфорилаза гликогена активируется после присоединения фосфатной группы, синтаза гликогена после присоединения фосфата инактивируется. Скорость фосфорилирования указанных ферментов повышается после воздействия на клеткуадреналина, глюкагона и некоторых других гормонов. В результате адреналин и глюкагон вызывают гликогенолиз, активируя фосфорилазу гликогена.Например,во время мышечной работы адреналин вызывает фосфорилирование внутримышечных ферментов обмена гликогена. В результате фосфорилаза гликогена активируется, синтаза инактивируется. В мышце происходит распад гликогена, образуется глюкоза для обеспечения энергией мышечного сокращения.При голодании в ответ на снижение глюкозы крови из поджелудочной железы секретируетсяглюкагон. Он воздействует на гепатоциты и вызывает фосфорилирование ферментов обмена гликогена, что приводит к гликогенолизу и повышению глюкозы в крови. Способы активации синтазы гликогена Аллостерическая активация гликогенсинтазы осуществляется глюкозо-6-фосфатом. Еще одним способом изменения ее активности является химическая (ковалентная)модификация. При присоединении фосфата гликогенсинтаза прекращает работу, т.е. она активна в дефосфорилированном виде. Удаление фосфата от ферментов осуществляютпротеинфосфатазы. Активатором протеинфосфатаз выступает инсулин – в результате он повышает синтез гликогена. Вместе с этим, инсулин и глюкокортикоиды ускоряют синтез гликогена, увеличиваяколичество молекул гликогенсинтазы. Способы активации фосфорилазы гликогена Скорость гликогенолиза лимитируется только скоростью работы фосфорилазы гликогена. Ее активность может изменяться тремя способами:ковалентная модификация,кальций-зависимая активация,аллостерическая активация с помощью АМФ. Кальций-зависимая активация Некоторые гормоны влияют на углеводный обмен посредством кальций-фосфолипидного механизма. Активация ионами кальция заключается в активации киназы фосфорилазы не протеинкиназой, а ионами Ca2+ и кальмодулином. Этот путь работает при инициации кальций-фосфолипидного механизма. Такой способ оправдывает себя, например, при мышечной нагрузке, если гормональные влияния через аденилатциклазу недостаточны, но в цитоплазму под влиянием нервных импульсов поступают ионы Ca2+. 47.Нарушение углеводного обмена. Сахарный диабет. При некоторых состояниях можно наблюдать повышение содержания глюкозы в крови - гипергликемию, а также понижение концентрации глюкозы – гипогликемию. Сахарный диабет. В регуляции гликолиза и глюконеогенеза большую роль играет инсулин. При недостаточности содержания инсулина возникает заболевание, которое носит название «сахарный диабет»: повышается концентрация глюкозы в крови (гипергликемия), появляется глюкоза в моче (глюкозурия) и уменьшается содержание гликогена в печени. Мышечная ткань при этом утрачивает способность утилизировать глюкозу крови. В печени при общем снижении интенсивности биосинтетических процессов: биосинтеза белков, синтеза жирных кислот из продуктов распада глюкозы - наблюдается усиленный синтез ферментов глюконеогенеза. При введении инсулина больным диабетом происходит коррекция метаболических сдвигов: нормализуется проницаемость мембран мышечных клеток для глюкозы, восстанавливается соотношение между гликолизом и глюконеогенезом. Инсулин контролирует эти процессы на генетическом уровне как индуктор синтеза ключевых ферментов гликолиза: гексокиназы, фосфофруктокиназы и пируваткиназы. Инсулин также индуцирует синтез гликогенсинтазы. Одновременно инсулин действует как репрессор синтеза ключевых ферментов глюконеогенеза. Следует отметить, что индукторами синтеза ферментов глюконеогенеза служат глюкокортикоиды. Развитие гипергликемии при диабете можно рассматривать также как результат возбуждения метаболических центров в ЦНС импульсами с хе-морецепторов клеток, испытывающих энергетический голод в связи с недостаточным поступлением глюкозы в клетки ряда тканей. Роль системы фруктозо-2,6-бисфосфата в регуляции метаболизма углеводов, а также нарушения ее функционирования при сахарном диабете. 48. Гликогенозы и агликогенозы. Гликогеновые болезни – это наследственные заболевания, обусловленные недостаточностью каких-либо ферментов, отвечающих за метаболизм гликогена. Могут быть нарушены обе стороны обмена: как синтез гликогена, так и его распад. Средняя частота встречаемости составляет 1:40000. Гликогенозы Ранее гликогенозы классифицировались по номерам, однако в связи с открытием новых вариантов этих болезней появилось много разночтений. В настоящее время гликогенозы делят по патогенетическому признаку на печеночные, мышечные и смешанные формы. Следует отметить, что при гликогенозах количество гликогена не всегда изменено, изменения могут быть только в структуре его молекулы. Печеночные гликогенозы Самый частый гликогеноз I типа или болезнь фон Гирке обусловлен аутосомно-рецессивным дефектом глюкозо-6-фосфатазы. Из-за того, что этот фермент есть только в печени и почках, преимущественно страдают эти органы, и болезнь носит еще одно название –гепаторенальный гликогеноз. Даже у новорожденных детей наблюдаются гепатомегалия и нефромегалия, обусловленные накоплением гликогена не только в цитоплазме, но и в ядрах клеток. Кроме этого, активируется синтез липидов с возникновением стеатоза печени. Так как фермент необходим для дефосфорилирования глюкозо-6-фосфата с последующим выходом глюкозы в кровь, у больных отмечается гипогликемия и, как следствие, ацетонемия, метаболический ацидоз, ацетонурия. Гликогеноз III типа или болезнь Форбса-Кори или лимит-декстриноз – это аутосомно-рецессивный дефект амило-α1,6-глюкозидазы, "деветвящего" фермента, гидролизующего α1,6-гликозидную связь. Болезнь имеет более доброкачественное течение, и частота ее составляет примерно 25% от всех гликогенозов. Для больных характерна гепатомегалия, умеренная задержка физического развития, в подростковом возрасте возможна небольшая миопатия. Еще два печеночных гликогеноза – гликогеноз IV типа (болезнь Андерсена), связанный с дефектом ветвящего фермента и гликогеноз VI типа (болезнь Херса), связанный с дефицитом печеночной фосфорилазы гликогена встречаются довольно редко. Мышечные гликогенозы Для этой группы гликогенозов характерны изменения ферментов мышечной ткани. Это приводит к нарушению энергообеспечения мышц при физической нагрузке, к болям в мышцах, судорогам. Гликогеноз V типа (болезнь Мак-Ардля) – отсутствие мышечной фосфорилазы. При тяжелой мышечной нагрузке возникают судороги, миоглобинурия, хотя легкая работа не вызывает каких-либо проблем. Агликогенозы Агликогенозы – состояния, связанные с отсутствием гликогена. В качестве примера агликогеноза можно привести наследственный аутосомно-рецессивный дефицит гликоген-синтазы. Симптомами является резкая гипогликемия натощак, особенно утром, появляется рвота, судороги, потеря сознания. В результате гипогликемии наблюдается задержка психомоторного развития, умственная отсталость. Болезнь несмертельна при адекватном лечении (частое кормление), хотя и опасна. 49. Цикл Кребса Окисление ацетата дает много энергии Образующийся в ПВК-дегидрогеназной реакции ацетил-SКоА далее вступает в цикл трикарбоновых кислот (ЦТК, цикл лимонной кислоты, цикл Кребса). Кроме пирувата, в цикл вовлекаются кетокислоты, поступающие из катаболизма аминокислотили каких-либо иных веществ. Цикл трикарбоновых кислот Цикл протекает в матриксе митохондрий и представляет собой восемь последовательных реакций: связывание ацетила и оксалоацетата(щавелевоуксусной кислоты) с образованием лимонной кислоты, изомеризация лимонной кислоты и последующие реакции окисления с сопутствующим выделением СО2. После восьми реакций цикла вновь образуется оксалоацета. Основная роль ЦТК заключается в генерации атомов водорода для работы дыхательной цепи, а именно трех молекул НАДН и одной молекулы ФАДН2. Кроме этого, в ЦТК образуется одна молекула АТФ,сукцинил-SКоА, участвующий в синтезе гема, кетокислоты, являющиеся аналогами аминокислот – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой. 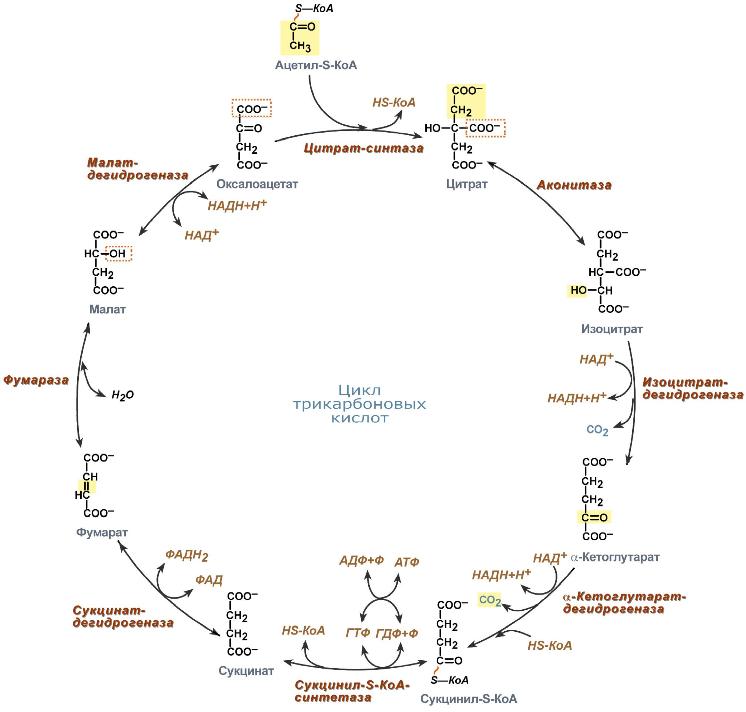 Регуляция цикла трикарбоновых кислот Регуляция цикла трикарбоновых кислотГлавным и основнымрегулятором ЦТК является оксалоацетат, а точнее его доступность. Наличие оксалоацетата вовлекает в ЦТК ацетил-SКоА и запускает процесс. Обычно в клетке имеется балансмежду образованием ацетил-SКоА (из глюкозы, жирных кислот или аминокислот) и количеством оксалоацетата. Источникомоксалоацетата являетсяглюкоза (синтез из пирувата в анаплеротической реакции), поступление из фруктовых кислотсамого цикла (яблочной, лимонной), образование из аспарагиновой кислоты в результатетрансаминирования. Примером существенной роли оксалоацетата служит активация синтеза кетоновых тел икетоацидоз плазмы крови при недостаточном количестве оксалоацетата в печени. Такое состояние наблюдается при инсулинзависимом сахарном диабете, при голодании, алкогольном отравлении или длительной физической нагрузке 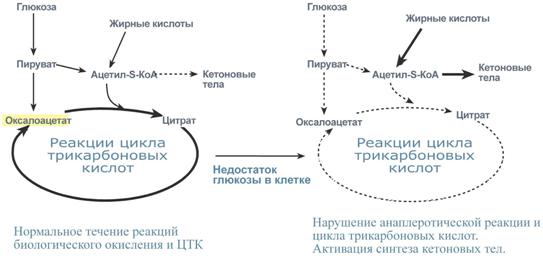 50. Глюконеогенез. Глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата,глицерола, кетокислотцикла Кребса и других кетокислот, из аминокислот. Все аминокислоты, кроме кетогенных лейцина и лизина, способны участвовать в синтезе глюкозы. Углеродные атомы некоторых из них – глюкогенных – полностью включаются в молекулу глюкозы, некоторых – смешанных – частично. Кроме получения глюкозы, глюконеогенез обеспечивает и уборку"шлаков" – лактата, постоянно образуемого в эритроцитах или при мышечной работе, и глицерола, являющегося продуктом липолиза в жировой ткани. Как известно, в гликолизесуществуют три необратимые реакции: пируваткиназная(десятая),фосфофруктокиназная(третья) и гексокиназная (первая). В этих реакциях происходит высвобождение энергии для синтеза АТФ. Поэтому в обратном процессе возникаютэнергетические барьеры, которые клетка обходит с помощью дополнительных реакций. Глюконеогенез включает все обратимые реакции гликолиза, и особые обходные пути, т.е. он не полностью повторяет реакции окисления глюкозы. Его реакции способны идти во всех тканях, кроме последней глюкозо-6-фосфатазной реакции, которая идет только в печениипочках. Поэтому, строго говоря, глюконеогенез идет только в этих двух органах. Обход десятой реакции гликолиза На этом этапе глюконеогенеза работают два ключевых фермента – в митохондрияхпируваткарбоксилаза и в цитозоле фосфоенолпируват-карбоксикиназа. В химическом плане обходной путь десятой реакции выглядит достаточно просто: 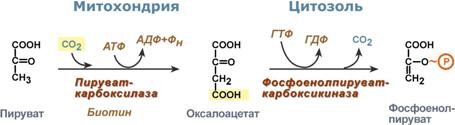 Упрощенный вариант обхода десятой реакции гликолиза Однако дело в том, что пируваткарбоксилазанаходится в митохондрии, афосфоенолпируват-карбоксикиназа – в цитозоле. Дополняет проблему непроницаемостьмитохондриальной мембраны для оксалоацетата. Зато через мембрану может пройти малат, предшественник оксалоацетата по ЦТК. Поэтому в реальности все выглядит более сложно: 1. В цитозоле пировиноградная кислота может появиться при окислении молочной кислоты и в реакции трансаминирования аланина. После этого пируват симпортом с ионами Н+, движущимися по протонному градиенту, проникает в митохондрии. В митохондрияхпируваткарбоксилаза превращает пировиноградную кислоту в оксалоацетат. Эта реакция идет в клетке постоянно, являясь анаплеротичской (пополняющей) реакцией ЦТК. 2. Далее оксалоацетат мог бы превратиться в фосфоенолпируват, но для этого сначала он должен попасть в цитозоль. Поэтому происходит реакция восстановления оксалоацетата в малат при участии малатдегидрогеназы.В результате малат накапливается, выходит в цитозоль и здесь превращается обратно в оксалоацетат. Повернуть малатдегидрогеназную реакцию ЦТК вспять позволяет избыток НАДН в митохондриях. НАДН поступает из β- окисления жирных кислот, активируемого в условиях недостаточности глюкозы в гепатоците. 3. В цитоплазме фосфоенолпируват-карбоксикиназа осуществляет превращение оксалоацетата в фосфоенолпируват, для реакции требуется энергия ГТФ. От молекулы отщепляется тот же углерод, что и присоединяется. 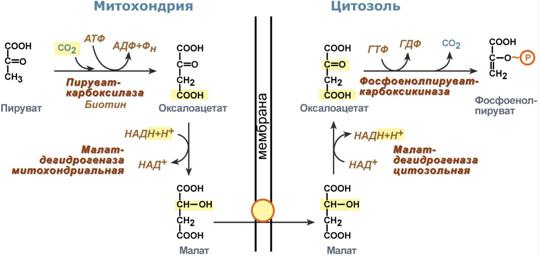 Обход десятой реакции гликолиза Обход третьей реакции гликолиза Второе препятствие на пути синтеза глюкозы – фосфофруктокиназная реакция – преодолевается с помощью фермента фруктозо-1,6-дифосфатазы. Этот фермент есть в почках, печени, поперечно-полосатых мышцах. Таким образом, эти ткани способны синтезировать фруктозо-6-фосфат и глюкозо-6-фосфат. 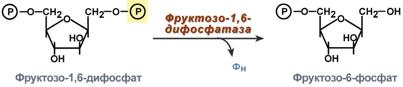 Обход третьей реакции гликолиза Обход первой реакции гликолиза Последняя реакция катализируется глюкозо-6-фосфатазой. Она имеется только в печени ипочках, следовательно, только эти ткани могут продуцировать свободную глюкозу. 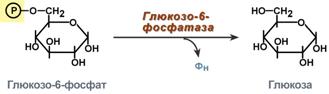 |
