6. Какие виды упаковки применяются для лекарственной формы таблетки
 Скачать 106.03 Kb. Скачать 106.03 Kb.
|
|
6. Какие виды упаковки применяются для лекарственной формы таблетки? Таблетки: пленочные контурные упаковки безъячейковая (стриповая) и ячейковая тара (блистер); банка из стекломассы с винтовой горловиной, металлические банки; пеналы; полимерные контейнеры с контролем первого вскрытия; пробирки пластмассовые, стеклянные; полимерные дозирующие контейнеры типа «Пуш-топ». Вторичные упаковоки: картонные пачки и коробки, куда помещаются в первичной упаковке таблетки. 13. Номенклатура капсулированных лекарств, выпускаемых в мягких и твердых желатиновых капсулах. Капсулированные антибиотики (ампициллин, окси-тетрациклин, фузидат натрия, хлорамфеникол, гризеофульвин, канамицин, линкомицин и др.), витаминные препараты (жир печени палтуса, витамин А, Д и др.), противосудорожные средства в капсулах (параметадион, триметадион, этоксуксимид, дифенилгидантоин и др.), антиаритмические средства (хинидин сульфат, прокаинамид гидрохлорид и др.), снотворные и седативные средства (барбамил, хлоралгидрат, люминал, этаминал-натрий и др.), транквилизаторы (хлордиазепоксид, элениум и др.), сосудосуживающие (эфедрин и др.), антигельминтные (тетрахлорэтилен), слабительные (диоктилсульфонксинат натрия), диуретики (триамтерен), обезболивающие (декстропропоксифен), гипохолестеринемические (хлофибрейт) и другие лекарственные средства. Особенно разнообразны комбинации аск с различными веществами, в том числе с аскорбиновой кислотой, атропином, барбитуратами, камфорой, порошком Довера, сульфатом натрия, фенацетином, эфедрином и др. Так,например, препарат «Alcaps» состоит из аспирина, фенобарбитала, аскорбиновой кислоты, эфедрина хлористоводородного (фирма Arlington); препарат «Paadon» содержит аск, фенобарбитал, алкалоиды белладонны, ацетофенетидин (фирма «Rorer»); препарат «Bellaturic» состоит из атропина сернокислого, барбитала, гиосциамина сернокислого, гиосцина бромистоводородного (фирма Entlcail); препарат «Semhyten» содержит рутин, аскорбиновую кислоту, маннитол, гексанит-рат, фенобарбитал, теофиллин (фирма Massengil.) 20. Чем отличается технология производства твердых и мягких желатиновых капсул методом погружения? Какие машины при этом применяются? Каковы их устройство и принцип работы? Метод «погружения». Сущность метода погружения заключается в том, что изготовление желатиновых оболочек производится с помощью металлических «макальных» рам со штифтами, отображающими форму капсул. Штифты погружают в расплав желатиновой массы и поднимают с вращательными движениями для равномерного распределения массы на штифтах, затем сушат твердые капсулы, подрезают у основания и снимают половинку капсулы — корпус или крышечку, которые комплектуют. При получении мягких мягких капсул желатиновую оболочку охлаждают, снимают с форм, наполняют масляными растворами лекарственных веществ и запаивают. В зависимости от различных модификаций отдельных механизмов и устройств, а также формы рам-держателей и их количества имеются разные конструкции машин, работающие по принципу погружения, выпускаемые фирмами «Colton», «Parke, Davis&Co», «Elanco», «Elli Lilli» (США), «Zanazi» (Италия), «Hofliger und Karg» (Германия), «Capsule Technology International» (Канада), которые отличаются формой рам - держателей со штифтами, их количеством, механизмами устройства. Установка состоит из следующих основных частей: сосуда для желатиновой массы (в термостатированном кожухе); погружающего механизма с формочками-штифтами; сушильной установки; — автоматического узла для подрезания, снятия и комплектования капсул. 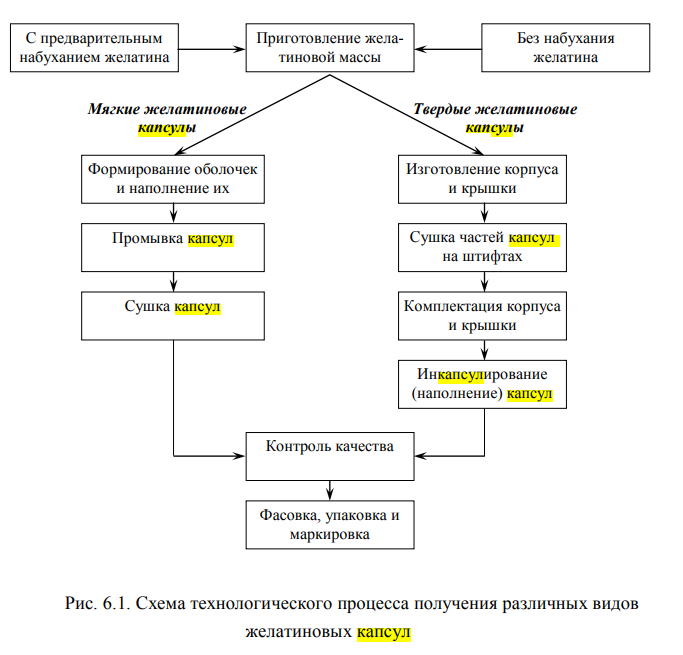 27. По каким показателям проводят оценку качества медицинских капсул? Какие требования предъявляются к медицинским капсулам согласно ГФ РК? Препараты в капсулах контролируют по следующим показателям качества: описание (внешний вид), идентификация, однородность массы, однородность содержания, сопутствующие примеси, растворимость, распадаемость, потеря массы при высушивании, микробиологическая чистота, количественное определение действующих веществ. Однородность содержания (2.9.6, В). Капсулы с содержанием действующего вещества менее 2 мг или менее 2 % от массы содержимого должны выдерживать испытание однородности содержания действующего вещества в единице дозированного лекарственного средства. Однородность массы (2.9.5). Капсулы должны выдерживать испытание однородности массы для единицы дозированного лекарственного средства. Испытание однородности массы не требуется, если испытание однородности содержания предусмотрено для всех действующих веществ. Растворение (2.9.3). Испытание может быть проведено для подтверждения соответствующего высвобождения действующего вещества или веществ, например, одним из способов, описанных в разделе «Тест «Растворение» для твердых дозированных форм». Если проводят испытание по показателю «Растворение», испытание «Распадаемость» не требуется. Распадаемость (2.9.1) Твердые капсулы должны вы Не держивать испытание распадаемости таблеток или капсул. Испытание считают выдержанным, если распались все 6 капсул. ХРАНЕНИЕ При температуре не выше 30 C МАРКИРОВКА На этикетке указывают название всех входящих в состав антимикробных консервантов. Там, где это необходимо, контейнеры для капсул должны соответствовать требованиям разделов «Материалы, используемые для производства контейнеров» (3.1 и подразделы) и «Контейнеры» (3.2¼ подразделы). Не по нашему ГФ Описание. Капсулы должны иметь гладкую поверхность без повреждений и видимых воздушных и механических включений. Их внешний вид должен соответствовать требованиям частных нормативным документам. Идентификация. Проводят определение наличия всех действующих веществ и антимикробных консервантов, входящих в состав препарата. Однородность массы в единице дозированного лекарственного средства. Допустимое отклонение не должно превышать 10 % от средней массы меньше 300 мг и 7,5 % для капсул со средней массой 300 мг и более. Данное испытание не распространяется на поливитаминные препараты и капсулы, содержащие микроэлементы. Однородность содержания. Препарат отвечает требованиям, если содержание не больше чем в одной однодозовой единице не выходит за пределы 85-115 %, а в каждой единице не более 75-125 % от среднего содержания в препарате. Содержание действующего вещества в капсуле. Если нет других указаний в частной статье, отклонение в содержании действующих веществ при до зировке менее 1 мг (±15%), от 1 мг до 10 мл (±10%), от 10 мг до 100 мг (±7,5%) и от 100 мг и более (±5%). В мягких капсулах, содержание которых представляет собой масла или масляные растворы, дополнительно контролируют кислотное и перекисное числа. Распадаемость. Твердые и мягкие капсулы должны выдерживать требования на распадаемость. Если нет других указаний в частных статьях, желудочно-растворимые капсулы должны распадаться в течение 30 минут, кишечно-растворимые – в течение 1 часа в растворе фосфатного буфера рН 6,8. Микробиологическая чистота. При производстве, упаковке, хранении и реализации капсул должны быть реализованы мероприятия, обеспечивающие необходимую микробиологическую чистоту в соответствии с требованиями. Упаковка и маркировка. Капсулы должны выпускаться в плотно закрытой упаковке, предохраняющей от воздействия влаги. Поверхность капсулы может быть маркирована. На упаковке дополнительно указывают название всех антимикробных консервантов, входящих в состав. Хранение. Капсулы следует хранить в сухом месте, при температуре не выше 30°С или в соответствии с указанием нормативной документации на препарат. |
