Ацилирование
 Скачать 358.6 Kb. Скачать 358.6 Kb.
|
|
Коллоквиум №2 Модуль 11. 1. Приведите примеры ацильных групп и дайте им названия. 2. Приведите примеры реакций ацилирования. АЦИЛИРОВАНИЕ - введение ацильной группы R-C=O в молекулу органического соединения путем замещения атома Н. В широком смысле ацилированием называют замещение любого атома или группы атомов на ацильную группу. В зависимости от того, к какому атому присоединяется ацил, различают N-ацилирование, O-ацилирование, S-ацилирование и С-ацилирование. Реакция, при которой вводится формильная группа (НСО) -формилированием, ацетильная (СН3СО) - ацетилированием, бензоильная (С6Н5СО)-бензоилированием. Ацилирующими реагентами называются соединения, дающие в результате соответствующих реакций различные производные карбоновых кислот, в частности, сложные эфиры. В приведенном ниже примере ацилирующим реагентом является уксусная кислота. Гораздо более активные ацилирующие реагенты - хлорангидриды и ангидриды кислот: 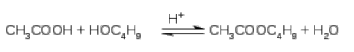 Уксусная кислота Бутиловый спирт бутилацетат 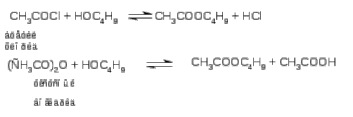 Бензоилирование аминов, спиртов и тиолов ведут в водно-щелочной среде (10%-ный р-р NaOH, р-ры NaHCO3,(Гидрокарбонат натрия) Na2CO3 (Карбонат натрия): бензоилхлорид аминогруппа 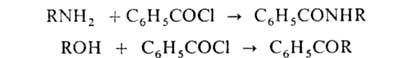 1)Бензойный альдегид Механизм реакции аренов по Фриделю-Крафтсу: 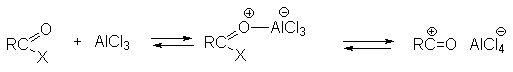 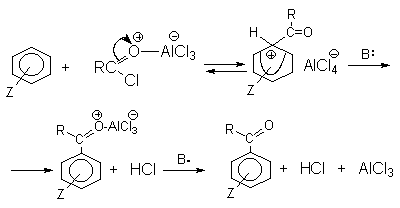 3. Сравните ацилирующую (реакционную) способность различных функциональных групп. 4. Представьте технологическую схему промышленного способа получения ёи дайте е описание. Модуль 8. 1. Укажите особенности синтезов с участием альдегидов и кетонов. Альдольная конденсация, образование полуацеталей и ацеталей. 2. Получение монохлордиметилового эфира (МХДМЭ). основные и побочные реакции, катализаторы.Где используется МХДМЭ. 3. Приведите основные реакции с участием формальдегида. 4. Приведите примеры синтезов на основе формальдегида и ацетилена. 5. Приведите примеры синтезов на основе формальдегида и олефинов. 6. Приведите условия промышленных синтезов ацетальдоля и кротонового альдегида. 7. Хлорметилирование по Блану. Для чего применяют хлорметилирование по Блану. Синтез бензилхлорида, основные, побочные реакции, катализаторы. 8. Производство дифенилолпропана (диана), основные, побочные реакции, катализаторы.Где применяется диан. 9. Синтез ДДТ, основные, побочные реакции, катализаторы. 10. Производство капролактама, основные, побочные реакции, катализаторы. 11. Реакция Принса. Синтез изопрена, основные, побочные реакции, катализаторы.Синтез пентаэретрита, основные, побочные реакции, катализаторы. Синтез диоксолана, основные, побочные реакции, катализаторы. 12. Продукты конденсации альдегидов с аммиаком и аминами. Синтез уротропина. 13. Синтез пиридинов, катализаторы и основные реакции. Образование оснований Шиффа и их использование. 14. Приведите технологическую схему получения метилизобутилкетона из ацетона и описание к ней. Метилизобутилкетон используют как растворитель для нитроцеллюлозных, полиакриловых, перхлорвиниловых лкм, в производстве линолеума, а также клеев, депарафинизации масел для смазки, краски для типографии, чернил, а также в качестве обемасливающего состава для парафинов (для того, чтобы удалить низкоплавкий парафин в смеси с маслами). Метилизобутилкетон в промышленности получают одностадийным синтезом из ацетона в жидкой фазе при низких температурах(393-433К) и высоких давлениях(1-10Мпа) в многотрубчатых реакторах. Химическая реакция для данного синтеза выглядит следующим образом: 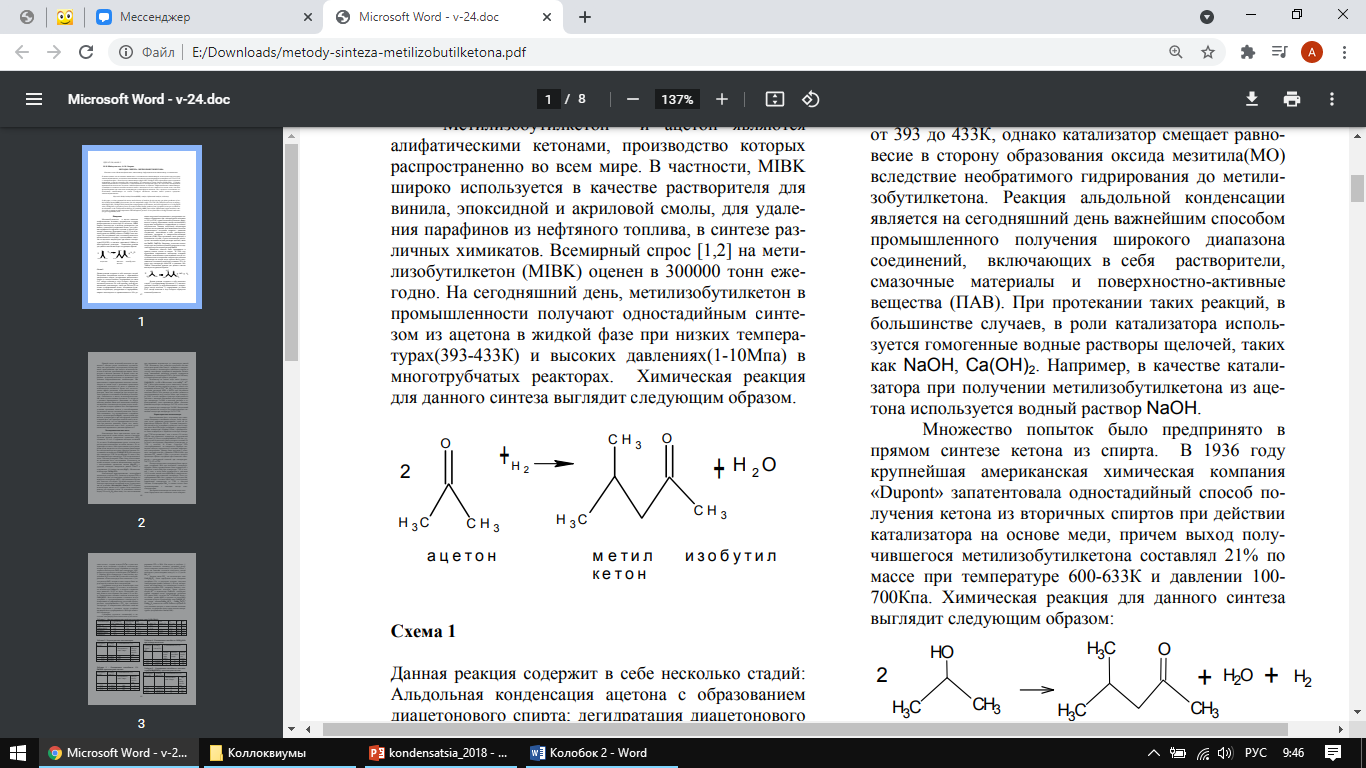 Данная реакция содержит в себе несколько стадий: Альдольная конденсация ацетона с образованием диацетонового спирта; дегидратация диацетонового спирта до оксида мезитила; гидрирование по связи С=С оксида мезитила в ходе которого образуется метилизобутилкетон. По этой причине, многофункциональные катализаторы, такие как Рd или Pt на основе сульфированной смолы, обладающие функциями конденсации, дегидратации и гидрирования, широко используются в промышленности. (Тех.схему не нашла) Модуль 6. 1. Приведите примеры реакции этерификации различных типов. Укажите условия их протекания. 2. Почему сложные эфиры применяются в пищевой промышленности? Приведите примеры запахов сложных эфиров. Сложные эфиры используются в парфюмерии, косметике, в качестве пищевых добавок, для изготовления искусственных волокон, краски, лаков, клея. Сложные эфиры служат исходными веществами в производстве многих фармацевтических препаратов. Сложные эфиры на основе низших спиртов и кислот используют в пищевой промышленности при создании фруктовых эссенций, а сложные эфиры на основе ароматических спиртов – в парфюмерной (изготовление мыла, духов, кремов) промышленности, т.к. именно присутствие сложных эфиров придает фруктам и цветам их запах. Этилформиат – ромовая эссенция. Этилацетат – грушевый аромат. HCOOCH2CH(CH3)2 — изобутилформиат напоминает запах ягод малины. CH3COOC5H11 — н-амилацетат (н-пентилацетат) напоминает по запаху грушу. CH3COOCH2CH2CH(CH3)2 — изоамилацетат (изопентилацетат) используется как компонент грушевой и банановой эссенции. CH3COOC8H17 — н-октилацетат имеет запах апельсинов. C3H7COOC2H5 — этилбутинат, имеет характерный запах ананасов. 3. Приведите технологическую схему производства этилацетата и описание к ней. 4. Приведите технологическую схему производства диметилтерефталата и описание к ней. Модуль 5. 1. Изложите теоретические основы процесса сернокислотной гидратации олефинов. Приведите условия проведения сернокислотной гидратации олефинов и побочные реакции. 2. Сформулируйте основные положения для разработки рациональной технологической схемы сернокислотной гидратации олефинов. 3. Представьте технологическую схему сернокислотной гидратации пропилена и описание к ней. 4. Изложите теорию процесса прямой гидратации этилена. 5. Приведите побочные реакции при прямой гидратации этилена. 6. Представьте технологическую схему прямой гидратации этилена и описание к ней. 7. Укажите возможные пути совершенствования процесса прямой гидратации этилена. 8. Дайте сравнительный анализ достоинств и недостатков технологий сернокислотной и прямой гидратации олефинов. Модуль 3. 1. Приведите примеры реакций неполного окисления различных типов. 2. Объясните радикально-цепной механизм окисления углеводородов. 3. Приведите известные промышленные способы окисления алканов. 4. Расскажите о производстве оксидов олефинов методом окисления. Объясните механизм окисления этилена в этиленоксид на серебре. 5. Изложите влияние различных факторов на эффективность процесса окисления этилена в этиленоксид. 6. Приведите технологическую схему производства этиленоксида окислением этилена техническим кислородом и описание к ней. 7. Изложите достоинства технологии получения этиленоксида окислением этилена техническим кислородом. 8. Приведите схему синтеза полиамидных волокон на основе циклогексана. 9. Изложите теоретические основы процесса синтеза адипиновой кислоты окислением циклогексана. 10. Приведите технологическую схему первой стадии окисления циклогексана в адипиновую кислоту и описание к ней. 11. Приведите технологическую схему второй стадии окисления циклогексана в адипиновую кислоту (доокисления) и описание к ней. 12. Изложите теоретические основы процесса окисления кумола в фенол и ацетон. 13. Приведите блок-схему процесса совместного получения фенола и ацетона. 14. Приведите технологическую схему установки по производству фенола и ацетона и описание к ней. |
