анемия. Актуальность темы. Под анемией понимают уменьшение количества эритроцитов и (или) гемоглобина. Гемоглобин является переносчиком кислорода в тканях
 Скачать 0.85 Mb. Скачать 0.85 Mb.
|
СОДЕРЖАНИЕВВЕДЕНИЕАктуальность темы. Под анемией понимают уменьшение количества эритроцитов и (или) гемоглобина. Гемоглобин является переносчиком кислорода в тканях. Поэтому при его недостатке развивается кислородное голодание тканей (гипоксия). Гипоксия проявится быстрой утомляемостью, слабостью, снижением памяти, головокружениями. Чем сильнее выражена анемия, тем выраженнее эти симптомы. Анемии чаще всего являются лишь синдромом, который присущ тому или иному заболеванию. В таких случаях говорят о вторичных анемиях. Однако в ряде случаев причин возникновения анемии установить не удается, и тогда говорят о первичной анемии как о самостоятельной патологии крови. Важными методами в диагностике анемии являются лабораторные методы анализа – определение концентрации гемоглобина, количества эритроцитов, величины и насыщенности их гемоглобином. Во всех случаях анемии необходимо полное морфологическое исследование крови с определением количества ретикулоцитов, тромбоцитов, лейкоцитов и лейкограммы. В случаях, когда на основании результатов клинических и лабораторных исследований нельзя установить диагноз, необходимо провести морфологическое исследование пунктата костного мозга, которое позволяет судить о функциональном состоянии кроветворной системы и установить диагноз. Для уточнения характера анемии необходимы исследования мочи и крови, определение СОЭ, содержания свободного гемоглобина в сыворотке крови, количества билирубина в крови, концентрации уробилиногена и желчных пигментов в моче, серологические исследования для определения содержания антиэритроцитарных факторов (антител), сывороточного железа, железосвязывающей способности плазмы и другие исследования. Цель исследования – на основании лабораторных данных провести дифференциальную диагностику анемий у пациентов в биохимической лаборатории. Задачи исследования: 1) представить теоретические основы развития анемий; 2) рассмотреть современные методы и алгоритм исследования в дифференциальной диагностике анемии; 3) провести исследования заболеваемости анемией взрослого населения Котласского района по данным статистики ГБУЗ АО « КОТЛАССКАЯ ЦЕНТРАЛЬНАЯ ГОРОДСКАЯ БОЛЬНИЦА ИМЕНИ СВЯТИТЕЛЯ ЛУКИ ( В.Ф ВОЙНО-ЯСЕНЕЦКОГО); База исследования – ГБУЗ АО « КОТЛАССКАЯ ЦЕНТРАЛЬНАЯ ГОРОДСКАЯ БОЛЬНИЦА ИМЕНИ СВЯТИТЕЛЯ ЛУКИ ( В.Ф ВОЙНО-ЯСЕНЕЦКОГО). Теоретической основой настоящей работы являются труды ученых, занимавшихся изучением анемии: С. А. Гусева, В. П. Вознюк, А. Г. Дубкова, К.М. Амбдулкадырова и др; внутренними болезнями: В.И.Маколкин, С.И.Овчаренко, Н.Н.Семенков и др. Поставленные цели и задачи в работе определяют структуру работы: введение, 2-х глав – теоретической и экспериментальной, выводами после каждой главы, заключением и приложениями. В первой главе рассмотрены теоретические основы развития анемий – рассмотрены патологические изменения состава крови, дана клиническая картина анемии, где представлена также классификация анемий, рассмотрены методы и критерии дифференциальной диагностики анемий. Во второй главе – экспериментальной – анализ зпболеваемости взрослого населения Котласского района. Теоретическая и практическая значимость работы заключается в том, что применяемые методы исследования могут применяться в клинической диагностике анемий. Глава 1. Теоретическая часть1.1 Общая характеристикаАнемия представляет собой серьезное состояние организма, характеризующееся значительным снижением количества гемоглобина в крови. Это обуславливает появление нарушений в работе внутренних органов, ухудшение общего состояния и вида. Лечение анемии у взрослых подразумевает использование лекарственных средств и правильного питания. При отсутствии противопоказаний допускается применение народных средств, но только в качестве комплексной терапии. Анемия-снижение уровня Нв и\или эритроцитов (гематокрита) по сравнению с нормальным уровнем [3 c.13]. Существует несколько классификаций анемий: 1.вызванные кровопотерей (постгеморрагические), 2. обусловленные нарушением кроветворения (гипопластическне) 3. связанные с повышенным разрушением эритроцитов (гемолитические) [12 c.125]. В зависимости от величины ЦП анемии бывают нормохромные, гипохромные и гиперхромные [1 c. 18]. При всех формах анемий наблюдается гипоксический синдром, вызванный нарушением дыхательной функции крови, который проявляется слабостью, повышенной утомляемостью, головокружением, шумом в ушах, одышкой, сердцебиением, бледностью и другими изменениями, зависящими от степени анемии. Снабжение кислородом органов ухудшается из-за недостатка выработка красных кровяных телец, за счет которых, соответственно, органы и обеспечиваются кислородом, отмечаемый в, заставляет, тем самым, страдать весь организм от нехватки железа. Преимущественно количественные показатели эритроцитов и гемоглобина являются достаточными в распознавании заболевания. Примечательно, что анемия (малокровие) может выступать как в качестве самостоятельного заболевания, так и в качестве сопутствующего проявления либо осложнения других видов заболеваний и состояний. И причины возникновения, и механизм развития заболевания могут быть совершенно различными, причем именно за счет выявления конкретной специфики в каждом отдельном случае впоследствии определяется соответствующая адекватная терапия. На рисунке 1 рассмотрим основные симптомы анемии 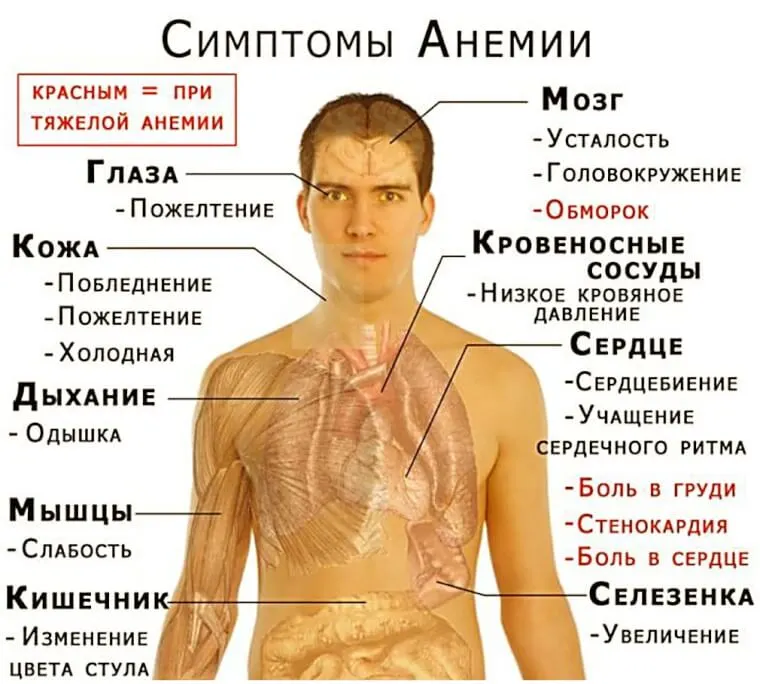 Рисунок 1 – Симптомы анемии Если останавливаться на конкретных цифрах, то анемия определяется как снижение гемоглобина до отметки ниже 110 г/л - у детей 6мес.-6 лет, ниже 120 г/л – у детей 6-14 лет, ниже 120 – у взрослых женщин, ниже 130 – у взрослых мужчин. Анемия может долгое время никаким образом не проявлять себя, при этом в организме пациента может наблюдаться сильная кровопотеря. Такие состояния обычно регистрируются у женщин во время менструаций, а также у обоих полов при наличии хронических эрозивных очагов. Помимо этого, болезнь может быть вызвана наличием раковых образований и сильным снижением уровня железа в крови. Выявить точную причину патологии может только лечащий врач. 1.2 Железодефицитные анемииВозникают в тех случаях, когда расходование Fe превышает его поступление [3 c.91]. Причина – кровотечения (маточные, желудочно-кишечные, легочные, носовые, десневые, геморроидальные, из мочевых путей), кровоизлияния в замкнутые полости с последующим нарушением реутилизации Fe, в также кровопотери у доноров; недостаточное и нерациональное питание (алиментарный дефицит), нарушение всасывания (после резекции желудка, обширных резекций тонкой кишки, при хронических энтеритах, хронических энтеритах, хронических панкреатитах), повышенный расход Fe (при беременности, лактации, усиленном росте, половом созревании) [5 c.82]. Клиника. Развивается постепенно. Сидеропенические симптомы: извращение вкуса и обоняния, выпадение волос, повышенная ломкость ногтей, трофические нарушения кожи и ее дериватов, сухость кожи и образование трещин на руках и ногах, ангулярный стоматит, дисфагия в сочетании с глосситом, мышечная слабость, императивные позывы на мочеиспускание. Выявляются нарушения желудочной секреции, поверхностный или атрофический гастрит, дуоденит, нарушения кишечного всасывания [7 c.73]. При исследовании крови определяют анемию различной степени. Цветовой показатель низкий. Среднее содержание Hb в эритроците снижено. Эритроциты гипохромные, отмечаются микроцитоз и пойкилоцитоз. Снижаются концентрация Fe в сыворотке крови и насыщение трансферрина Fe (меньше 16%). Повышается общая железо-связывающая способность сыворотки крови. ДифДианг с сидероахрестическими анемиями (высокое содержание Fe в сыворотке крови, обусловленное нарушением синтеза или утилизации порфиринов) [9 c.64]. Гипохромные анемии наблюдаются при талассемии, ночной пароксизмальной гемоглобинурии. Ведущими симптомами указанных гипохромных анемий являются признаки гемолиза [11 c.59]. Анемия, при инфекциях и воспалениях, может быть гипохромной. Причиной ее возникновения считается перераспределение Fe, его количество увеличивается в очагах воспаления и макрофагах костного мозга. Общая железосвязывающая способность сыворотки крови снижена; изолированный легочный сидероз и синдром Гудпасчера. 1.3 Витамин B12-дефицитные анемииЭтиология: недостаточность/отсутствие внутреннего факторы Касла (париетальные клетки желудка) – гастрэктомия, инвазия широким лентецом, хронический алкоголизф, хронический панкреатит [20 c.21]. Клиника. Витилиго, ангулярный стоматит, фуникулярный миелоз, атрофический глоссит, увеличение печени и селезенки [18 c.12]. ОАК – панцитопения. БАК - В12 менее 100 пг/мл (норм. 160-950 пг/мл), гипербилирубинемия, может быть АТ к фактору Касла и париетальным клеткам желудка [16 c.32]. Диагностическая Проба Шиллинга – экскреция с мочой радиоактивного кобаламина, принятого внутрь. Пункция костного мозга – «синий» костный мозг (много мегалобластов). ДифДифгн. фолиеводефицитная анемия – нет глоссита. гемолитические и постгеморрагические анемии – анамнез, нет глоссита [14 c.23] 1.4 Анемии, вызванные дефицитом фолиевой кислотыУ лиц, перенесших резекцию части тонкой кишки, при спру, целиакии, синдроме слепой кишки, у беременных, не употребляющих овощей и фруктов, а также у беременных, больных гемолитической анемией. Больные с дефицитом фолиевой кислоты жалуются на общую слабость, головокружение, склеры глаз у них иктеричны. При анемии, обусловленной спру, наблюдаются потеря в массе, вздутие живота, стеаторея, гипокальциемия, тетания, деминерализация в костной ткани, боль в костях, патологические переломы. При исследовании крови определяются гиперхромная анемия с анизоцитозом, макроцитоз, уменьшение количества тромбоцитов и лейкоцитов. В костном мозге обнаруживаются мегалобласты. ДифДианг определение метилмалоновой кислоты, радиоиммунологическое исследование цианокобаламина и фолиевой кислоты. 1.5 Гемолитические анемииВиды гемолитических анемий представлены на рисунке 2 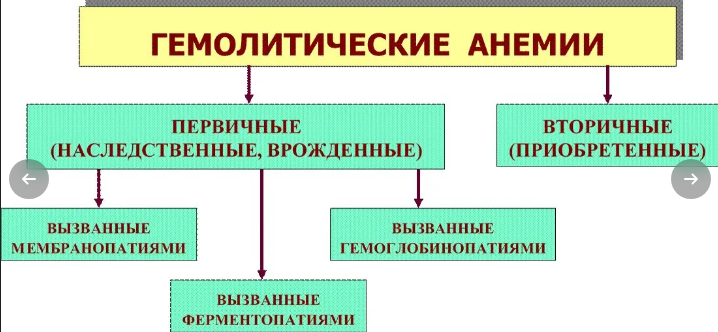 Рисунок 2 – Гемолитические анемии По локализации гемолиза их можно разделить на: - анемии с внутриклеточным разрушением эритроцитов; - анемии с внутрисосудистым разрушением эритроцитов [2 c.20]. Наследственный микросфероцитоз (болезнь Минковского—Шоффара) является одной из самых частых форм гемолитических анемий [4 c.19]. Заболевание обычно носит семейно-наследственный характер и передается по доминантному принципу аутосомно [6 c. 28]. Патогенез. Набухание эритроцитов [8 c.37]. Клиника. Наследственный микросфероцитоз проявляется в любом возрасте, но чаще в детском. При тяжелом течении у больных с детства отмечаются деформации скелета (башенный череп, микрофтальмия, высокое небо, трофические язвы голени). Клинические проявления наследственного микросфероцитоза — анемия разной степени, желтуха, увеличение селезенки [10 c.46]. Частым осложнением является образование пигментных камней в желчном пузыре и желчевыводящих путях, что связано с выерким содержанием билирубина в желчи [12 c. 55]. Диагн и ДиффДиагн. Диагноз устанавливают на основании семейного анамнеза, наличия у больного анемии, желтухи и спленомегалии, ретикулоцитоза, микросфероцитоза, снижения осмотической резистентности эритроцитов [14 c.91]. При аутоиммунных гемолнтических анемиях в периферической крови определяются микросфероциты, однако для этих анемий не характерны длительность заболевания, наличие болезни у родителей и близких родственников. В отличие от наследственного микросфероцитоза при аутоиммунных гемолитнческих анемиях в сыворотке крови обнаруживаются антитела [16 c.82]. 1.6 Серповидно-клеточная анемияКлиника. Серповидно-клеточная анемия проявляется в детском возрасте, но не ранее 6 мес [1 c.37]. Характерны поражение костно-суставной системы, замедленное физическое развитие, желтуха, спленогепатомегалия, хронические язвы конечностей, нарушение зрения [3 c.46]. В крови определяются нормохромная анемия, ретикулоцитоз, базофильная пунктация эритроцитов, СОЭ чаще в пределах нормы. В костном мозге увеличено количество эритрокариоцитов [5 c.45]. Диагностика. Для диагностики серповидно-клеточной анемии используют определение серповидности эритроцитов в пробе крови с мета бисульфитом или в крови, взятой после наложения жгута на основание пальца, электрофорез Hb [7 c. 66]. 1.7 ТалассемииЭтиология и патогенез. Талассемия — заболевание с наследственным нарушением синтеза одной из цепей глобина, которая синтезируется в малом количестве или совсем не синтезируется [9 c.2]. Другая цепь синтезируется в избыточном количестве, агрегирует и откладывается в эритрокариоцитах. Эритрокариоциты гибнут в костном мозге, что приводит к анемии [11 c.33]. Клиника. Гомозиготной талассемии свойственно проявление тяжелой гемолитической анемии к концу первого года жизни. Отмечаются значительное увеличение селезенки, желтуха, бледность с сероватым оттенком кожи, отставание в физическом развитии, остеопороз костей, аномалия развития. При исследовании крови обнаруживается выраженная гипохромная анемия (содержание Hb составляет 30— 50 г/л, цветовой показатель 0,5 и ниже), ретикулоцитоз. Эритроциты гипохромные, резко выражен анизоцитоэ, много мишеневидных эритроцитов, базофильная пунктация. Содержаяие Fe в сыворотке крови повышено [13 c.5]. Десфераловый тест позволяет установить увеличение запасов Fe [15 c. 7]. При тяжелой форме талассемии дети погибают в первый год жизни, яри среднетяжелой доживают до 5—8 лет, при промежуточной форме дети доживают до взрослого возраста. Лабораторный диагноз талассемии подтверждается исследованием содержания фетального Hb в эритроцитах. Гетерозиготная талассемия протекает бессимптомно или в манифестной форме со спленомегалией и изменениями костей [17 c.17]. Методом электрофоретического разделения Hb устанавливают увеличение количества Hb, у некоторых больных — Hb F [19 c.32]. 1.8 Аутоиммунные гемолитические анемииКлиника. Начало заболевания может быть разным. При острой форме аутоиммунной ГА внезапно появляются резкая слабость, озноб, повышение температуры до 39—40 С [20 c.21]. Отмечаются боль в области сердца, сердцебиение, одышка, боль в пояснице, тошнота, рвота, схваткообразная боль в животе, моча черного цвета. Быстро развивается желтуха. Обнаруживаются расширение границ сердца, тахикардия, систолический шум над верхушкой и в пятой точке, гипотензия, в тяжелых случаях возникает шок. Селезенка и печень могут быть увеличены, возможно развитие острой почечной недостаточности. Картина крови характеризуется резко выраженной анемией, ретикулоцитозом, нормоэритробластозом, микросфероцитозом, наличием фрагментированных эритроцитов, лейкоцитозом с ядерным сдвигом до миелоцитов [3 c.99]. В пунктате костного мозга отмечается гиперплазия красного ростка. Диагн и ДифДианг. Диагноз аутоиммунных гемолитических анемий подтверждается положительной прямой пробой Кумбса. ДифДиангс острыми инфекциями: острым гепатитом, острым лейкозом-эритромиелозом, другими видами гемолитических анемий (болезнью Минковского—Шоффара, дефицитом Г-6-ФДГ). Для острого гепатита характерна высокая концентрация непрямого билирубина и трансфераз в сыворотке крови. При остром эритромиелозе в пунктате костного мозга обнаруживают бластные клетки. Серологическая диагностика, определение активности Г-б-ФДГ, сахарозная проба и проба Хема, отсутствие болезни у родственников помогают в проведении дифференциального диагноза с другими гемолитическими анемиями. 1.9 Ночная пароксизмальная гемоглобинурия (болезнь Маркиафавы-Микели)Приобретенная форма гемолитической анемии, связанная с изменением структуры мембраны эритроцитов, протекающая с внутрисосудистым гемолизом. Клиника. НПГ чаще развивается постепенно, больные жалуются на слабость, недомогание, головокружение, одышку, сердцебиение, боль в животе различной локализации, желтушность склер, кожи, темную мочу (чаще утром). У них выявляют тромбофлебиты различной локализации. Печень и селезенка обычно не увеличены. В период гемолитического криза появляются сильная боль в животе, пояснице, температура повышается до фебрильной, выделяется черная моча. При исследовании крови обнаруживают нормохромцую или гипохромную анемию. Диагн. Диагноз болезни Маркиафавы—Микели подтверждается данными специфических гемолитических тестов — пробы Хема и сахарозной пробы. 1.10 Гипопластические анемииГипопластические анемии (апластическая, арегенераторная, гипорегенераторная) обусловлены уменьшением продукции клеток костного мозга. Этиология и патогенез. Причиной развития заболевания могут быть различные факторы экзогенного и эндогенного происхождения: ионизирующая радиация, химические вещества (бензол, бензин, мышьяк, ртуть, висмут), органические растворители, минеральные удобрения, инсектициды, лекарственные средства (цитостатические и сульфаниламидные препараты, левомицетин, стрептомицина сульфат, салициловая кислота, антигистаминные, противомалярийные, противосудорожные, противотиреоидные, противотуберкулезные средства, препараты золота и др.). Гипопластическая анемия возникает также после перенесенного вирусного гепатита, при хронических инфекциях. Выделяют конституциональную гипопластическую анемию, наблюдаемую в детском возрасте. Однако в 50—75 % случаев причина гипопластической анемии остается неизвестной. Формы гипопластической анемии: с поражением всех трех ростков кроветворения (панцитопения), с сохраненным тромбоцитопоэзом (парциальная форма), с депрессией эритропоэза (красноклеточная аплазия), с гипергемолизом. Клиника. Наиболее характерным признаком картины крови является пангемоцитопения (эритро-, тромбо-, лейкопения с нейтропенией и относительным лимфоцитозом). Анемия носит нормохромный, реже гиперхромный характер. Количество ретикулоцитов снижено. У большинства больных увеличена СОЭ. В миелограмме обнаруживается уменьшение количества миелокариоцитов, угнетение эритроидного, гранулоцитарного и мегакариоцитарного ростков при относительном увеличении числа лимфоидных клеток. В трепанате подвздошной кости преобладает жировой костный мозг. ДифДиагн проводится в первую очередь с алейкемическим острым лейкозом, злокачественными новообразованиями, цианокобаламиндефицитной анемией, ночной пароксиэмальной гемоглобинурией (болезнью Маркиафавы—Микели), идиопатической тромбоцитопенической пурпурой. Стернальная пункция позволяет исключить острый лейкоз, для которой характерна лейкозная метаплазия костного мозга, и В12-дефицитную анемию с наличием мегалобластов в пунктате костного мозга. Исследование костного мозга играет ведущую роль также в дифференциальной диагностике гипопластической анемии, протекающей с внутрисосудистым гемолизом, и пароксизмальной ночной гемоглобинурии, при которой не наблюдается угнетения кроветворения. При идиопатической тромбоцитопенической пурпуре костный мозг богат клеточными элементами и характеризуется повышенным содержанием мегакариоцитов. Злокачественным новообразованиям (чаще выявляются опухоли желудочно-кишечного тракта) свойственно токсическое влияние на костный мозг и (или) метастазирование в этот орган, что обусловливает угнетение кроветворения поэтому больным гипопластической анемией необходимы исследования желудочно-кишечного тракта, органов грудной клетки, консультации уролога и гинеколога. Наличие «немотивированной» высокой лихорадки также более характерно для опухоли. В пунктате костного мозга могут быть раковые клетки. 2. Практическая частьПо данным ВОЗ анемии занимают первое место среди 38 самых распространенных заболеваний во всем мире [2]. Наиболее часто анемии встречаются у детей, подростков и женщин детородного возраста. Литературные данные свидетельствуют о том, что 80% всех анемий приходится на железодефицитные [1, 7, 9]. В России и ближнем зарубежье (СНГ) частота железодефицитных анемий (ЖДА) у женщин колеблется от 7,3 до 57,7%, а у мужчин - от 3 до 29,7% [5, 6, 10, 11]. В настоящее время доказано, что железодефицитные состояния являются причиной тяжелых поражений жизненно важных органов и систем организма, вызывающих снижение работоспособности, увеличение инфекционной заболеваемости. Огромное негативное влияние дефицит железа оказывает на развитие детей, подростков, беременность и нервно-психическую сферу человека, что определяет социально-экономическую значимость данной проблемы [7, 8, 13]. На сегодняшний день раскрыты многие этиологические и патогенетические механизмы развития, изучены вопросы диагностики и лечения ЖДА. Однако многие звенья патогенеза требуют уточнения [3, 12]. Основными причинами дефицита железа в организме считаются кровопотери, алиментарная недостаточность железа в пище, усиленные его траты у подростков, беременных и кормящих женщин, нарушение всасывания и транспорта в кишечнике [14]. Среди экзогенных факторов особое место занимают факторы внешней среды, влияние которых отражается на состоянии адаптационных систем организма и прежде всего систем гемопоэза и иммунитета. Истощение их резерва приводит к росту гемо- и иммунопатологии среди населения экологически неблагополучных регионов [13]. Обследование жителей различных регионов России показало, что частота ЖДА зависит от экологических условий и профилей производственной деятельности [4]. Представляет интерес изучение заболеваемости анемиями взрослых жителей региона с развитой химической промышленностью, каким является Котласский район. Цель данной работы заключалась в анализе распространенности анемии среди взрослого населения ГБУЗ АО «КОТЛАССКАЯ ЦЕНТРАЛЬНАЯ ГОРОДСКАЯ БОЛЬНИЦА ИМЕНИ СВЯТИТЕЛЯ ЛУКИ (В.Ф. ВОЙНО-ЯСЕНЕЦКОГО) и медикосоциальной оценке факторов риска возникновения данного заболевания. Материалы и методы Котласский район приравнен к районам Крайнего Севера. Расположен в юго-восточной части Архангельской области, площадь территории — 6,3 тыс. км². Граничит: - на западе с Устьянским районом - на севере с Красноборским районом - на северо-востоке с Ленским районом - на востоке c Вилегодским районом - на юго-востоке с Лузским районом Кировской области - на юге с Великоустюгским районом Вологодской области Также территория муниципального района граничит с территорией двух самостоятельных муниципальных образований (городских округов) Архангельской области: город Коряжма и Котлас. Проведено изучение распространенности анемии среди взрослого населения Котласского района в период с 2017 по 2021 гг. С этой целью нами были использованы официальные отчетные документы: Форма № 12 «Сведения о числе заболеваний, зарегистрированных у больных, проживающих в районе обслуживания лечебного учреждения» (сводная по Котласскому району). Форма № 30 «Сведения о лечебно-профилактическом учреждении» (сводная по Котласскому району). Статистические материалы о заболеваемости населения России. Так как в форме № 12 в числе сведений о заболеваниях, зарегистрированных у больных, проживающих в районе обслуживания лечебного учреждения, отсутствует рубрика «Железодефицитные анемии», заболеваемость оценивалась по показателям обращаемости в лечебно-профилактическое учреждение. Для оценки факторов риска был проведен анализ динамики выбросов загрязняющих веществ предприятиями Котласского района. Для этого были использованы официальные документы: Статистическая отчетность по форме № 2-ТП (водхоз) по предприятиям Котласского района. Статистическая отчетность по форме № 2-ТП (воздух) по предприятиям Котласского района. Комплексный доклад о состоянии окружающей среды Архангельской области. Результаты и обсуждение Установлено, что в среднем общая заболеваемость взрослого населения Котласского района составила 83821,26 на 100000 населения, что на 11,15% выше, чем по Российской Федерации. В то же время заболеваемость гематологическими болезнями и анемиями оказалась ниже показателей по РФ на 54,1% (294,72) и на 43,8% (251,3) соответственно. За исследуемый период уменьшилась распространенность болезней крови с 312,08 до 265,86 на 100000 населения (на 14,8%); анемий – с 259,75 до 251,49 (на 3,2%) и впервые выявленных анемий – с 50,5 до 35,9 (на 28,9%) (рис. 1, табл. 1). Что касается общей заболеваемости, то она уменьшилась всего лишь на 2,4% (с 91603 до 89399,66 на 100000 населения). Следует отметить, что удельный вес анемий при всех болезнях крови увеличился с 83 до 94,6%, а впервые выявленных анемий во всех анемиях уменьшился с 19,4 до 14,3% (табл. 1). Известно, что оценка заболеваемости по обращаемости на 100000 населения не отражает истинную картину распространенности какой-либо патологии среди населения, однако позволяет судить об общей динамике процесса, степени ее выявляемости на различных территориях. 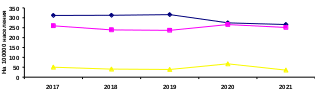  Заболеваний крови и кроветворных органов Заболеваний крови и кроветворных органов  Из них анемий Из них анемий  Впервые выявленные анемии Впервые выявленные анемииРисунок 1 - Динамика заболеваемости болезнями крови и кроветворных органов взрослого населения Котласского района за 2017-2021 гг. (на 100000 населения). Таблица 1 Показатели общей, гематологической заболеваемости и заболеваемости анемиями взрослого населения Котласского района (на 100000 населения) за 2017 – 2021 гг.
Анализ распространенности анемии в городах района с учетом социальных и экологических факторов выявил неравномерность распределения данной патологии. В г. Устьянск она составила 222,3 на 100000 населения, а в г. Красноборск – 399,1. Причем, эти показатели не коррелировали с общей заболеваемостью населения. Так, в г. Красноборск при самой низкой общей заболеваемости (76663,9 на 100000 населения) распространенность анемии оказалась самой высокой (табл.2). Таблица 2 Показатели общей, гематологической заболеваемости и заболеваемости анемиями взрослого населения Котласского района в городах Котласского района (на 100000 населения) за 2021г
Наличие в Ашинском районе нескольких промышленных предприятий, построенных без учета нагрузки на окружающую среду, привело к возникновению целого ряда экологических проблем. По данным специальных исследований, в жилой зоне г. Устьянск зарегистрировано превышение предельно допустимых концентраций оксида железа, оксида марганца, диоксида кремния, оксида углерода, взвешенных веществ, пыли неорганической с содержанием SiO2> 70%. В реке обнаружены железо общее, медь, цинк, шестивалентный хром, азот аммонийный, нефтепродукты. Объем вредных выбросов от стационарных источников достиг 5,945 тыс. тонн. Основным источником загрязнения атмосферы района является химический завод, на долю которого приходится 84% от всех вредных выбросов. Предприятие специализируется на выплавке стали в мартеновских печах. При этом в атмосферу выделяются оксиды металлов, оксиды азота, оксид углерода, сернистый ангидрид. Необходимо признать, что спонтанно сложившиеся взаимоотношения жилых и промышленных зон исключает их возможность беспроблемного сосуществования на сегодняшний день. В данном случае, признавая приоритет интересов жителей района, путь обеспечения санитарного благополучия за счет технически обоснованного вложения средств в совершенствование и реконструкцию технологических процессов представляется единственно верным. Следует отметить, что в последние годы закончен перевод основных производств Котласского района химического завода с мазута на природный газ, введены в эксплуатацию новые очистные сооружения. В результате проведенных мероприятий уменьшился выброс загрязняющих веществ Котласским химическим заводом с 5,174 до 4,151 тыс. тонн. ЗАКЛЮЧЕНИЕЧтобы снизить вероятность развития анемии, желательно придерживаться рекомендованных мер: - совершать хотя бы раз в два дня часовую прогулку на свежем воздухе; - отдыхать после трудового дня, при этом желательно это делать в спокойной обстановке; - правильно питаться, постоянно включая в свой рацион железосодержащие продукты и напитки; - раз в год пропивать железосодержащие препараты; - не допускайте глистной инвазии; - избегайте частого контакта с химическими веществами и токсинами; - во время заправки автомобиля не допускайте вдыхания паров горючего; - поддерживать оптимальную физическую форму. Так как профилактические меры не всегда дают должный результат, рекомендуется два раза в год сдавать общий анализ крови на уровень гемоглобина. Если у вас ранее наблюдались проблемы с показателем красных телец, желательно проходить подобные обследования каждые три месяца. Анемия – это в большинстве случаев результат неправильного питания и образа жизни. Лишь в небольшом проценте случаев подобное состояние обусловлено наличием серьезных патологий, которые могут приводить к малокровию. Составление правильного рациона, прием поливитаминов и забота о собственном здоровье – это залог долголетия и отсутствия проблем с показателями гемоглобина. В Котласском районе – регионе с развитой химической промышленностью - в период с 2017 по 2021 гг. отмечается снижение показателя заболеваемости анемиями взрослого населения на 3,2% (с 259,75 до 251,49 на 100000 населения). В структуре общей гематологической заболеваемости удельный вес анемий составил 94,6%. Установить достоверно распространенность анемий в Котласском районе с учетом количественных показателей, таких как «заболеваемость-загрязненность», «доза-эффект», при соответствующем уровне информированности и отсутствии в форме не представляется возможным. Снижение заболеваемости в Котласском районе, вероятнее всего, связано с улучшением экологической ситуации за счет перевода основных производств Котласского химического завода с мазута на природный газ, реконструкцией охранительно-очистительных сооружений, что привело к уменьшению выбросов загрязняющих веществ в атмосферу и водоемы района. СПИСОК ЛИТЕРАТУРЫ1. Лунякова М.А. et al. Патогенез и возможности терапии анемии у детей с острым лимфобластным лейкозом//Вопросы гематологии, онкологии и иммунопатологии в педиатрии. 2013. Vol. 12, N 2. P. 5 - 16. 2. Павлов А.Д., Морщакова Е.Ф., Румянцев А.Г. Эритропоэз, эритропоэтин, железо. М.: ГЭОТАР-Медиа, 2011. 304 p. 3. Безнощенко А.Г. et al. Эритропоэтин в лечение анемии у детей и подростков с острым лимфобластным лейкозом//Детская онкология. 2008. Vol. 3. P. 11 - 15. 4. Dicato M. Anemia in Cancer: Some Pathophysiological Aspects//Oncologist. Alphamed Press, 2003. Vol. 8, N S1. P. 19 - 21. 5. Dicato M., Plawny L., Diederich M. Anemia in Cancer//Ann. Oncol. 2010. Vol. 21, N Supp. 7. P. 167 - 172. 6. Dallalio G., Law E., Means R.T. Hepcidin inhibits in vitro erythroid colony formation at reduced erythropoietin concentrations//Blood. Blood, 2006. Vol. 107, N 7. P. 2702 - 2704. 7. Wang W. et al. Influence of Tumor Necrosis Factor-Alpha and Interferon-Gamma on Erythropoietin Production and Erythropoiesis in Cancer Patients With Anemia//Zhonghua Xue Ye Xue Za Zhi. 2007. Vol. 28, N 10. P. 681 - 684. 8. Corazza F. et al. Anemia in Children With Cancer Is Associated With Decreased Erythropoietic Activity and Not With Inadequate Erythropoietin Production//Blood. 1998. Vol. 92, N 5. P. 1793 - 1798. 9. Kim M.H. et al. Defective erythropoiesis in bone marrow is a mechanism of anemia in children with cancer.//J. Korean Med. Sci. J Korean Med Sci, 2002. Vol. 17, N 3. P. 337 - 340. 10. Kivivuori S.M. et al. Serum transferrin receptor and erythropoiesis in children with newly diagnosed acute lymphoblastic leukemia//Leuk. Res. Leuk Res, 1994. Vol. 18, N 11. P. 823 - 828. 11. Hellebostad M. et al. Serum immunoreactive erythropoietin in children with acute leukaemia at various stages of disease - and the effects of treatment//Eur. J. Haematol. Eur J Haematol, 1990. Vol. 44, N 3. P. 159 - 164. 12. Dowd M. et al. Serum Erythropoietin Levels in Children With Leukemia//Med. Pediatr. Oncol. Med Pediatr Oncol, 1997. Vol. 28, N 4. 13. Corazza F.V. Physiopathologic Aspects of Anemia and Thrombocytopenia in Children With Cancers: The Roles of Erythropoietin and Thrombopoietin//Bull Mem Acad R Med Belg. 2008. Vol. 163, N 1 - 2. P. 152 - 156. 14. Лунякова М.А. et al. Уровни сывороточного эритропоэтина при анемиях у детей с острым лимфобластным лейкозом до начала химиотерапии//Онкогематология. 2008. Vol. 4. P. 54 - 55. 15. Bhavnani М., Morris Jones P.H., Testa N.G. Children in long-term remission after treatment for acute lymphoblastic leukaemia show persisting haemopoietic injury in clonal and long-term cultures//Br. J. Haematol. Br J Haematol, 1989. Vol. 71, N 1. P. 37 - 41. 16. Gardner R.V., Astle C.M., Harrison D.E. Hematopoietic Precursor Cell Exhaustion Is a Cause of Proliferative Defect in Primitive Hematopoietic Stem Cells (PHSC) After Chemotherapy//Exp. Hematol. 1997. Vol. 25. P. 495 - 501. 17. Yao M. et al. Quantitative and qualitative alterations of long-term culture-initiating cells in patients with acute leukaemia in complete remission//Br. J. Haematol. Br J Haematol, 1998. Vol. 103, N 1. P. 124 - 128. 18. Galotto M. et al. Stromal damage as consequence of high-dose chemo/radiotherapy in bone marrow transplant recipients//Exp. Hematol. Exp Hematol, 1999. Vol. 27, N 9. P. 1460 - 1466. 19. Verfaillie C.M., Catanzarro P.M., Li W.N. Macrophage inflammatory protein  , interleukin 3 and diffusible marrow stromal factors maintain human hematopoietic stem cells for at least eight weeks in vitro//J. Exp. Med. Rockefeller University Press, 1994. Vol. 179, N 2. P. 643 - 649. , interleukin 3 and diffusible marrow stromal factors maintain human hematopoietic stem cells for at least eight weeks in vitro//J. Exp. Med. Rockefeller University Press, 1994. Vol. 179, N 2. P. 643 - 649.20. Shankar A.G. The Role of Recombinant Erythropoietin in Childhood Cancer//Oncologist. Alphamed Press, 2008. Vol. 13, N 2. P. 157 - 166. 21. Michon J. Incidence of anemia in pediatric cancer patients in Europe: Results of a large, international survey//Medical and Pediatric Oncology. Med Pediatr Oncol, 2002. Vol. 39, N 4. P. 448 - 450. 22. Becker P.S. et al. Hematopoietic growth factors. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Version 2.2020. 2020. P. 98. 23. Ludwig H. et al. Iron metabolism and iron supplementation in cancer patients//Wien. Klin. Wochenschr. Springer-Verlag Wien, 2015. Vol. 127, N 23 - 24. P. 907 - 919. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
