алгоритм решения цепочек. Алгоритм решения цепочек. Алгоритм решения цепочек превращения по химии
 Скачать 19.72 Kb. Скачать 19.72 Kb.
|
|
Алгоритм решения «цепочек превращения» по химии В химии есть задания со схемами превращений одних веществ в другие, которые характеризуют генетическую связь между основными классами органических и неорганических соединений. Схему превращения одних веществ в другие называют «цепочкой превращений». Для выполнения этих заданий необходимо знать основные классы соединений, их номенклатуру, химические свойства, механизм осуществления реакций. Алгоритм решения «цепочки превращений» 1 шаг. Перепишите цепочку, которую необходимо решить Ca → CaO → Ca(OH)2 → Ca3(PO4)2 2 шаг. Пронумеруйте количество реакций для удобства решения 1 2 3 Ca → CaO → Ca(OH)2 → Ca3(PO4)2 Таким образом, мы видим, что нам надо составить 3 уравнения реакции 3 шаг. Запишем 1 уравнение реакции – из кальция (Сa) надо получить оксид кальция (CaO). Вспомним, что данное превращение происходит, когда металлы окисляются на воздухе, вступая в реакцию с кислородом. Записываем эту реакцию. Внимание! Не забывайте уравнивать реакции! 2Сa + O2 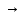 2Ca+2O-2 2Ca+2O-24 шаг. Осуществляем второе превращение. Из оксида кальция (CaO) нужно получить гидроксид кальция (Ca(OH)2). Это уравнение возможно при взаимодействии оксида с водой. (Такая реакция возможна, если в итоге получается щелочь – растворимое в воде основание). Записываем уравнение и уравниваем его. 2) 2Ca+2O-2 + H2O → Ca 2+(OH)2- 5 шаг. Осуществляем 3 превращение. Из гидроксида кальция (Ca(OH)2) необходимо получить соль – фосфат кальция (Ca3(PO4)2). Вспоминаем, что при взаимодействии основания и кислоты получается соль и вода. Значит, для этой реакции подойдет фосфорная кислота – H3PO4, так как именно она дает соли – фосфаты. Записываем уравнение реакции и уравниваем его. 3) 3Ca2+(OH)2- + 2H3+PO43- → Ca32+(PO4)23- + 6H2O |
