органическая химия. ХИМИЯ ЕГЭ. Алканы Электролиз солей кк декарбоксилирование солей кк каталитическое окисление Алкены
 Скачать 129.37 Kb. Скачать 129.37 Kb.
|
|
Алканы: Электролиз солей КК 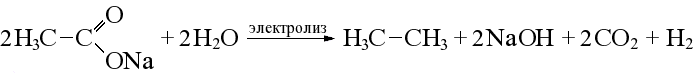 Декарбоксилирование солей КК Каталитическое окисление Алкены: Дегалогенирование дигалогеналканов Обесцвечивают бромную воду Обеспечивают перманганат калия Радикальное галогенирование Циклоалканы: Малые циклы Галогенирование Гидрогалогенирование 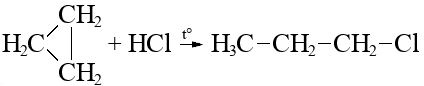 Большие циклы Радикальное галогенирование 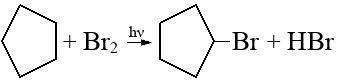 Алкадиены Номенклатура: Дивинил Изопрен Хлоропрен Можно получить дегидрированием алканов, дегидрогалогенированием дигалогеналканов Синтез Лебедева Присоединение: -40* = 1,2 +40* = 1,4 Алкины: Получение: Дегидрогалогенирование дигалогеналканов 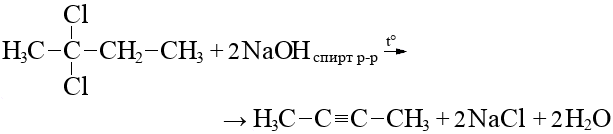 Пиролиз метана Свойства: Димеризация ацетилена Гидратация (реакция Кучерова) С амидами металлов С аммиакатами Арены: Номенклатура: Толуол Ксилол Кумол Стирол Реакция Вюрца-Фиттига Хлорирование: ALCL3 = 1-хлорбензол hV = хлоран Алкилирование Толуол: Галогенирование 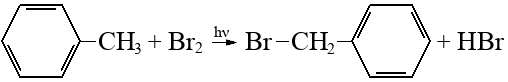 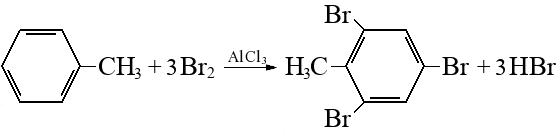 Нитрование 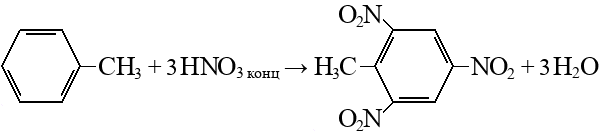 Стирол: Обесцвечивает бромную воду (присоединение по кратной связи) Одноатомные спирты: Этерификация С сильными хлорирующими агентами Внутримолекулярная дегидратация Межмолекулярная дегидратация Окисление оксидом меди Дегидрирование С аммиаком Каталитическое окисление кислородом Многоатомные спирты: С азотной кислотой 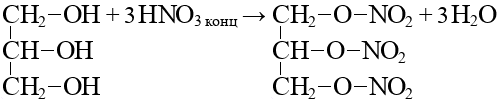 С гидроксидом меди – синий раствор 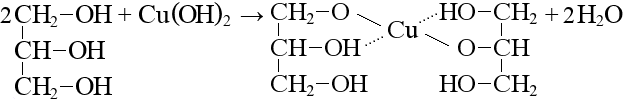 Фенолы: Номенклатура: крезол 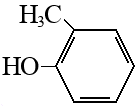 пирокатехин 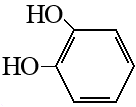 резорцин 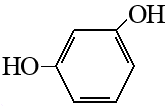 гидрохинон Получение: Каталитическое окисление кумола = фенол+ацетон 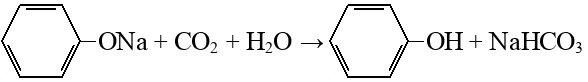 Свойства: Каталитическое галогенирование 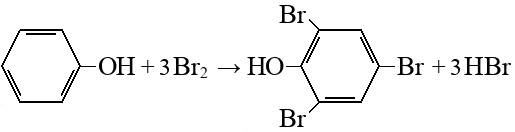 Карбонильные соединения: Номенклатура: Формальдегид (муравьиный альдегид) - метаналь Ацетальдегид (уксусный альдегид) – этаналь Бензальдегид – фенилметаналь Ацетон – пропанон-2 Ацетофенол – метилфенилкетон Получение: Щелочной гидролиз дигалогеналканов 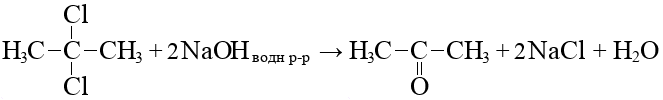 Окисление спиртов оксидом меди или соединениями хрома (первичные = альдегид, вторичные = кетон) Пиролиз солей КК 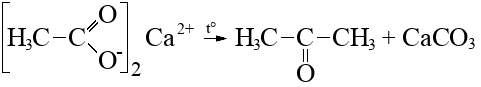 Свойства: Со спиртами = полуацетали 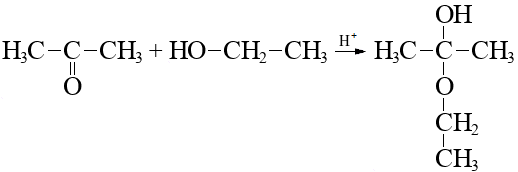 Восстановление до альдегидов и кетонов до спиртов водородом Жесткое окисление альдегидов до кислот Серебряное зеркало Окисление альдегидов до кислот (с бромом аналогично) 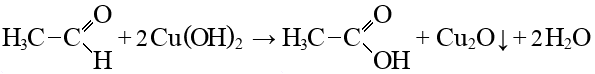 Карбоновые кислоты: Номенклатура Муравьиная (формиаты) – С1 Уксусная (ацетаты)- С2 Пропионовая (пропионаты) – С3 Масляная (бутираты) – С4 Бензойная (бензоаты) –С7 Пальмитиновая (пальмитаты) - предельная Стеариновая (среараты) – предельная Щавелевая (оксалаты) - Двухосновная С2 Малоновая (малонаты) - Двухосновная С3 Фталевая (фталаты) – Двухосновная С7 (бензольное кольцо) Акриловая (акрилаты) Олеиновая – непредельная Линолевая – непредельная Линоленовая – непредельная Кислотно-основное взаимодействие как обычные кислоты с металлами, основными оксидами, основными гидроксидами Галогенирование 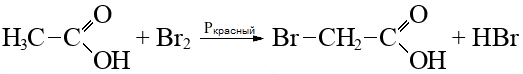 Получение ангидридов 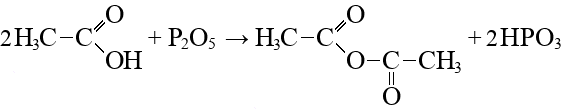 У кислот с кратной связью реакции присоединение против правила Марковникова!! Особые свойства муравьиной кислоты: 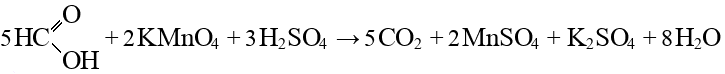 Окисление гидроксидом меди до углекислого газа 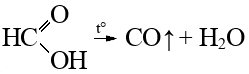 Простые эфиры: Кислотное расщепление Сложные эфиры: Восстановление 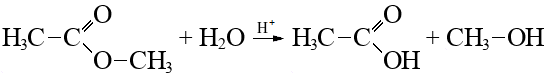 Омыление Амины: Получение: Аммонолиз Восстановление Гидрирование нитросоединений Свойства: С азотистой кислотой Со спиртами С галогеналканами и щелочью 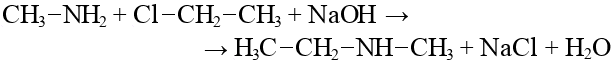 |
