Принцип Ле Шателье. Правила увеличение объема сосуда, уменьшает давление ( гидролиз это эндотермический процесс )
 Скачать 0.61 Mb. Скачать 0.61 Mb.
|
|
ПРИНЦИП ЛЕ ШАТЕЛЬЕ ПРАКТИКА ПО 22 заданию ПРАВИЛА - увеличение объема сосуда, уменьшает давление ( ГИДРОЛИЗ – это эндотермический процесс) Для реакций гидролиза тепловой эффект реакции могут не указывать, но Вы должны помнить, что гидролиз это эндотермический процесс. Разбавление усиливает диссоциацию слабых электролитов (закон разбавления Оствальда). Внесение веществ Если вам все же достанется добавление твердого вещества в качестве воздействия на равновесную систему, помните: Твердое нерастворимое вещество не влияет на равновесие. Твердое растворимое вещество диссоциирует на ионы. Увеличение концентрации ионов может повлиять на равновесие. Твердое растворимое вещество может взаимодействовать с одним из участников реакции. В таком случае равновесие сместится в сторону протекания реакции. Добавление инертного газа, которого нет в реакции, не влияет на смещение равновесия Если реакция записана в виде ионов, а мы добавляем вещество, то алгоритм следующий Разбиваем вещество на ионы , например КОН – К+ и ОН - , если такие ионы есть в реакции, то мы увеличиваем их концентрацию. Если таких ионов в реакции нет, то мы ищем вещество в реакции, которое может прореагировать с добавляемым веществом, тогда равновесие сместится в сторону протекания реакции. Давайте рассмотрим примерное задание:  Как бы Вы ответили на эти вопросы? А - увеличение объема сосуда, уменьшает давление, равновесие смещается в сторону исходных веществ (ответ 2). Б - повышение давления, равновесие смещается в сторону продуктов реакции (ответ 1). В - внесение оксида фосфора (V) - как бы Вы ответили на этот вопрос? Р2О5 - нет в уравнении реакции, почему же его внесение должно влиять на смещение равновесия? Но оно повлияет, да еще как! Давайте проанализируем с каким веществом в реакционной смеси может реагировать оксид фосфора (V), ответ очевиден - с водой (Р2О5 сильное водоотнимающее средство). То есть внесение Р2О5 ведет за собой уменьшение концентрации одного из реагентов (Н2О), и равновесие смещается в строну продуктов реакции (ответ 1). Г - понижение концентрации SO2 смещает равновесие в сторону исходных веществ (ответ 2). Еще примеры:  Здесь рассмотрим только пункт Г - добавление гидроксида натрия. Гидроксид натрия реагирует только с NO2, уменьшая его концентрацию в реакционной системе, поэтому равновесие смещается в сторону прямой реакции (ответ 1). Другой пример: 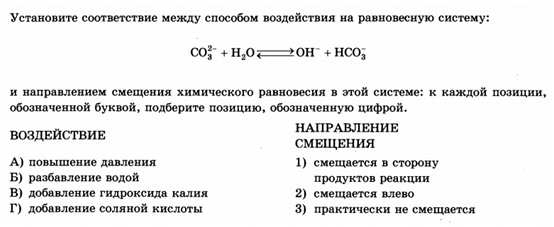 Здесь рассмотрим пункты В и Г. Пункт В - добавление гидроксида калия равнозначно добавлению ионов ОН- так как это сильный электролит, поэтому равновесие сместится в сторону исходных веществ (ответ 2). Пункт Г - добавление соляной кислоты обратно по влиянию добавлению гидроксида калия, так как ионы ОН- связываются ионами Н+ (соляной кислоты) в малодиссоциированное вещество - воду и поэтому равновесие сместится в сторону продуктов реакции (ответ 1). И еще один, последний пример:  Для такого задания лучше всего записать уравнение диссоциации: СН3СООН = СН3СОО(-) +Н(+) Пунк А - добавление ацетата натрия: СН3СООNa = СН3СОО(-) + Na(+), то есть добавление ацетат иона ( СН3СОО(-)), равновесие смещается в сторону обратной реакции (ответ 2). Пунк В - добавление газообразного НСl в водный раствор даст нам соляную кислоту: НСl = H(+) + Cl(-), равновесие смещается в сторону обратной реакции (ответ 2). Пунк Г - разбавление раствора. Разбавление усиливает диссоциацию слабого электролита (закон разбавления Оствальда). То есть, при разбавлении равновесие сместится в сторону прямой реакции (ответ 1). А вот задания для самостоятельного решения:      Влияние других веществ, не участвующих в реакции Прибавление веществ не участвующих в реакции, но взаимодействующих с реагентами или продуктами реакции: Для реакции: добавление Н2SO4(конц.) (сильное водоотнимающее средство) снижает концентрацию Н2О(ж). Равновесие смещается вправо. Добавление NaOH снижает концентрацию CH3COOH(ж), так как образуется соль - ацетат натрия. Равновесие смещается влево. Прибавление веществ, несущих одноименный ион. Для реакции: добавление НCl увеличивает концентрацию ионов H(+). Равновесие смещается влево. Добавление катализатора (ингибитора) Катализаторы (ингибиторы) не приводят к смещению равновесия, а только ускоряют (замедляют) достижение состояния равновесия.  А - повышение давления смещает равновесие в сторону образования меньшего количества моль газов. Смотрим на уравнение реакции и видим, что у нас слева 3 моль газа (Н2) и справа 3 моль газа (Н2О (г)), поэтому равновесие практические не смещается. (ответ 3) Б - добавление катализатора не смещает равновесие. (ответ 3) В - увеличение концентрации паров воды приводит к увеличению концентрации одного из продуктов, поэтому равновесие сместиться в сторону их расходования, то есть в сторону обратной реакции. ( ответ 2) Г - измельчение железа, твердого вещества - не смещает равновесие. (ответ 3)  Другой пример: А - повышение давления не влияет на смещение равновесия в растворе. (ответ 3). Б - добавление твердого гидроксида натрия в раствор приведет к его растворению. В растворе гидроксид натрия прореагирует с соляной кислотой. Таким образом равновесие сместится в сторону прямой реакции, так как уменьшается концентрация одного из продуктов реакции. (ответ 1) В - увеличение температуры приводит к усилению гидролиза. (ответ 1) Для реакций гидролиза тепловой эффект реакции могут не указывать, но Вы должны помнить, что гидролиз это эндотермический процесс. Г - разбавление или увеличение концентрации воды приводит к смещению равновесия в сторону прямой реакции. ( ответ 1) Третий и последний пример:  А - введение инертного газа при постоянном объеме не влияет на смещение равновесия. (ответ 3) Б - уменьшение концентрации бутадиенасмещаетравновесие в сторону прямой реакции, так как уменьшается концентрация одного из продуктов. (ответ 1) В - увеличение температуры приводит к смещению равновесия в сторону эндотермической реакции, то есть в сторону прямой реакции. (ответ 1) Г - понижение давления смещает равновесие в сторону образования большего числа моль газа, то есть в сторону прямой реакции, в ходе которой образуется 3 моль газа. ( ответ 1) А вот некоторые задания для самостоятельного решения:      1. Задаемся вопросом, твердое вещество растворимо в воде или нет? 2а. Если ответ нет, то оно никакого влияния на реакционную смесь не окажет, а выпадет в осадок. 2б. Если ответ да, то мы задаем себе второй вопрос: реагирует ли это вещество с одним из участников предложенной реакции (рассматриваем и реагенты, и продукты. Ведь реакция обратимая!) Равновесие сместится в сторону, где и произойдет эта химическая реакция. 3. Но и это еще не все. Если задана реакция в ионном виде, то при добавлении твердого растворимого вещества происходит его диссоциация (распад на ионы) и увеличивается концентрация ионов. А увеличение концентрации ионов смещает равновесие в сторону их меньшего содержания. Установите соответствие между видом воздействия на равновесную систему и направлением смещения химического равновесия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. CO32- + H2O ⇄ HCO3— + OH— — Q
А) Добавление кислоты. Видим, что в нашей реакции нет никакой кислоты. Будет ли изменяться равновесие в системе? Конечно, ведь кислота всегда реагирует со щелочью, а за щелочь в реакции отвечают гидроксид-ионы. Равновесие смещается в сторону протекания реакции, то есть вправо. Б) Повышение температуры смещает равновесие в сторону эндотермической реакции, то есть туда, где теплоты меньше. В сторону прямой реакции. В) Катализатор не влияет на положение равновесия. Г) Разбавление раствора – это то же самое, что и добавление воды. А увеличение концентрации реагента смещает равновесие в сторону образования продуктов. Ответ: 1131. Светлана Вдовицкая Страница |
