Аналитическая часть Историческая справка о методах получения и использования
 Скачать 1.14 Mb. Скачать 1.14 Mb.
|
|
Содержание Введение Аналитическая часть Историческая справка о методах получения и использования продукта Химизм процесса Влияние различных факторов на процесс окисления изопропилбензола Патентные исследования Расчетно-технологическая часть Функциональная схема производства ГПИПБ 2.1.2 Операторная схема производства Описание принципиальной схемы производства 2.2 Техническая характеристика сырья, продуктов Требования к составу и чистоте сырья Характеристика целевого продукта Материальный баланс Теоретический материальный баланс Практический материальный баланс Технико-экономические показатели Тепловой баланс Расчет теплофизических величин веществ по Бенсону Расчет теплового баланса Расчет окислительной колонны Автоматизированная система управления производством Безопасность и экологичность работы Заключение Список использованных источников Введение Фенол и ацетон являются важнейшими крупнотоннажными продуктами промышленности органического и нефтехимического синтеза. Фенол широко применяется в производстве неионогенных моющих средств, присадок к маслам и топливам, пластических масс и синтетических волокон и т. д. Ацетон является одним из широко применяемых растворителей. Его используют в производстве химических волокон, в экстракционных процессах, при очистке масел. Совместное их получение гораздо более экономичнее всех ранее реализованных методов, вследствие чего оно нашло широкое применение во всех промышленно развитых странах мира. Первое крупное производство фенола и ацетона кумольным методом было реализовано в 1949 году в Советском Союзе. В основу этого производства были положены исследования П.П Сергеева, Б.Д. Кружалова и Р.Ю. Удриса по окислению изопропил бензола в гидроперекись с последующим её разложением на фенол и ацетон[1]. Процесс производства фенола и ацетона кумольным методом складывается из следующих стадий: 1. Алкилирование бензола пропиленом. 2. Окисление изопропилбензола в гидроперекись. 3. Выделение гидроперекиси изопропилбензола. 4. Разложение технической гидроперекиси изопропилбензола серной кислотой. 5. Нейтрализация реакционной массы после разложения. 6. Ректификация реакционной массы после разложения и выделение товарных фенола и ацетона. Наиболее важной стадией кумольной технологии фенола является окисление кумола до его гидропероксида (ГПК), так как именно на этой стадии образуются основные и побочные продукты производства. Побочные продукты в дальнейших стадиях участвуют в разнообразных реакциях, тем самым усложняют производство. Аналитическая часть Историческая справка о методах получения и использования продукта Изопропилбензол, или кумол, С6Н5СН (СН3)2 был впервые получен сухой перегонкой кальциевой соли или бариевой соли куминовой (n- изопропилбензойной) кислоты. Впоследствии его обнаружили в продуктах сухой перегонки каменного угля. Строение кумола установили Р.Фиттинг и его ученики, а классический синтез по Вюрцу-Фиттингу взаимодействием йодистого изопропилбензола, бромбензола и натрия провёл О.Якобисен. в 1895 году был осуществлён синтез изопропилбензола из бензола и пропилена при помощи безводного хлористого алюминия в жидкой фазе. Изопропилбензол в обычных условиях - бесцветная легкоподвижная жидкость с приятным запахом, при большом разведении, напоминающем запах древесины хвойных пород. Несмотря на то, что химические методы получения изопропилбензола разработаны давно, промышленное производство его впервые было начато лишь во время второй мировой войны в СССР и США. В то время изопропилбензол целиком использовался в качестве высокооктановой добавки к авиационным бензинам. В промышленности органического синтеза изопропилбензол стал применяться совсем недавно как исходный продукт для получения фенола и ацетона, а также в производстве а-метилстирола. Известны три метода получения изопропилбензола, имеющие промышленное значение: 1.Алкилирование бензола пропиленом в присутствии безводного хлористого алюминия (алкилирование по Фриделю-Крафтсу). 2.Алкилирование бензола пропиленом в паровой фазе с применением фосфорнокислотного катализатора. 3.Алкилирование бензола пропиленом в жидкой фазе в присутствии серной кислоты как катализатора. В России изопропилбензол производят главным образом алкилированием по Фриделю-Крафтсу[3] Процесс является жидкофазным и протекает с выделением тепла. Можно предложить три типа реактора для проведения данного процесса. Наиболее простым является трубчатый аппарат, в нижней части которого размещается мощная мешалка, предназначенная для эмульгирования катализаторного раствора и реагентов.  Бензол и олефины,а также катализаторный раствор подают в нижнюю часть реактора. Эмульсия поднимается вверх по трубам, охлаждается за счет воды, которая подается в межтрубное пространство. Алкилаты (продукты синтеза),непрореагировавшие бензол и олефины, и катализаторный раствор выводятся в верхней части реактора и поступают в сепаратор. Там происходит отделение катализаторного раствора от остальных продуктов(алкилата).Катализаторный раствор возвращается в реактор, а алкилаты направляются на разделение. Основное количество изопропилбензола за рубежом производят этим же способом на гетерогенном фосфорнокислом катализаторе при 200°С и давлении 2,8–4,2 МПа. Для получения фенола и ацетона в настоящее время производится свыше 17 млн. т. в год изопропилбензола. Фирмой UOP в 1996 г. был осуществлен синтез изопропилбензола из бензола и пропилена на основе гетерогенного катализатора — бета-цеолите (каталитическая система QZ-2000), обладающего высокой кислотностью. Селективность продукта составляет 99,7% (мас.). Производительность установки составляет от 350 до 700 тыс. т кумола в год. Изопропилбензол используется для производства гидропероксида изопропилбензола и α-метилстирола:  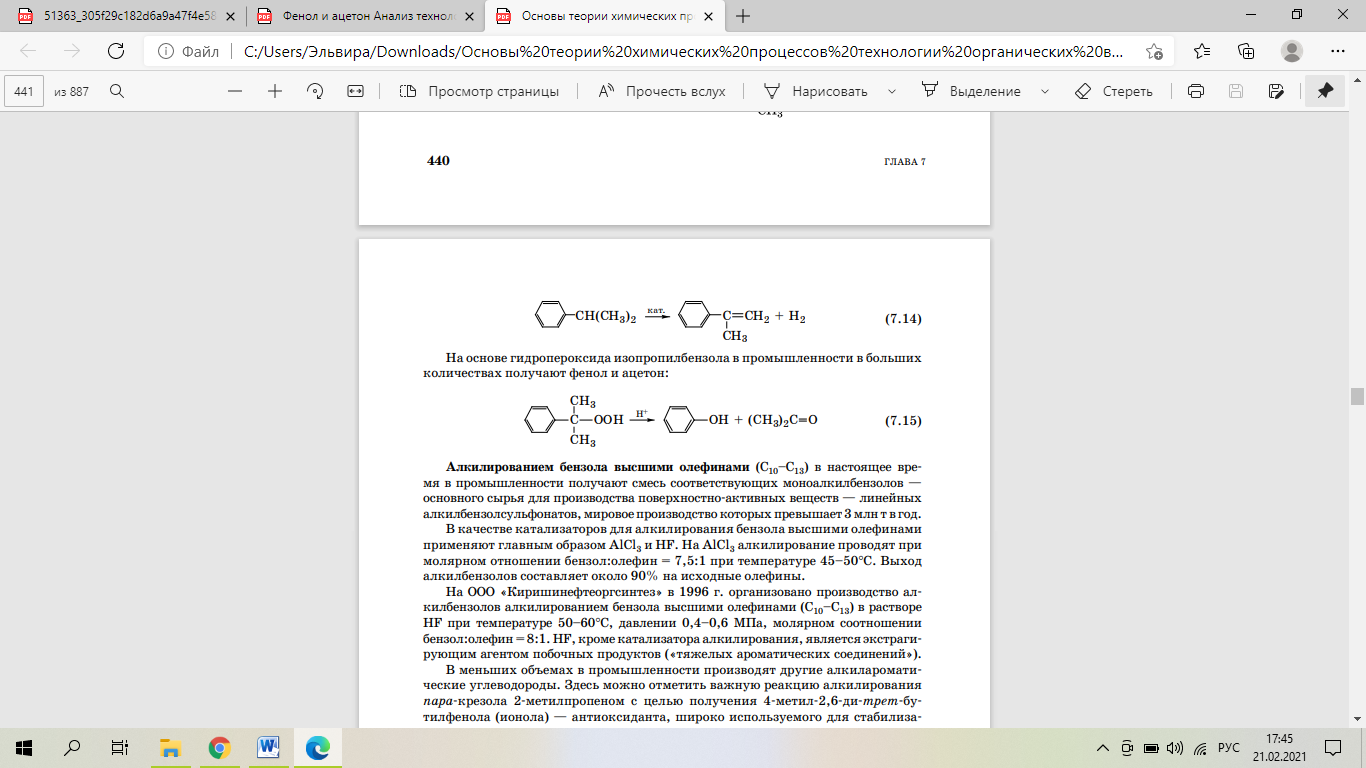 На основе гидропероксида изопропилбензола в промышленности в больших количествах получают фенол и ацетон:  Химизм процесса Гидропероксиды - это первичные молекулярные продукты окисления углеводородов. Они относятся к числу довольно нестабильных соединений, превращающихся при окислении в другие продукты. Поэтому их концентрация в реакционной массе, особенно при каталитическом окислении или при повышенных температурах, невелика. Наиболее нестабильны первичные гидропероксиды и, наоборот, относительно стабильны третичные гидропероксиды, которым, собственно и является гидропероксид изопропилбензола. Процесс окисления углеводородов, как и всякий цепной процесс, включает в себя по крайней мере три реакции: зарождение (инициирование), рост и обрыв цепи.[4] Реакция зарождения цепи связана с разрывом С—Н-связи в валентнонасыщенной молекуле окисляемого углеводорода RH: Однако энергия разрыва связи С—Н обычно составляет 335000—418 700 кдж/кмоль (80—100 ккал/моль) и, следовательно, в условиях жидкофазного окисления такой разрыв самопроизвольно не происходит. Он может наблюдаться при столкновении молекулы RH с какой-либо активной частицей А: или при поглощении кванта световой энергии в случае фотохимического окисления: В настоящее время принято, что реакция зарождения цепи при окислении углеводородов кислородом протекает по схеме: которая является наиболее энергетически выгодной так как требует затраты энергии на 196 900 кдж/кмоль (47 ккал/моль) меньше, чем процесс образования радикалов Re путем распада молекулы по связи С—Н32. Рост цепи при наличии в системе радикалов происходит таким образом: 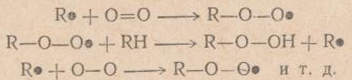 Возникает более или менее длинная реакционная цепь, в результате чего значительная часть молекул исходного углеводорода может превратиться в гидроперекись. Обрыв цепи происходит вследствие различных причин, основные из которых следующие: рекомбинация свободных радикалов, обрыв цепи на стенках реактора и взаимодействие свободных радикалов с примесями, являющимися ингибиторами. Реaкция окисления изопропилбензола: 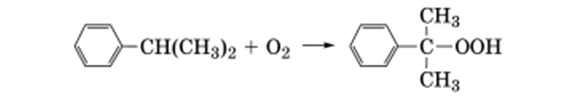 Протекает по механизму сложных цепных реакций с вырожденным рaзветвлением цепи. Пaрaллельно с основным продуктом обрaзуются побочные продукты, тaкие кaк диметилфенилкaрбинол, aцетофенон, мурaвьинaя кислотa и в незнaчительной степени пероксидные продукты типa дикумилпероксидa, поэтому получить 100%-ную селективность по гидропероксиду невозможно[3]. В нaстоящее время в промышленных условиях селективность стaдии окисления изопропилбензолa по гидропероксиду состaвляет 91-95%(мол.). Дaннaя селективность получaется блaгодaря конструктивному оформлению реaкторa, использовaнию оптимaльных концентрaций гидропероксидa в реaкционной мaссе (15-25%), оптимaльной темперaтуре (100-120℃) и нaиболее aктивному кaтaлизaтору. Окисление можно проводить как в жидкой, так и в пaровой фaзе нa рaзных кaтaлизaторaх. В кaчестве кaтaлизaторов процессa,проходящего в жидкой фaзе при темперaтурaх выше 100℃ (100-120℃), нaиболее широко применяются резинaты и нaфтенaты кобaльтa и мaргaнцa.Тaкже используют и инициaторы, нaпример сaми гидропероксиды, которые добaвляют в шихту в количестве 2,5-3,5%. Обрaзующийся гидропероксид изопропилбензолa чaстично подвергaется термическому рaзложению. Скорость рaспaдa гидропероксидa с повышением темперaтуры увеличивaется. Диметилфенилкaрбинол, aцетофенон и метиловый спирт являются основными продуктaми рaспaдa гидропероксидa изопропилбензолa.  С6Н5(СН3)2СООН С6Н5(СН3)2СОН С6Н5(СН3)2СООН С6Н5(СН3)2СОН С6Н5(СН3)2СООН С6С5СОСН3+СН3ОН С6Н5(СН3)2СООН С6С5СОСН3+СН3ОНИнгибитором процессa окисления изопропилбензолa является обрaзующийся метaнол,который окисляется в формaльдегид и мурaвьиную кислоту.Кaк уже отмечaлось,нa выход гидропероксидa влияют темперaтурa и продолжительность окисления (рис.1.1).Скорость реaкции будет уменьшaться при чрезмерном понижении темперaтуры.Из рисункa видно,что зa 1 чaс при t=120℃ выход гидропероксидa состaвляет 8-10,a при t=100℃ - 2 -3 %(мaс.). Р  ис.1.1 Зависимость содержания гидропероксида в реакционной массе от продолжительности окисления при различной температуре. ис.1.1 Зависимость содержания гидропероксида в реакционной массе от продолжительности окисления при различной температуре.Рaспaд гидропероксидa нaчинaет зaметно протекaть при его концентрaции в реaкционной мaссе 18% и выше.При повышенных темперaтурaх его рaспaд сопровождaется взрывом.В оксидaте содержится от 0,5 до 5% продуктов рaспaдa при оптимaльной концентрaции пероксидa. Щелочнaя средa (pH=7,5) блaгоприятствует процессу окисления,потому что нейтрaлизуются кислоты-ингибиторы,которые обрaзуются в процессе окисления.Пaрaллельные реaкции нейтрaлизaции позволяют ускорять основную реaкцию и в этом случaе осуществляется совмещенный процесс. Из-зa этого окисление иногдa ведут кислородом воздухa в водно-щелочной эмульсии (1%-ный рaствор Na2CO3) при интенсивном перемешивании и в присутствии поверхостно-активных веществ. Исходя из вышесказанного, процесс окисления проводят чаще всего при 120-130℃, Р=0,5-1 Мпа, рН=8,5-10,5.При таких условиях конечное содержание гидропероксида составляет около 25%. Обычно для проведения процесса окисления применяются реакторы колонного типа,с перемешивающим устройством (каскад реакторов);эрлифтового типа(рис.1.2)  Рис.1.2. Реакторы окисления:а- колонного типа;б-с перемешивающим устройством; в- эрлифтового типа Для отвода тепла в колонных аппаратах устанавливаются змеевики (отводится 1967 кДж на 1 кг превращенного изопропилбензола). Реактор колонного типа является компактным, в то время как каскад реакторов с перемешивающим устройством или каскад реакторов эрлифтового типа требуют большого количества арматуры.В таких реакторах управлять процессом сложно. Если учитывать,что в оксидате содержится около 25% пероксида,а для дальнейшей переработки нужно подавать концентрированный раствор,то концентрирование проводят в мягких условиях(при низких температурах в вакууме). Для этой цели наиболее широко применяют вакуумную ректификацию (чаще всего на двухколонной установке).Получаемый техничсекий гидропероксид имеет следующий состав ( в %): гидропероксид изопропил бензола – 90–91; диметилфенилкарбинол – 5-7; ацетофенон – 1,0-1,5; дикумилпероксид - 0,4–0,6; муравьиная кислота - 0,01–0,04. В зависимости от целей процесса (дальше получают только фенол и ацетон или фенол, ацетон и пропиленоксид) пероксид направляется на разложение или на эпоксидирование пропилена. Влияние различных факторов на процесс окисления изопропилбензола Процесс окисления изопропилбензола чрезвычайно чувствителен по отношению к целому ряду факторов. Особенно большое значение имеет чистота изопропилбензола. Присутствие в окисляемом изопропилбензоле даже следов некоторых веществ может существенно изменить скорость процесса. В качестве примера можно привести влияние тиофена и его производных, а также фенола на процесс окисления. Наличие этих продуктов в чистом изопропилбензоле вполне возможно: тиофен содержится в бензоле, идущем на приготовление изопропилбензола, а следы фенола (появляются в изопропилбензоле при его получении. Оба продукта в большой степени тормозят окисление изопропилбензола.[1] Этот и многие другие факторы, как правило, не учитываются в равной степени в опытах одних и тех же авторов, а тем более в работах, выполненных различными исследователями. В литературе опубликованы результаты опытов по окислению изопропилбензола при разнообразных скоростях накопления гидроперекиси и использовании сырья различного качества. Поскольку указанные опыты проводились по различной методике, то при оценке полученных данных можно легко допустить ошибку. Однако при тщательном анализе всех имеющихся в настоящее время экспериментальных данных удается обнаружить общие закономерности, свойственные процессу окисления чистого изопропилбензола. Сюда относится влияние температуры, глубины окисления, количества катализаторов, примесей некоторых веществ и других факторов (на выход и скорость накопления гидроперекиси. При окислении наиболее чистых образцов изопропилбензола скорость накопления гидроперекиси может достигать величины 10—13% в час, в то время как в промышленных условиях эта величина составляет 5—7% в час. Вначале протекает процесс зарождения цепи (индукционный период), затем скорость реакции резко возрастает и остается постоянной в течение некоторого промежутка времени, после чего происходит уменьшение скорости, вызванное увеличивающимся распадом гидроперекиси и торможением (процесса окисления продуктами ее распада). Добавка некоторого количества гидроперекиси к изопропилбензолу перед окислением позволяет избежать индукционного периода. Было показано, что средняя скорость накопления гидроперекиси с повышением температуры последовательно от 90 до100 °С, от 100 до 110°С и от 110 до 120 °С возрастает неодинаково (соответственно в 2,3, 1,8 и 1,1 раза). Установлено также, что при 120° С продукты распада в количестве более 1% можно обнаружить в реакционной массе через 1 ч после начала окисления; при 110 °С это происходит через 4—5 ч, а при 100 °С — через 6—8 ч. Существенное значение для получения оптимальных выходов гидроперекиси имеет степень конверсии изопропилбензола в гидроперекиси и продолжительность протекания процесса. В качестве обратимся к данным, полученным при окислении одного из образцов изопропилбензола при 110°С.Эти данные показывают, что для достижения высокого выход гидроперекиси при минимальном распаде необходимо ограничить глубину окисления изопропилбензола до содержания гидроперекиси 20—25%. Для других образцов изопропилбензола эта величина составляет 20—30%. В условиях жидкофазногоокисления дальнейшее увеличение содержания гидроперекиси в реакционной массе неизбежно приводит к повышенному содержанию продуктов ее распада и к снижению выхода. Поскольку целью процесса окисления изопропилбензола является получение гидроперекиси, то при выборе оптимальных условий процесса необходимо учитывать факторы, способствующие распаду гидроперекиси. С этой точки зрения следует тщательно подходить к выбору материалов для изготовления оборудования, применяющегося в производстве гидроперекиси, и к оценке схем технологического и аппаратурного оформления процесса. Так, многочисленные эксперименты показали, что лучшие результаты достигаются при окислении изопропилбензола в аппаратах, изготовленных из нержавеющей стали марки 1Х18Н9Т. В этом случае процесс протекает так же эффективно, как в стеклянном или эмалированном оборудовании. Как уже подчеркивалось, основным фактором, влияющим на процесс получения гидроперекиси с высоким выходом, является чистота изопропилбензола, подвергаемого окислению. Вредные примеси различных веществ, ингибирующих процесс окисления, могут попадать в реакционную зону из следующих источников: со свежим изопропилбензолом; с возвратным изопропилбензолом после отгонки его от гидроперекиси из реакционной смеси; в результате побочных реакций, протекающих в самом процессе окисления изопропилбензола; с воздухом, при помощи которого производится окисление изопропилбензола. Патентные исследования. Для выявления патентных документов был определен следующий предмет поиска: «способ получения гидропероксида изопропилбензола». Поиск патентной информации проводился по информационным электронным ресурсам базы данных ФИПС (http://www1.fips.ru). В процессе поиска за период с 2017 по 2021 год были обнаружены 5 патентных документов, максимально схожих с предметом поиска. Таблица 1 – Перечень отобранных патентных материалов
Патент № 2 659 403 «СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРОКСИДОВ АЛКИЛАРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ» Автор(ы):Курганова Екатерина Анатольевна (RU),Кошель Георгий Николаевич (RU),Петухов Александр Александрович (RU),Фролов Александр Сергеевич (RU) Патентообладатель(и): Общество с ограниченной ответственностью "Ярославские Химические Технологии" (RU) Дата регистрации:02.07.2018 Краткое описание: Описан способ получения гидропероксидов алкилароматических углеводородов в процессах совместного получения фенола (метилфенолов)и ацетона, стирола и пропиленоксида. Предложен способ получения гидропероксидов жидкофазным окислением алкилароматических углеводородов кислородом воздуха при атмосферном давлении, температуре процесса 100-140°С, в течение 0,5-1 часов, в присутствии в качестве катализатора N-гидроксифталимида, предварительно обработанного озоно-воздушной смесью, в количестве 1-3% масс. Технический результат заключается в повышении скорости накопления гидропероксидов в 1,5-2 раза при сохранении высокой селективности их образования (92-98%). Средством достижения технического результата является использование катализатора N-гидроксифталимида,который перед использованием обработан озоно-воздушной смесью. Патент № 2 696 444 «СПОСОБ ОЧИСТКИ АБГАЗОВ ПРОЦЕССА ОКИСЛЕНИЯ ИЗОПРОПИЛБЕНЗОЛА» Автор(ы): Гараев Тимур Талгатович (RU),Мингазов Алмаз Тагирзянович (RU), Фролов Владислав Владимирович (RU),Шайхов Ренат Лирамович (RU), Хайруллин Марат Гусманович (RU),Штатнов Дмитрий Владимирович (RU) Патентообладатель(и): Казанское публичное акционерное общество "Органический синтез" (RU) Дата регистрации:01.08.2019 Краткое описание: Способ очистки абгазов процесса окисления изопропилбензола в производстве фенола-ацетона кумольным методом, отличающийся тем, что абгазы проходят четырехстадийную очистку от органических примесей: на первой стадии абгазы при повышенном давлении пропускают через первый холодильник-сепаратор; на второй стадии частично охлажденные абгазы при повышенном давлении пропускают через второй холодильник-сепаратор; на третьей стадии абгазы при повышенном давлении пропускают через насадочную колонну; на четвертой стадии абгазы при атмосферном давлении пропускают через аппарат циклонного типа. 2. Способ по п.1, отличающийся тем, что в первом холодильнике-сепараторе в качестве хладагента используют оборотную воду. 3. Способ по п.1, отличающийся тем, что во втором холодильнике-сепараторе в качестве хладагента используют «холод минус 4°С». 4. Способ по п.1, отличающийся тем, что насадочная колонна состоит из двух секций, заполненных регулярной сегментной насадкой. Технический результат достигается за счет использования четырехстадийного способа очистки абгазов от изопропилбензола. Патент № 2 640 595 «СПОСОБ АЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ» Автор(ы): ХВАН Манон (US),ДЖОНСОН Дана Е. (US) Патентообладатель(и): БЭДЖЕР ЛАЙСЕНСИНГ ЭлЭлСи (US) Дата регистрации:10.01.2018 Краткое описание: Изобретение относится к двум вариантам способа алкилирования ароматических соединений. Один из вариантов включает: (a) предоставление исходного ароматического углеводородного сырья, содержащего алкилируемый ароматический углеводород, по меньшей мере 150 ч./млн по массе воды и по меньшей мере одну органическую азотную примесь, причем алкилируемый ароматический углеводород представляет собой бензол; (b) удаление воды из исходного ароматического углеводородного сырья в зоне обезвоживания с получением обезвоженного исходного ароматического сырья, имеющего содержание воды не более чем 20 ч./млн по массе; (c) контактирование обезвоженного исходного ароматического сырья с адсорбентом из глины в условиях, включающих температуру менее чем 130°С, так что адсорбент удаляет по меньшей мере часть органической азотной примеси, содержащейся в исходном сырье, с получением обработанного ароматического исходного сырья; и (d) подачу обработанного ароматического исходного сырья в реакционную зону алкилирования и/или реакционную зону трансалкилирования. Использование предлагаемого способа позволяет повысить эффективность очистки глиной. Патент № 2 639 706 «СПОСОБ ПОЛУЧЕНИЯ ИЗОПРОПИЛБЕНЗОЛА» Автор(ы): Нестерова Татьяна Николаевна (RU),Востриков Сергей Владимирович (RU),Мазурин Олег Анатольевич (RU) Патентообладатель(и): Федеральное государственное бюджетное образовательное учреждение высшего образования "Самарский государственный технический университет" (RU) Дата регистрации:22.12.2017 Краткое описание: Заявленный результат достигается тем, что в способе получения изопропилбензола алкилированием бензола пропиленом и переалкилированием полиалкилибензолов реакции алкилирования и переалкилирования проводят раздельно, причем реакцию алкилирования проводят в жидкой фазе с применением полимерного катализатора, имеющего только Бренстодовые кислотные центры, а для осуществления реакции переалкилирования в качестве катализатора применяют кислоту Льюиса, где в качестве катализатора переалкилирования используют каталитический комплекс на основе хлористого алюминия, при этом температура реакции алкилирования находится в интервале 50÷150°С, а температура реакции переалкилирования находится в интервале 30÷80°С, для алкилирования используют пропан-пропиленовую фракцию с содержанием пропилена 20÷100% масс. Технический результат достигается повышением эффективности процесса за счет проведения реакции алкилирования и переалкилирования в раздельных реакторах при оптимальном температурном режиме. Патент № 2 737 897 «СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА И СПОСОБ ПОЛУЧЕНИЯ ИЗОПРОПИЛБЕНЗОЛА С ИСПОЛЬЗОВАНИЕМ ЭТОГО КАТАЛИЗАТОРА» Автор(ы): Ечевский Геннадий Викторович (RU),Коденев Евгений Геннадьевич (RU) Патентообладатель(и): Федеральное государственное бюджетное учреждение науки "Федеральный исследовательский центр "Институт катализа им. Г.К. Борескова Сибирского отделения Российской академии наук" (ИК СО РАН, Институт катализа СО РАН) (RU) Дата регистрации:04.12.2020 Краткое описание: Изобретение относится к способу получения изопропилбензола в процессе алкилирования бензола пропиленом при температуре 170-230°C, давлении от атмосферного до 50 атм, мольном отношении бензол/пропилен в исходной смеси от 4:1 до 10:1, весовой скорости подачи исходной смеси от 0,2 до 10 ч-1 с использованием катализатора на основе цеолита Бета, приготовленного контактированием цеолита Бета с раствором нитрата аммония для удаления соединений натрия и переведения цеолита в водородную форму, с последующими стадиями грануляции со связующим, сушки и прокаливания гранул, причем цеолит Бета перед грануляцией со связующим предварительно подвергают обработке раствором хелатирующего агента, а затем обрабатывают перегретым водяным паром при температуре не выше 550°С в течение не менее 2 ч, в качестве хелатирующиего агента применяют сульфосалициловую кислоту, этилендиаминтетрауксусную кислоту ЭДТА, сульфобензойную кислоту, 3-гидроксинафталин-1,4-дисульфокислоту. Технический результат заключается в увеличении длительности межрегенерационного пробега катализатора Список использованных источников 1. Кружалов, Б. Д. Совместное получение фенола и ацетона / Б. Д. Кружалов, Б. И. Голованенко. М.: Госхимиздат, 1963. - 200 с. 2. Закошанский, В. М. Кумольный процесс получения фенола и ацетона / В. М. Закошанский // Нефтехимия. 2007. - Т.47. - №4. - С. 301-303. 3.Тимофеев, В.С. Серафимов, Л.А. Принципы технологии основного органического и нефтехимического синтеза.-2-е изд.,перераб.-М.:Высш.шк.,2003.-536с.:ил. 4. Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза: Учебник для ВУЗов.4-е изд., - М. Химия,1988-592 с. |
