Тема 25. Ароматические диазо- и азосоединения. Ароматические диазо и азосоединения
 Скачать 314.31 Kb. Скачать 314.31 Kb.
|
|
Ароматические диазо- и азосоединения Классификация. Номенклатура. Формы диазосоединений. Таутомерные превращения. Способы получения. Физические свойства и строение. Химические свойства: реакции, идущие с выделением азота (нуклеофильное и радикальное замещение диазониевой группы); реакции, идущие без выделения азота (восстановление до арилгидразинов); реакции азосочетания, их маханизмы. Значение азосоединений. Понятие об азокрасителях. Восстановительное расщепление азосоединений. АРОМАТИЧЕСКИЕ ДИАЗО- И АЗОСОЕДИНЕНИЯ Ароматические диазосоединения Ароматические диазосоединения – соединения с общей формулой Ar-N2X, в молекулах которых содержится группа из двух атомов азота – азогруппа (-N=N-), связанная одновременно с ароматическим радикалом Ar и Х – кислотный остаток или гидроксильная группа. Классификация и номенклатура Связь N-X в диазосоединениях может быть ионной или ковалентной, что зависит от природы кислотного остатка (Х). 1) Если Х – анион сильной кислоты, то связь носит ионный характер и такие соединения называются солями диазония. Соли диазония называют добавляя к названию органического радикала слово диазоний, а затем название аниона (допускается название аниона ставить впереди): 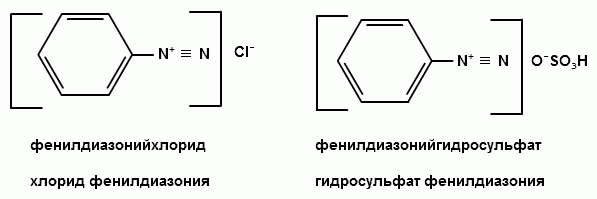 2) Если Х – анион слабой кислоты или гидроксильная группа, то образуется ковалентная связь. Такие соединения называют, добавляя к названию органического радикала - диазо, а затем название группы Х (цианид, хлорид): 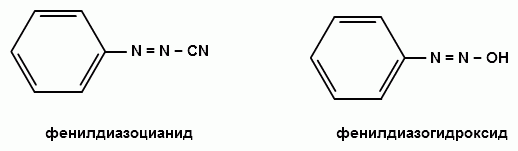 Строение диазосоединений с ионной связью Ароматические соли диазония в отличие от алифатических являются более устойчивыми соединениями. Относительная устойчивость ароматических солей диазония объясняется устойчивостью катиона арилдиазония. Катион арилдиазония является сопряженным ионом, в котором происходит сильное взаимодействие между π-электронной системой бензольного кольца и тройной связью диазониевой группы: 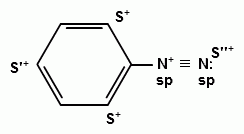 Оба атома азота находятся в состоянии sp-гибридизации, при этом один из них имеет положительный заряд. Это вызывает электронное смещение в диазониевой группировке, в результате второй атом азота приобретает частичный положительный заряд (δ”+). Диазониевая группа проявляет –I и –M-эффекты и является очень сильным ориентантом второго рода. Диазониевая группа принадлежит к самым сильным электроноакцепторным группам (она оказывает даже больший эффект, чем нитрогруппа). Диазосоединения с ковалентной связью Атомы азота в диазосоединениях с ковалентной связью находятся в состоянии sp2-гибридизации и соединены друг с другом двойной связью. При этом две гибридные орбитали каждого из атомов участвуют в образовании σ-связей, а на третьей располагается неподеленная электронная пара. Негибридизованные рz-орбитали атомов азота располагаются перпендикулярно плоскости молекулы и участвуют в образовании π-связи, а также участвуют в сопряжении с бензольным кольцом с образованием единой сопряженной системы. 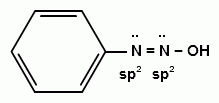 В результате такого строения диазосоединения с ковалентной связью могут существовать в виде цис-(син-) и транс-(анти-) изомеров. Более стабильной является транс-форма. 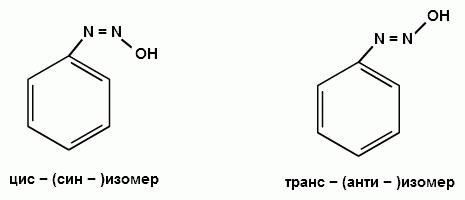 Образование диазогидроксида объясняется тем, что при взаимодействии диазокатиона с гидроксильным ионом положительный заряд полностью смещается к крайнему атому азота и между ним и гидроксильной группой возникает ковалентная связь: [ Ar – N ≡ N ]+ + OH- → Ar – N = N – OH диазокатион диазогидроксид Диазогидроксиды в свободном виде не выделены. В водных растворах они проявляют амфотерные свойства: при действии кислот они дают соли диазония, при действии щелочей – диазотаты: 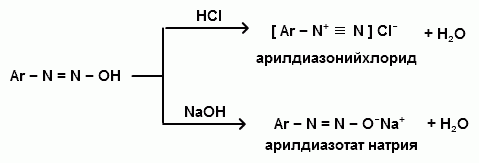 Изменение строения диазосоединений в зависимости от рН-среды В водных растворах различной кислотности диазосоединения находятся в сложном кислотно-основном и таутомерном равновесии. Изменение рН-среды в щелочную сторону приводит к превращению арилдиазонийхлорида в арилдиазонийгидроксид. Довольно быстро ионная связь между гидроксид-ионом и катионом арилдиазония превращается в ковалентную с образованием цис-арилдиазогидроксида. В присутствии избытка щелочи (рН > 7) цис-арилдиазогидроксид переходит в цис-арилдиазотат натрия, который в щелочном растворе при нагревании переходит в более устойчивый транс-арилдиазотат натрия, который может быть выделен в твердом виде. Как более устойчивую форму транс-арилдиазотат натрия используют для получения солей диазония: при подкислении транс-арилдиазотат натрия превращается в транс-арилдиазогидрогидроксид, который затем переходит в арилдиазонийхлорид. 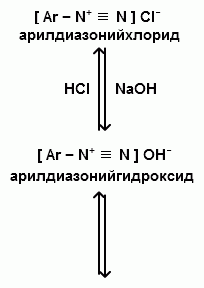 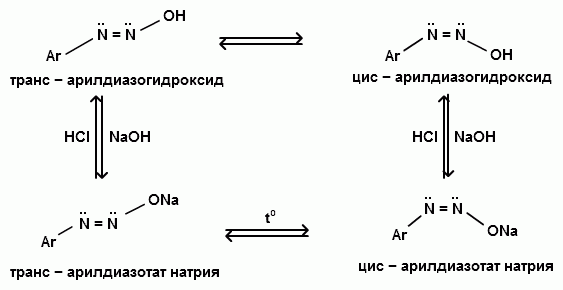 Ароматические азосоединения Ароматические азосоединения – органические вещества, в молекулах которых содержится азогруппа -N = N-, связанная с двумя ароматическими радикалами. Простейшим представителем ароматических азосоединений является азобензол, являющийся основной группировкой азокрасителей: 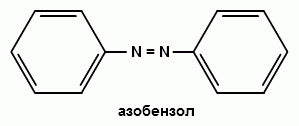 Многие азокрасители используются в качестве индикаторов, так как их окраска может меняться в зависимости от рН-среды. Строение азосоединений По строению азосоединения напоминают диазосоединения с ковалентной связью. Атомы азота в азогруппе находятся в состоянии sp2-гибридизации, при этом две гибридные орбитали каждого из атомов участвуют в образовании σ-связей, а на третьей располагается неподеленная электронная пара. Негибридизованные рz-орбитали атомов азота располагаются перпендикулярно плоскости молекулы и участвуют в образовании π-связи, а также участвуют в сопряжении с бензольными кольцами с образованием единой сопряженной системы. В результате такого строения азосоединения могут существовать в виде цис- и транс-изомеров. Более стабильной является транс-форма. 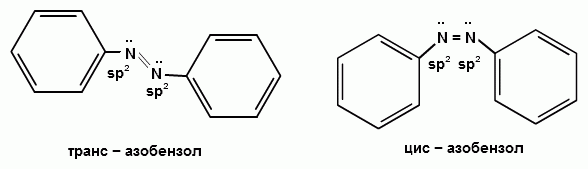 Способы получения 1. Реакция диазотирования Реакция диазотирования первичных ароматических аминов азотистой кислотой открыта П. Гриссом в 1858 г. Реакция протекает в присутствии нитрита натрия (или калия) и минеральной кислоты (азотистая кислота неустойчива). Так как реакция диазотирования является экзотермической, а диазосоединения легко разлагаются при нагревании, поэтому реакцию проводят при температуре 0-50С. 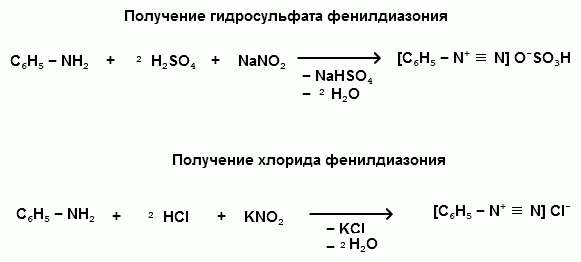 Соли диазония представляют собой твердые вещества. В индивидуальном виде их выделяют крайне редко, поскольку в твердом виде они очень взрывоопасны. Поэтому, после проведения реакции диазотирования полученный раствор соли арилдиазония используют в дальнейших превращениях для получения самых разных ароматических соединений. Соли арилдиазония при подщелачивании превращаются в арилдиазогидроксиды, а затем в арилдиазотаты натрия. При подкислении протекает обратная реакция: 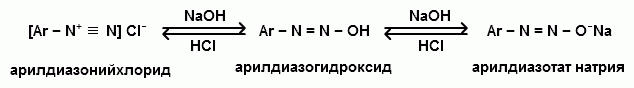 В реакции с алифатическими аминами не удается получить соль диазония, поскольку по мере образования она тут же превращается в спирт. Механизм реакции диазотирования 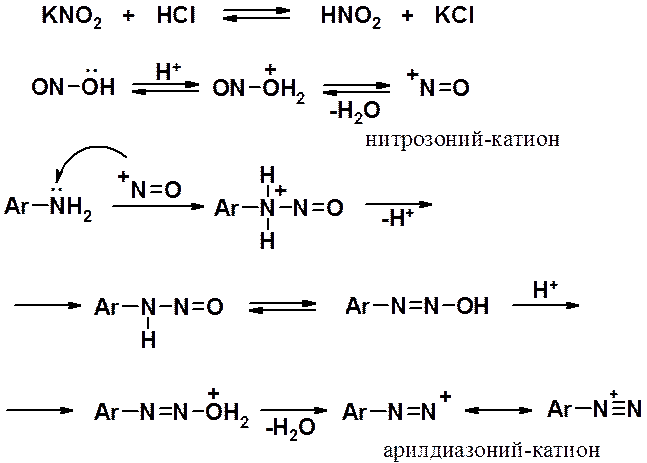 Химические свойства Многочисленные реакции, в которые вступают соли диазония можно разделить на две большие группы: 1) реакции, идущие с выделением азота; 2) реакции. Идущие без выдения азота. 1. Реакции солей диазония с выделением азота Эти реакции широко используются для получения ароматических соединений различных классов. При этом диазогруппа замещается различными атомами и группами атомов (У): В основе этих превращений лежит легкость отщепления диазогруппы и большая стабильность молекулы выделяющегося азота. В зависимости от условий реакций и характера реагирующих веществ замещение может протекать по гомолитическому или гетеролитическому механизм 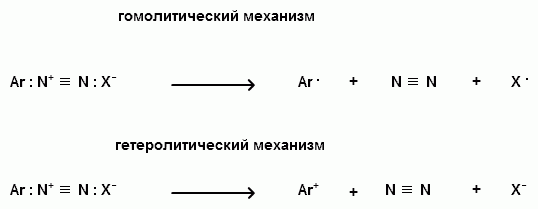 1) Замещение диазогруппы на гидрокси-группу (алкокси-группу) Образование фенолов При кипячении кислых растворов солей диазония выделяется азот и образуются фенолы: Лучше всего применять для этой цели соли серной кислоты, так как с другими кислотами могут происходить побочные явления. Замещение диазогруппы протекает по механизму SN1. На первой стадии происходит гетеролитическое расщепление связи C-N, выделяется азот и образуется арил-катион. На второй стадии арил-катион взаимодействует с водой с образованием фенола: 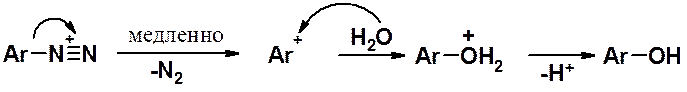 Образование эфиров фенолов Аналогично, по гетеролитическому механизму, в водном растворе спирта диазогруппа замещается на алкокси-группу с образованием простых эфиров: 2) Замещение диазогруппы на иод При нагревании солей диазония с иодидом калия диазогруппа замещается иодом: Из всех галогенов иод обладает самой низкой реакционной способностью в реакциях электрофильного замещения, поэтому замещение диазогруппы на иод является одним из основных методов получения иодпроизводных ароматического ряда. Реакция протекает по радикальному механизму, что обусловлено легкой окисляемостью аниона иода: 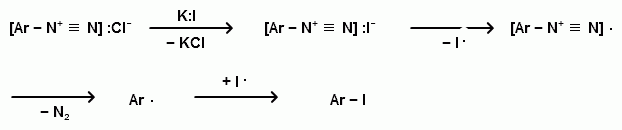 3) Замещение диазогруппы на другие атомы или группы атомов (реакция Гаттермана-Зандмейера) Замещение диазогруппы на другие атомы или группы атомов требует применения в качестве катализаторов соответствующих солей меди (1): 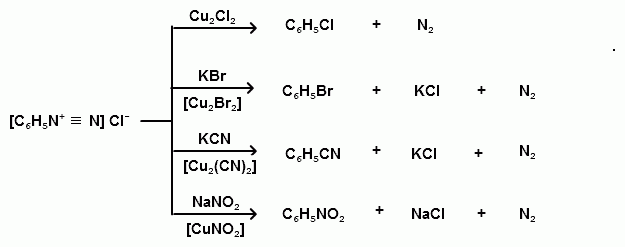 Механизм реакции Реакция протекает по радикальному механизму. Каталитическое действие солей меди связано с тем, что они способствуют образованию арильных радикалов: 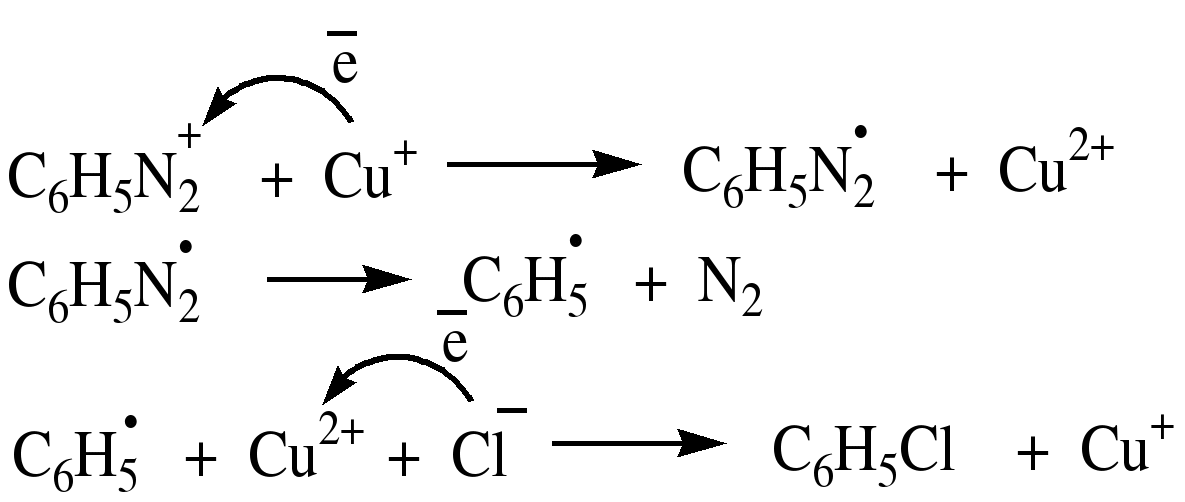 4) Получение фторпроизводных ароматических углеводородов (реакция Шимана) Нагревание фторборатных солей диазония является лучшим методом введения фтора в ароматическое кольцо. Тетрафторбораты обычно получают обработкой раствора хлорида фенилдиазония раствором тетрафторбората натрия:  Термическое разложение по гетеролитическому механизму тетрафторборатов диазония приводит к фтораренам: 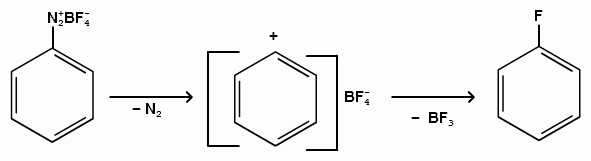 Реакция протекает по механизму SN1аром. В отличие от реакций Гаттермана-Зандмейера промежуточной частицей здесь является не радикал, а арильный катион. 5) Получение металлорганических соединений (реакция Несмеянова) Металлорганические соединения получаются действием металлических порошков на двойные соли диазония: 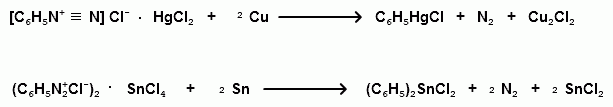 6) Реакция Меервейна 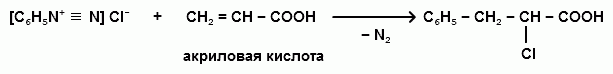 7) Реакция Гомберга Одним из способов получения производных дифенила является реакция Гомберга, заключающаяся во взаимодействии соли диазония с ароматическими углеводородами в присутствии щелочи:  8) Замещение диазогруппы на водород Для замещения диазогруппы на водород могут быть использованы следующие восстанавливающие агенты: - восстановление фосфорноватистой кислотой: - восстановление щелочным раствором формальдегида: 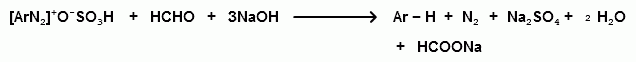 - восстановление алифатическими спиртами: Восстановление диазониевых соединений иногда достигается с помощью алифатических спиртов, однако эта реакция часто сопровождается образованием алкоксипроизводных: 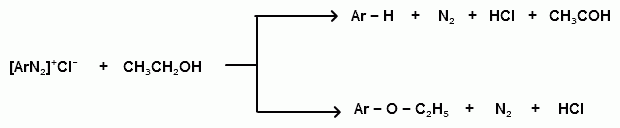 Эта реакция имеет большое практическое значение для синтеза различных веществ. Восстановление дает возможность использовать аминогруппу для активирования ядра или для требуемой ориентации; затем она может быть удалена диазотированием и восстановлением: 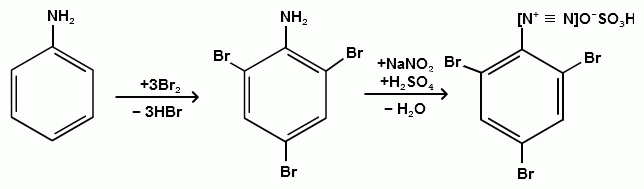 анилин 2,4,6-триброманилин 2,4,6-трибромфенилдиазоний гидросульфат 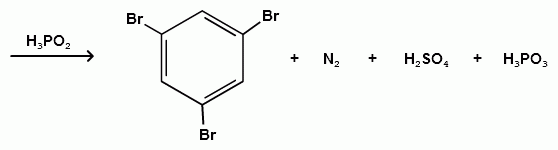 1,3,5-трибромбензол 2. Реакции диазосоединений без выделения азота 1) Восстановление солей диазония При восстановлении солей диазония образуется солянокислый фенил-гидразин: 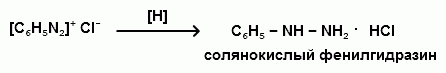 В качестве восстановителей применяют SnCl2 в HCl или смесь сульфита и гидросульфата натрия: 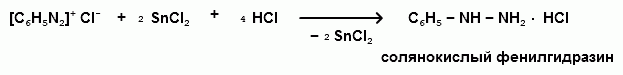 Эта реакция имеет большое значение. Так как фенилгидразин используется для идентификации альдегидов и кетонов, выделения и идентификации сахаров. Фенилгидразин также используется как исходный продукт при производстве азокрасителей и лекарственных веществ (например, амидопирина и антипирина). Фенилгидразин является сильным ядом, разрушающим эритроциты и лейкоциты крови, превращающим гемоглобин в метгемоглобин. 2. Окисление диазосоединений При окислении диазотатов пероксидом водорода получаются нитроамины и нитрозогидроксиламины: 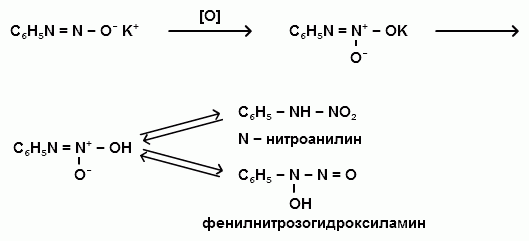 3. Реакции азосочетания Реакции азосочетания имеют большое практическое значение, так как позволяют получать азокрасители. Азосочетанием называют взаимодействие диазосоединений с фенолами и ароматическими аминами, сопровождающееся образованием веществ, содержащих азогруппу –N=N-, связанную с двумя ароматическими радикалами. 1) Взаимодействие солей диазония с фенолами Сочетание с фенолами ведут в слабощелочной среде, так как фенолят-ион значительно активнее, чем сам фенол: 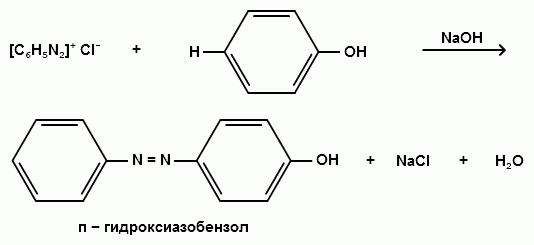 2) Взаимодействие солей диазония с ароматическими аминами Сочетание с ароматическими аминами ведут в слабокислой среде, так как в сильнокислом растворе аминогруппа превращается в аммонийную, которая дезактивирует ароматическое ядро: 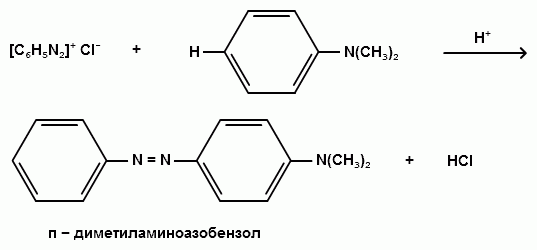 Механизм реакции азосочетания Азосочетание относится к реакциям электрофильного замещения, в которых диазокатион является сильным электрофильным реагентом. Сочетание всегда происходит в пара-положение, а если оно занято, то в орто-положение. Диазосоединение, участвующее в реакции азосочетания называется диазосоставляющей, а ароматические амины или фенолы, вводимые в реакцию азосочетания – азосоставляющей: 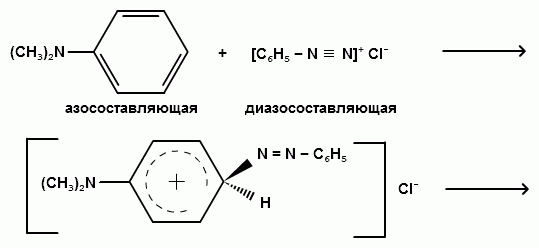 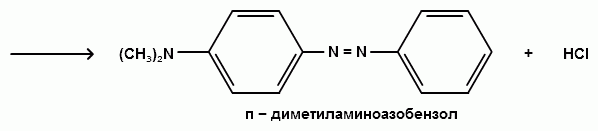 Наиболее важными диазосоставляющими являются анилин, метаниловая кислота, сульфаниловая кислота, антраниловая кислота, пара- и мета-нитроанилины, 1-нафтиламин-5-сульфокислота, бензидин и его производные. В качестве азосоставляющих применяются фенол, β-нафтол, мета-фенилендиамин, α-нафтиламин, нафтиламинсульфокислоты, нафтолсульфо-кислоты и аминонафтолсульфокислоты. Варьируя диазо- и азосоставляющие, оказалось возможным получить тысячи азосоединений, которые являются ценными красящими веществами (азокрасители). Классический синтез азосоединения – получение метилового оранжевого (красителя и индикатора). 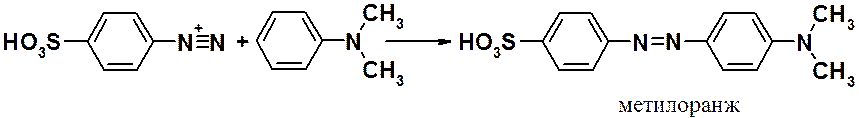 сульфаниловая кислота метиловый оранжевый 4. Взаимодействие с аминами В случае первичных и вторичных ароматических аминов в нейтральной или слабощелочной среде азогруппа вступает не в ароматическое ядро, а в аминогруппу с образованием диазоаминосоединений:  диазоаминосоединения 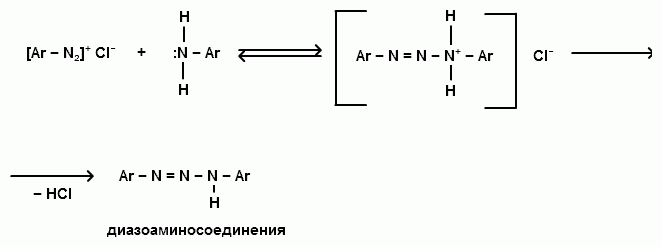 Под влиянием кислот при нагревании диазоаминосоединия превращаются в аминоазосоединения: 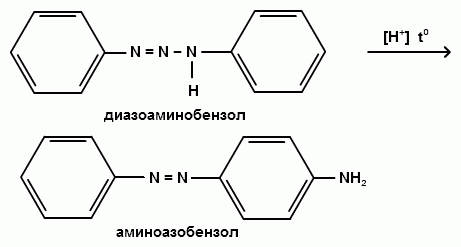 Понятие об азокрасителях Азосоединения окрашены, поскольку содержат хромофорную группу (азогруппа), которая способствует поглощению света в видимой области спектра, а также ауксохромные группы (ОН, NH2 и т.д.), которые углубляют цвет и способствуют связыванию красителя с волокном. Такие азосоединения относят к красителям. Примерно половина используемых в промышленности красителей относится к азокрасителям. Они могут быть моно-, ди-, полиазокрасителями в зависимости от количества азогрупп, иметь окраску от красного до зеленого цвета (зеленый, желтый, оранжевый, красный).  Некоторые азокрасители способны изменять цвет при определенном значении рН, и их используют в аналитической химии в качестве кислотно – основных индикаторов. У используемых в качестве индикаторов азокрасителей в азосоставдяющей имеются обладающие основными свойствами аминогруппы. Важнейшими кислотно-основными индикаторами являются красители метиловый оранжевый, метиловый красный, конго красный и др. Метиловый оранжевый: 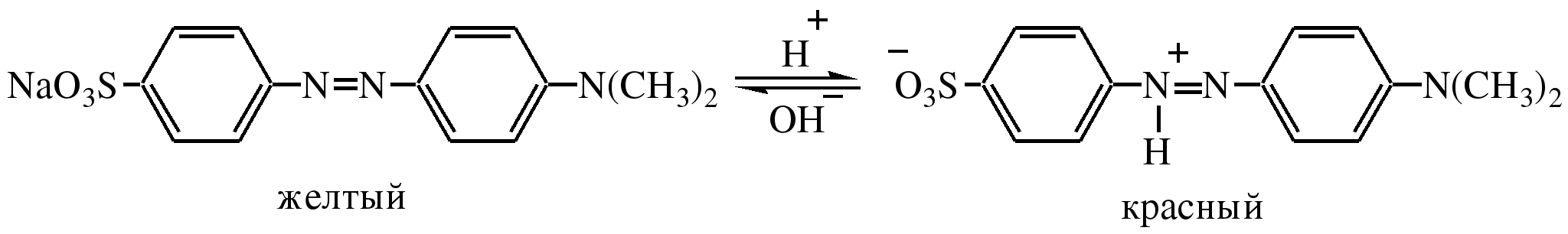 Конго красный: 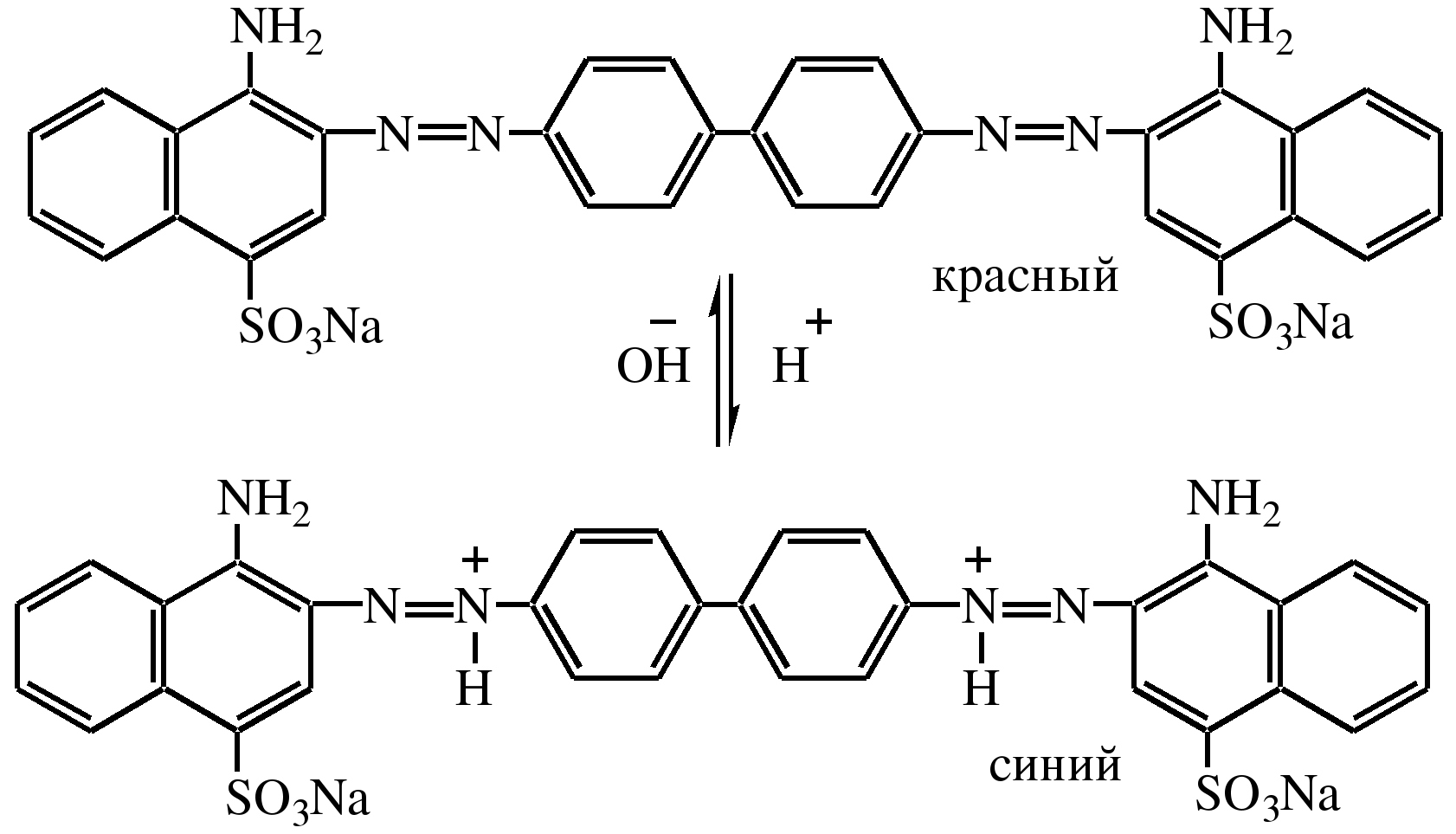 Методы крашения тканей: А. Красители, содержащие полярные группы Б. Дисперсные красители В. Красители, образующие химические соединения с волокном Г. Проявляющие красители (ледяное крашение) Д. Протравные красители Е. Кубовые красители Ж. Пигменты Относительная устойчивость ароматических солей диазония объясняется устойчивостью катиона, которая достигается не только за счет эффективной делокализации заряда между двумя атомами азота, но и за счет трех атомов углерода бензольного кольца: 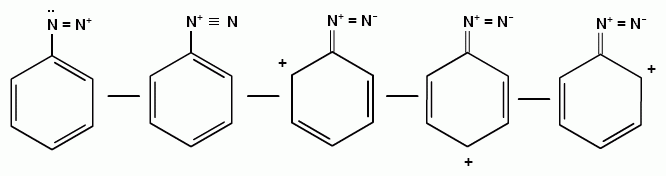 (1) (2) (3) (4) (5) Однако предельные (граничные) структуры 3,4,5 вносят наименьший вклад в реальное строение катиона, поэтому наиболее часто учитывают только первые две структуры. Наибольший положительный заряд сосредоточен на центральном атоме азота (δ+ > δ'+): 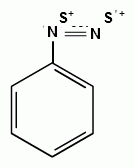 мезоформула катиона диазония Атомы азота в катионе находятся в состоянии sp-гибридизации, связь между атомами азота близка к тройной связи: 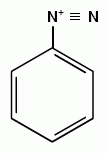 |
