Биотехнология получения аспартама, L-фенилаланина, L-аспарагиновой кислоты. Аспартам. Биотехнология получения аспартама, lфенилаланина, lаспарагиновой кислоты
 Скачать 1.45 Mb. Скачать 1.45 Mb.
|
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «» МЕДИЦИНСКИЙ ИНСТИТУТ ФАРМАЦЕВТИЧЕСКИЙ ФАКУЛЬТЕТ КАФЕДРА ФАРМАЦИИ КУРСОВАЯ РАБОТА ПО БИОТЕХНОЛОГИИ по специальности 33.05.01 Фармация НА ТЕМУ: «Биотехнология получения аспартама, L-фенилаланина, L-аспарагиновой кислоты» Содержание Введение 3 ГЛАВА 1. Общая характеристика аспартама, L-фенилаланина, L-аспарагиновой кислоты 5 1.1Принадлежность к химическому классу. Химическая структура, номенклатура 7 1.2Природные источники и биологическая роль в организме человека 9 ГЛАВА 2. Биотехнологический процесс получения аспартама, L-фенилаланина, L-аспарагиновой кислоты 12 2.1. Биотехнологическое получение L-Аспарагиновой кислоты 14 2.2. Биотехнологическое получение L-Фенилаланина 16 2.3. Биотехнологический процесс синтеза Аспартама 18 ГЛАВА 3. Значение и применение препаратов, анализ фармацевтического рынка 20 Заключение 29 Список литературы 31 ВведениеВ биотехнологии одним из векторов развития является медицина. Активно внедряются и используются новые подходы в биотехнологии. Совершенствование методов дало возможность получать высокопродуктивные штаммы-продуценты, которые используют прежде всего для биосинтеза различных лекарственных соединений. По оценкам BusinesStat, в 2015-2019 г. оборот рынка биотехнологий в России вырос на 30%: с 195 до 254 млрд руб. Основным фактором роста является политика стимулирования инновационных процессов и развития необходимой инфраструктуры с использованием механизмов государственно-частного партнерства. Лидером по объему выручки на рынке биотехнологий в России является сектор биофармацевтики – 42,5% общего оборота в 2019 г На втором месте сектор биотехнологий в сельском хозяйстве – 15,7% Доля продукции биомедицины составила 14%, ветеринарии – 10,8%, промышленности – 3,8%. В 2021-2024 гг оборот рынка биотехнологий будет продолжать увеличиваться на 3,7-6,7% ежегодно и в 2024 г составит 312 млрд руб., что на 23% выше показателя 2019 г[1]. Исходя из прогнозов можно сделать вывод о том, что отрасль является прогрессивной и изучение биотехнологических процессов весьма актуально. Актуальность темы: Перспективным направлением получения интенсивных подсластителей биотехнологическими методами является направленный синтез сладких аминокислот и дипептидов, в том числе Аспартама, а также аминокислот - фенилаланина и аспарагиновой кислоты. Целью курсовой работы является рассмотреть биотехнологию получения аспартама, L-фенилаланина, L-аспарагиновой кислоты. Для осуществления поставленной темы были поставлены следующие задачи: изучить теоретический материал по данной теме; дать общую характеристику аспартама, L-фенилаланина, L-аспарагиновой кислоты, а именно: принадлежность к химическому классу, биохимическая роль в организме и природные источники; рассмотреть биотехнологию получения аспартама, L-фенилаланина, L-аспарагиновой кислоты; представить значение и применение в фармацевтической деятельности и провести анализ рынка. ГЛАВА 1. Общая характеристика аспартама, L-фенилаланина, L-аспарагиновой кислотыВ пищевой промышленности, кулинарии, в качестве пищевых добавок для диетического питания, а также в фармацевтической отросли, с давних времен широко применяются вещества, обладающие сладким вкусом, - подсластители или сахарозаменители. История сахарозаменителей началась в 1879 году. В лаборатории американского профессора Ремсена работал никому не известный химик Фальберг, эмигрант из России. Однажды за обедом он обратил внимание на необычный вкус хлеба — он был сладким. Но домашние никакой сладости не ощущали. Тогда Фальберг понял: сладок не хлеб, а его пальцы — до обеда ученый возился с препаратом со страшным названием сульфаминбензойная кислота. После трапезы изобретатель помчался в лабораторию проверить догадку. Предположение подтвердилось: соединения сульфаминбензойной кислоты действительно были изумительно сладкими. Так был синтезирован сахарин. Химическое вещество с такими свойствами пригодилось очень быстро: во время Первой мировой войны сахара катастрофически не хватало. Сейчас, спустя многие годы после случайного открытия Фальберга, спрос на подсластители велик как никогда. Ведь многие сахарозаменители не имеют энергетической ценности[10]. Преимущества подобных подсластителей перед сахарозой при использовании их в различных пищевых продуктах: удешевление и упрощение технологии производства; сокращение погрузочно-разгрузочных и транспортно-складских операций; снижение калорийности готового продукта в десятки раз; усиление и обогащение сладости и вкуса продукта при сочетании с фруктовыми ароматизаторами и органическими кислотами; возможность расширения ассортимента выпускаемой продукции; улучшение биологической стойкости при хранении. В данную группу пищевых добавок входят вещества несахарной природы, которые придают пищевым продуктам сладкий вкус. Имеется множество классификаций сладких веществ, некоторые из них представлены в таблице 1[2]. Таблица 1 Классификации подсластителей по некоторым признакам.
По сладости различают несколько подсластителей, имеющие разное химическое строение и различную относительную сладость (Таб.2)[10]. Таблица 2 Подсластители с различной относительной сладостью.
Продолжение таблицы 2 Подсластители с различной относительной сладостью.
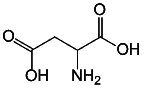
Помимо этого все заменители сахара можно условно разделить на две группы: натуральные и синтетические. К группе натуральных подсластителей относится: фруктоза, сорбит, ксилит. Они полностью усваиваются организмом и, как обычный сахар, обеспечивают человека энергией. Синтетические заменители наоборот не имеют энергетической ценности. В эту группу входит сахарин, цикламат, ацесульфам калия, сукразит и аспартам. [2]. Случайное открытие сладкого вкуса у метилового эфира (1)-аспартил-(1)-фенилаланина Джеймсом Шлаттером в 1965 г. произошло, когда он попробовал продукт, намочив палец, чтобы поймать лист бумаги, во время синтеза тетрапептида тестируемой в качестве лекарственного средства «Анти -Язва». Далее начали появляться множество работ, посвященных синтезу и применению «аспартама» - так был назван этот препарат, синтез которого впервые был опубликован в 1966 г. В промышленном масштабе аспартам был выпущен американской фирмой GD Searle & Company. В настоящее время это торговая марка и дочерняя компания Pfizer, работает в более чем 43 странах. Также бренд используется в качестве дистрибьюторского товарного знака для различных фармацевтических препаратов, которые были разработаны G. D. Searle & Company, часто называемой Searle. После чего дипептид начал активно продаваться в качестве подсластителя [3]. Принадлежность к химическому классу. Химическая структура, номенклатураАспартам представляет собой дипептид, производный от двух аминокислот, L-аспарагиновой кислоты и L-фенилаланина (Рис.1).
Рис.1 Структурные формулы L-аспарагиновой кислоты и L- фенилаланина Поэтому его химическое название - метил L-аспартил-L-фенилаланат (Рис.2)[10].  Рис.2 Структурная формула метил L-аспартил-L-фенилаланата (Аспартама). Фенилаланин – 2-амино-З-фенилпропионовая или α-амино-β-пропионовая кислота (сокращенно: Фен), имеющая химическую формулу C9H11NO2 (С6Н5СН2СН(NH2)COOH) и молекулярную массу 165,19 а.е.м.. Фенилаланин существует в виде двух оптически изомерных формах L (натуральная) и D (синтетическая) и рацемата (DL) [1-6]. DL-фенилаланин – эта форма незаменимой аминокислоты фенилаланина является смесью равных частей L- и D- фенилаланина, Т.пл. 271-273 °C, умеренно растворим в спирте[14]. Фенилаланин – ароматическая α–аминокислота, дает ксантопротеиновую реакцию, может быть осажден 2,5-дибромбензолсульфокислотой. При нагревании фенилаланин декарбоксилируется с образованием β-фенилэтиламина; при нитровании фенилаланина получают 4-нитрофенилаланин. Особенности физических и химических свойств аминокислоты обусловлены его строением – присутствием одновременно двух противоположных по свойствам функциональных групп: кислотной – СООН и основной – NH2. Аспарагиновая кислота относят к дикарбоновым аминокислотам, соединениям, имеющим два кислотных хвоста СООН. Она имеет 2 оптических изомера, которые условно называются L-аспартат и D-аспартат. Природная протеиногенная аминокислота относится к L – изомерам, D- изомер встречается в организме человека в свободном виде, но выполняет свои специфические функции и в состав белка не входит. L – изомер аспарагиновой кислоты благодаря наличию двух кислотных хвостов имеет гидрофильные свойства и хорошо растворяется в воде. Имеет химическую формулу HO2CCH(NH2)CH2CO2H и молекулярную массу 133,1 г/моль[4]. Природные источники и биологическая роль в организме человекаФенилаланин широко распространен в природе. Аминокислота встречается во всех организмах в составе молекул белков, в частности инсулина, яичного белка, гемоглобина, а также в овальбумине, зеине, фибрине. Натуральными источниками фенилаланина являются свинина, баранина и говядина, куриное мясо и яйца, икра, рыба и морепродукты, орехи, миндаль, арахис, семена подсолнечника соя и другие бобовые, твердые сыры, брынза, творог, молоко и молочные продукты, в которых он содержится в больших количествах. Усвоение фенилаланина повышают витамин C, B6, железо, медь и ниацин. Фенилаланин – кодируемая, незаменимая аминокислота для человека и животных. Суточная потребность данной аминокислоты составляет (в мг/кг) у взрослых мужчин 4,3, у женщин 3,1, у детей 90. Фенилаланин непрерывно образуется в организме при распаде белков пищи и тканевых белков. Потребность в фенилаланине возрастает при отсутствии в пище аминокислоты тирозина, который образуется в печени гидроксилированием фенилаланина с участием фермента фенилаланингидроксилазы [7]. Биохимическая роль фенилаланина для человека очень важна. Фенилаланин принимает участие в биохимических процессах формирования протеинов и кодируется определенным геном ДНК. Фенилаланин является исходным сырьем синтеза другой аминокислоты – тирозина, который, в свою очередь, является предшественником адреналина, норадреналина и дофамина, а также пигмент кожи меланина. L-фенилаланин является строительным материалом в цепочке реакций, в результате которых образуются нейромедиаторы – катехоламины (в том числе норадреналин и дофамин). Он обеспечивает достаточным количеством субстрата биохимические процессы мозга, протекающие в случае повышенной нагрузки. В отличие от искусственных стимуляторов таких как, кофе и алкоголь, которые истощают запас энергии и приводят человека в состояние раздражения, аминокислота позволяет успешно справляться с раздражением и чувством тревоги. L-Фенилаланин помогает человеку снять напряжение без применения алкоголя, сохраняя в мозгу пептиды эндогенной опиатной (внутренней) системы, тем самым делая человека менее зависимым от приема алкоголя и препаратов [12]. L-Аспарагиновая кислота - алифатическая аминокислота, одна из 20 протеиногенных аминокислот организма. Встречается во всех организмах в свободном виде и в составе белков. Кроме того, исполняет роль нейромедиатора в центральной нервной системе, участвуя в обмене азотистых веществ. А также принимает участие в образовании пиримидиновых оснований и мочевины. Аспарагиновая кислота является критически важными для роста и размножения лейкозных клеток при некоторых видах лимфолейкоза. Фермент микробного происхождения L-аспарагиназа, нарушающий превращение аспарагиновой кислоты в аспарагин и наоборот, оказывает сильное специфическое цитостатическое действие при этих видах лейкозов. Аспарагиновая кислота в больших количествах содержится в таких продуктах питания, как куриная грудка, соевые бобы, желток куриного яйца, арахис, говядина, базилик, фасоль красная, горох, форель и многие другие. Так как Аспартам является синтетически синтезированным веществом, в природе не встречается. Аспартам в организме человека распадается на две вышеперечисленные аминокислоты, а также метанол. Большое количество токсикологических и клинических исследований аспартама подтверждают его безвредность, если дневная доза не превышает 50 мг на килограмм массы тела. В Европе установлен максимум: 40 мг на килограмм массы в день. Потребление продуктов, содержащих аминокислоту фенилаланин, противопоказано людям с наследственным заболеванием фенилкетонурия, поэтому во многих странах, включая Россию, продукты, содержащие аспартам, должны иметь предупреждение «Содержит источник фенилаланина»[4,12]. ГЛАВА 2. Биотехнологический процесс получения аспартама, L-фенилаланина, L-аспарагиновой кислотыБиотехнологическое получение аминокислот является широко распространенным на сегодняшний день и основано на способности микроорганизмов к синтезу всех L-аминокислот. Кроме этого, селекционная работа со штаммами-продуцентами аминокислот позволяет обеспечивать их сверхсинтез. Пути синтеза большинства аминокислот взаимосвязаны и при этом одни аминокислоты являются предшественниками других [7] (Рис.3).  Рис.3 Схема биосинтеза аминокислот. Наиболее перспективен и экономически выгоден микробиологический синтез аминокислот. Более 60% всех производимых в настоящее время высокоочищенных препаратов аминокислот получают именно этим способом, главное преимущество которого в сравнении с методами химического синтеза состоит в возможности получения L-аминокислот из возобновляемого сырья (Рис.4)[8].  Рис.4 Общая схема получения аминокислот микробиологическим методом. Процесс получения аминокислот ферментационным методом основан на способности некоторых микроорганизмов синтезировать L-аминокислоты, а в определенных условиях – обеспечивать их сверхсинтез. Основное отличие микробиологической ферментации от химико-ферментативного метода заключается в отсутствии стадии химического синтеза предшественника, а также в использовании живых клеток микроорганизмов. Продуцентами аминокислот в биосинтезе являются бактерии родов Corynebacterium, Brevibacterium, Escherishia, Micrococcus. Субстратом может служить – углеводное сырье: меласса, гидролизаты крахмала и целлюлозы, а также этанол, уксусная или другие органические кислоты, помимо этого могут использоваться углеводороды. В качестве источника азота используют соли аммония, нитраты, а также аминокислоты. На основе культивирования микроорганизмов для получения чистых препаратов аминокислот применяют промышленные технологии, включающие одно- и двухступенчатый синтез аминокислот. При одноступенчатом синтезе в промышленных культиваторах выращивают ауксотрофные регуляторные мутанты, являющиеся сверхпродуцентами аминокислот. После завершения рабочего цикла их выращивания культуральную жидкость отделяют от клеток микроорганизмов, сгущают и получают товарный продукт с высокой концентрацией целевой аминокислоты. В процессе двухступенчатого синтеза вначале с помощью одного штамма микроорганизмов получают предшественник, а затем с помощью другого штамма превращают предшественник в целевую L-аминокислоту. Исходными веществами для синтеза аспартама являются L-аспарагиновая кислота и L-фенилаланин. После их получения необходима стадия химического синтеза аспартама, что требует дополнительных затрат на введение защитных групп в молекулы исходных веществ. На сегодняшний день, данный метод получения подсластителя является экономически нерентабельным, поэтому в настоящее время чаще применяют ферментативные методы получения этого продукта. Объем производства аспартама по данным 2020г составляет 20 000 т/г и эта цифра постоянно растет, в связи с увеличением потребления продуктов и лекарственных средств, содержащих в своем составе добавку – аспартам [15]. 2.1. Биотехнологическое получение L-Аспарагиновой кислотыОдним из методов получения L-аспарагиновой кислоты является экстракция из белкового гидролизата, однако экономически более выгодным оказался синтез клетками Escherichia coli из фумаровой кислоты в присутствии аммиака. Реакцию осуществляет фермент аспартаза, находящийся в клетках микроорганизма (Рис.5) [15].  Рис.5 Схема получения L-аспарагиновой кислоты. Как правило, для выращивания клеток используют биореактор, в котором бактерии иммобилизованы на каррагинане или полиакриламиде. Способ получения стационарных культур с высокой аспартазной активностью и урожаем клеток осуществляется культивированием клеток Escherichia coli на среде следующего состава, г/л: Na2HPO4•12H2O - 1.5 KH2PO4 - 0.75 NaCl - 0.5 CaCl2 - 0.01 Фумарат натрия - 3 Ацетат аммония - 5 Кукурузный экстракт - 5 В этих условиях штамм Е.coli 858 обладает высокой аспартазной активностью, которая достигает максимума на стационарной фазе роста около 20-21 часа. Активирование микробных клеток перед получением L-аспарагиновой кислоты проводят инкубированием суспензии клеток в 1М растворе фумарата аммония при 37°C в течение 16-18 ч. Целью активирования является увеличение проницаемости клеточной мембраны для ионов фумарата и аспартата[8]. Условия культивирования: температура 29°C, аэрация 2 л/мин, перемешивание 500 об/мин, pH 7.9. Система автоматического поддержания pH осуществляет дозировку питательного раствора уксусной кислоты. Время культивирования 22-26 ч. Выход продукта в такой системе достигает 140 г/л×ч, а срок службы биокатализатора на основе иммобилизованных клеток составляет два года. Использование сублимированных клеток промышленных штаммов позволяет получать до 166 г L-аспарагиновой кислоты с литра клеточной культуры. В лабораторных условиях удалось получить штамм E. coli с плазмидой, несущей ген аспартазы (aspA). В таком штамме выход L-аспарагиновой кислоты увеличивается в 30 раз[7]. 2.2. Биотехнологическое получение L-ФенилаланинаТрадиционно производство L-фенилаланина осуществлялось в ферментативных реакторах на доступном сырье. В последнее время в связи с развитием молекулярно-биологических методов, позволяющих получать генетически модифицированные штаммы-суперпродуценты, все шире используют ферментацию. Распространение ферментативных методов объясняется доступностью и невысокой стоимостью синтетического сырья, а также выгодным соотношением между производственными площадями, временными затратами и выходом продукта. Для производства L-фенилаланина наиболее выгодным оказалось использование биореактора, в котором в присутствии аммиака происходит аминирование коричной кислоты под действием фермента фенилаланинаммиаклиазы из Rhodotorula glutinis. В таком реакторе выход продукта достигает 50 г/л, а эффективность переработки сырья составляет 83%. Перспективным также считается метод расщепления D,L-5-бензилгидантоина ферментами L-гидантоиназой и L-N-карбамоилазой, выделенными из Flavobacterium ammoniagenes. Для ферментации в биореакторах в современном производстве, как правило, используют штаммы-суперпродуценты E. coli или коринебактерий. В этих организмах биосинтез L-фенилаланина из эритрозо-4-фосфата и фосфоенолпирувата протекает в несколько стадий. В качестве промежуточных соединений образуются шикимовая, префеновая и фенилпировиноградная кислоты, в диком штамме они предшественники L-триптофана и L-тирозина. Однако в промышленности используют мутантные ауксотрофные штаммы, в которых активность ключевых ферментов строго регулируется. Практически все гены, продукты которых участвуют в биосинтезе L-фенилаланина, к настоящему времени клонированы. Это позволяет получать новые штаммы-суперпродуценты, применяя генноинженерные методы. Так, выход L-фенилаланина в одном из рекомбинантных штаммов Brevibacterium fermentum составляет 45 г на литр клеточной культуры (Рис.6)[15].  Рис.6 Методы получения L-фенилаланина. Один из способов получения стационарных культур с высокой продуктивностью осуществляется культивированием клеток рода Methylophilus на среде следующего состава, (1 л): К2НРO4•3Н2О - 1,57 г К2НРO4 - 0,62 г (NH4)2SO4 - 3 г NaCl - 0,1 г MgSO4•7H2O - 0,2 г CaCl2 - 0,025 г ЭДТА-Nа2 - 5 мг FeSO4•7H2O - 3 мг MnSO4•5H2O - 0,01 мг ZnSO4•7H2O - 0,07 мг Na2MoO4•2H2O - 0,01 мг Н3ВО3 - 0,01 мг CoCl2•6H2O - 0,005 мг CuSO4•5H2O - 0,005 мг Метанол - 20 мл (стерилизованный фильтрованием) СаСО3 - 30 г Условия культивирования: температура 37°C, перемешивание 250 об/мин, pH 7. После завершения ферментации по воздушно-проточному способу клетки отделяют, а затем концентрируют культуральную жидкость ульрафильтрацией. Для окончательной очистки L-фенилаланина применяют ионообменную хроматографию или кристаллизацию[8]. 2.3. Биотехнологический процесс синтеза АспартамаДля синтеза аспартама из L-аспарагиновой кислоты и L-фенилаланина необходимо сначала ввести в исходные молекулы пять защитных групп, а в конце синтеза их удалить. Такой метод значительно сложнее синтеза с использованием протеиназы. В обычных условиях протеолитические ферменты катализируют гидролиз пептидных связей, однако возможно сдвинуть равновесие в сторону образования пептидной связи. Так, в концентрированных растворах, содержащих L-аспарагиновую кислоту (в которой аминогруппа защищена бензилоксикарбонилом) и метиловый эфир L-фенилаланина, протеиназа катализирует образование малорастворимого пептида, который выпадает в осадок. Особенно важно, что в этой реакции принимает участие только карбоксильная группа L-аспарагиновой кислоты, так как изомер аспартама – метиловый эфир L-аспартил-L-фенилаланина – обладает сильно выраженным горьким вкусом. В промышленном производстве, как правило, используют иммобилизованную протеиназу термолизин, выделенную из Bacillus thermoproteolyticus. Этот фермент устойчив к высоким температурам и может осуществлять реакцию при 60°С, что значительно повышает эффективность процесса, выход продукта достигает 30 г/л. Образовавшееся вещество - аспартам в значительной степени отделен от побочных продуктов, так что для окончательной очистки от примеси исходных веществ достаточно ионообменной хроматографии (Рис.7).  Рис.7 Биотехнологическая схема получения аспартама. Способ сушки и гранулирования аспартама заключается в том, что влажную массу кристаллов аспартама термически обрабатывают за счет горячего газа-носителя. Влажные кристаллы аспартама выделяют из суспензии, а из этой влажной массы кристаллов впоследствии получают гранулы диаметром 0,1-10 мм[15]. ГЛАВА 3. Значение и применение препаратов, анализ фармацевтического рынкаМировое производство Фенилаланина микробиологическим синтезом составляет свыше 25 000 т в год. Ежегодно данные показатели растут, это возможно связанно с тем, что фенилаланин используется в синтезе Аспартама, который в свою очередь занимает лидирующие позиции в России среди других заменителей сахара. Объемы потребления продуктов питания и использования лекарственных препаратов, содержащих аспартам, следовательно, тоже растут. Объем производства Аспартама по данным 2020г составляет 20 000 т/г. Что составляет около 23 % мирового объема производства искусственных подсластителей. Эти данные позволяют сделать вывод о том, что препараты, в которых сахар заменяют на подсластитель, являются актуальными, и такая необходимость возникает не только для коррекции вкуса, но и вследствие высокой заболеваемости диабетом среди населения. В России предположительная распространенность сахарного диабета составляет 5,7%, а численность больных - 9 миллионов человек. По прогнозам, к 2025 году количество больных сахарным диабетом увеличится вдвое, а к 2030 году, по расчетам Международной Федерации диабета, этот диагноз может быть поставлен 500 миллионам человек. Потребность в синтетических вкусовых агентах для замены сахарозы неуклонно возрастает. Многие представители ряда эфиров дипептидов превосходят сахарозу по интенсивности вкуса в сотни и тысячи раз. Их применение позволило резко снизить калорийную нагрузку в связи с малым количеством потребления. Процесс усвоения таких продуктов не связан с инсулином. Благодаря этим свойствам сладкие пептиды, наряду с другими низкокалорийными природными и синтетическими сладкими веществами, могут использоваться в диетическом низкокалорийном питании и рекомендоваться, прежде всего, больным, страдающим ожирением и сахарным диабетом[3]. Аспартам содержится в таких продуктах питания как, безалкогольные напитки, йогурты, молочные десерты, мороженное, кондитерские изделия, горячий шоколад, малоалкогольное пиво, жевательные резинки. Согласно с гигиеническими нормативами применения подсластителей, содержащихся в приложении к действующему техническому регламенту "Требования безопасности пищевых добавок, ароматизаторов и технологических вспомогательных средств" (ТР ТС 029/2012), допустимое содержание Аспартама в пищевых продуктах(Таб.3)[13]: Таблица 3 Гигиенические нормативы применения аспартама.
Помимо этого, сладкие дипептиды широко используют для коррекции вкуса. Они особенно удобны для применения в фармацевтических целях, так как менее подвержены микробной контаминации и порче. Например, Аспартам широко используется для подслащивания детских лекарственных форм, так как он безопасен для детей так же, как и для взрослых. С медицинской точки зрения у аспартама есть еще одно немаловажное преимущество по сравнению с сахарозой: он не стимулирует развитие зубного кариеса. При комбинированном использовании аспартама с сахарозой, глюкозой, цикламатом или сахарином проявляется синергизм, благодаря чему снижаются расходные коэффициенты обоих компонентов смеси. Среди наиболее широко употребляемых в настоящее время за рубежом, в частности, в США сладких синтетических агентов аспартам выгодно отличается своими вкусовыми свойствами. Хорошо изучены его метаболизм и потенциальная токсичность. Этот препарат выдержал многочисленные испытания на токсичность и канцерогенность, и противопоказан только страдающим заболеванием фенилкетонурией [2]. Крупнейшим производителем аспартама является американская компания "Нутрасвит-Келко". На российском рынке его можно встретить под марками Miwon (Южная Корея), Enzimologa (Мексика), Ajinomoto (Япония) и другие. В композиции с сахарозой, цикламатом и сахарином производится в России под маркой "Аспамикс" со степенью сладости в 100, 200 и 350 раз. Для экономического анализа рынка были рассмотрены препараты, являющиеся заменителями сахара. В таблице представлены основные характеристики, а именно наименование, производитель, состав, описание и цена(Таб.3)[11]: Таблица 4 Сравнительная характеристика сахарозаменителей.
Продолжение таблицы 4 Сравнительная характеристика сахарозаменителей.
В таблицы представлены 4 вида сахарозаменителей отечественных и зарубежных марок. По составу они также различаются, одни наименования содержат в своем составе натуральные вещества, другие синтетические. Цены вирируются от 117 до 226 руб., что входит в одну ценовую категорию, но более выгодным предложением, в зависимости от количества таблеток в одной упаковке, является заменитель сахара Новасвит Аспартам подсластитель столовый в таблетках. Необходимо более подробно разобрать его характеристики. В соответствии с заявленной инструкцией, заменитель сахара Новасвит подходит для подслащивания горячих и холодных напитков. Не повышает уровень сахара в крови человека, то есть гликемический индекс равен нулю. Одна таблетка может заменить кусочек сахара-рафинада или одну ложку сахарного песка. Добавка рекомендована для диетического и диабетического питания, которую можно применять 2-3 раза в день, добавляя в чай, кофе и другие напитки. Безопасная доза суточного потребления - не более 1 таблетки на 5кг веса тела. К побочным эффектам относится: редко – крапивница и другие аллергические реакции. В единичных случаях: парадоксальное усиление аппетита, мигрень. Противопоказания к применению, в согласно инструкции - гомозиготная фенилкетонурия, повышенная чувствительность к аспартаму. Хранить в сухом месте. Срок годности 24 месяца. Условия отпуска из аптек - без рецепта. В качестве вспомогательных субстанций, используемых для коррекции вкуса, аспартам входит в состав таких лекарственных форм, как[6]: Порошок для приготовления раствора для приема внутрь (АнвиМакс®, Дуоколд®, Мовипреп®) Таблетки, диспергируемые в полости рта (Блогир-3®, Торендо® Ку-таб) Таблетки шипучие (Максотропил®) Таблетки жевательные (Сингуляр®, Антарейт®, Пассажикс®) Таблетки, покрытые пленочной оболочкой (МОНЛЕР®) Гранулы для приготовления суспензии для приема внутрь (Строметта) Таблетки для рассасывания (Тантум® Верде) Сироп (Пантогам ®) Лекарственные препараты, в изготовлении которых используют вспомогательную субстанцию аспартам, имеют разнообразное фармакологическое действие. Данные препараты относятся к фармакологическим группам: Нестероидные противовоспалительные средства, ноотропы, слабительные средства, нейролептики, противорвотные средства, корректоры метаболизма костной и хрящевой ткани, H1-антигистаминные средства, простагландины, тромбоксаны, лейкотриены, их аналоги, антацидные средства и многие другие[9]. Это стало возможным так как, добавка E951 признана безопасной и отвечает всем требованиям, предъявляемым как фармацевтическим субстанциям, главное из которых – индифферентность по отношению к действующему веществу[5]. Фармацевтическая субстанция вспомогательного вещества прежде, чем использоваться в изготовлении лекарственных препаратов, должна быть зарегистрирована, и в соответствии с нормативным документом пройти стандартизацию. Аспартам FCC – вспомогательная субстанция, которая упакована в волокнистые барабаны, расфасованные по 25кг (Рис.8)  Рис.8 Внешний вид и упаковка фармацевтической субстанции аспартама. Ее необходимо хранить в прохладном, сухом, вентилируемом помещении вдали от источников тепла, влаги и несовместимости. Избегая образования пыли и контролируя источники воспламенения. Как и многие другие пептиды, Аспартам может гидролизоваться на его составляющие аминокислоты в условиях повышенной температуры, влажности или высокого значения рН. Поэтому ингредиенты, используемые для производства субстанции Аспартама, регулярно проверяются для обеспечения качества и безопасности, включая микробиологическую чистоту. Кроме того, проверяются физические и химические свойства готового продукта, такие как уровень pH, температура плавления и содержание влаги, чтобы обеспечить соответствие стандартам. Стандартизацию проводят по следующим признакам (Таб.4): Таблица 5 Показатели качества фармацевтической субстанции аспартам.
Из всего вышеперечисленного следует, что Аспартам является относительно экономически выгодной пищевой добавкой, которая официально разрешена к использованию в Российской федерации и ряда других стран, но ее содержание в продуктах питания и БАД к пище регламентируется техническим регламентом. Также Аспартам используют как вспомогательную субстанцию на фармацевтическом рынке, для коррекции вкуса. Множество производителей лекарственных препаратов, под различными торговыми марками, выбирают из большого количества именно данную субстанцию, так как она обладает рядом положительных характеристик. ЗаключениеВ ходе курсовой работы была раскрыта тема биотехнологического получения L-аминокислот – аспарагиновой кислоты и фенилаланина, а также их производного дипептида – аспартама, используемого в качестве искусственного подсластителя. Для этой цели были изучена и представлена общая характеристика выбранных веществ, а именно принадлежность к химическому классу, роль в организме человека, свойства и особенности. Таким образом, аминокислоты, из которых состоит аспартам, относятся к незаменимым аминокислотам для человека. Они участвуют в таких важнейших биохимических процессах, как образование пиримидиновых оснований, каскад реакций образования нейромедиаторов – катехоламинов. Рассмотрев методы получения аминокислот, можно сделать вывод о том, что наиболее перспективен и экономически выгоден микробиологический синтез. Что касается получения L-аспарагиновой кислоты более распространенным и эффективным оказался синтез клетками Escherichia coli из фумаровой кислоты в присутствии аммиака. Выход продукта при таком культивировании составляет 166 г/л Для производства L-фенилаланина наиболее выгодным оказалось использование биореактора, в котором в присутствии аммиака происходит аминирование коричной кислоты под действием фермента фенилаланинаммиаклиазы из Rhodotorula glutinis. В таком реакторе выход продукта достигает 50 г/л, а эффективность переработки сырья составляет 83%. Внедрение биотехнологий в промышленость, специализирующуюся на производстве заменителей сахара, позволило во многом снизить себестоимость получаемого сырья, и как следствие увеличить объемы потребления. В промышленном производстве для получения аспартама используют иммобилизованный термолизин из Bacillus thermoproteolyticus. При использовании метода ферментации выход продукта достигает 30 г/л. Помимо этого, был проведен анализ рынка, исходя из полученных данных, можно сделать вывод, о том, что на сегодняшний день множество лекарственных препаратов в своем составе имею вспомогательное вещество – аспартам. Также он используется в качестве разрешенной добавки E951, которая необходима для диетического питания, в частности для больных сахарным диабетом. Поэтому существует множество разработок и методов, которые направлены на более выгодное получение вышеперечисленных веществ. Это необходимо для рентабельного и конкурентно способного производства. Список литературыАнализ рынка биотехнологий в России в 2015-2019 гг, прогноз на 2020-2024 гг https://businesstat.ru/ Азрилевич М. Р. Заменители сахара // Кондитерское производство. – 2004. – № 1. – С. 42. Баев В. В. Аспартам // Наука и жизнь. – 2006. – № 12. – С. 28-29. Беликов В.Г. Фармацевтическая химия. В 2 частях. Часть 1. Общая фармацевтическая химия: Учеб. для фармац. ин-тов и фак. мед. ин-тов. - М.: Высш. шк., 1993. - 432 с. . ГОСТ Р 53904-2010 Добавки пищевые ПОДСЛАСТИТЕЛИ ПИЩЕВЫХ ПРОДУКТОВ Государственный реестр лекарственных средств. Москва, 2021. Краснопольский Ю.М., Клещев Ю.Ф. Фармацевтическая биотехнология: производство активных веществ: учеб. пособие в 2 ч., Харьков НТУ «ХПИ», 2013. - 192 с Леонтьев, В. Н. «Промышленная технология лекарственных препаратов» /– Минск: БГТУ, 2014. – 94 с. Машковский М.Д. Лекарственные средства. – М.: «Новая волна», 2010.-534с. Павлова Л. Α., Комарова Т. В., Давидович Ю. Α., Рогожин С. В. АСПАРТАМ И ЕГО АНАЛОГИ Успехи химии, 1981, Том 50, Номер 4, Страницы 590-605. Регистр лекарственных средств в России (РЛС). Энциклопедия лекарств. 2012. Сыровая А.О., Шаповал Л.Г., Макаров В.А., Петюнина В.Н., Грабовецкая Е.Р., Андреева С.В., Наконечная С.А., Бачинский Р.О., Лукьянова Л.В., Козуб С.Н., Левашова О.Л. Аминокислоты глазами химиков, фармацевтов, биологов: в 2-х т. Том 2 / − Х. «Щедра садиба плюс», 2015 – 268 с. Технический регламент Таможенного союза "Требования безопасности пищевых, добавок, ароматизаторов и технологических вспомогательных средств", ТР ТС 029/2012 Химическая энциклопедия: в 5 т. – М.: Сов. энцикл.; Большая Рос. энцикл., 1988- 1999. – ISBN 5-85270-008-8. Шмид Р. Наглядная биотехнология и генетическая инженерия перевод с нем.: БИОНОМ Лаборатория знаний., 2014 - 324с. |