|
|
Бж таырыбы Mn Марганец Орындаан Айтжанова. Н тексерген Азимбаева. Г алматы 2022 жоспар
Қазақ ұлттық қыздар педагогикалық университеті КеАҚ
Жаратылыстану институты
Химия кафедрасы

БӨЖ
Тақырыбы:
Mn Марганец
Орындаған:Айтжанова.Н
Тексерген:Азимбаева.Г
Алматы 2022
ЖОСПАР
Кіріспе
Негізгі бөлім
2.1 Марганецтің жалпы сипаттамасы
2.2 Марганецтің табиғатта таралуы
2.3 Марганецтің физика химиялық қасиеттері
2.4Марганец қосылыстары
2.5 Марганец қосылыстарының қолдану аясы
Қорытынды
Пайдаланылған әдебиттер
Кіріспе
Ашылу тарихы

Марганецтің негізгі минералдарының бірі — пиролюзит-ежелгі уақытта қара магнезия ретінде белгілі болған және оны ағарту үшін әйнекті дайындауда қолданылған. Ол магниттік темір тордың бір түрі болып саналды және оны магнит тартпайтынын Плиний ақсақал магнит "бей-жай қарамайтын"қара Магнезияның әйел жынысымен түсіндірді. 1774 жылы швед химигі К.Шееле кен құрамында белгісіз металл бар екенін көрсетті. Ол өзінің досы химик Ю. Ганға кен үлгілерін жіберді, ол пеште көмірмен пиролюзит қыздырып, марганец металын алды. XIX ғасырдың басында ол үшін "манганум" (одан. Manganerz-марганец кені).
Негізгі бөлім
2.1 Марганецтін жалпы сипаттамасы
Марганец дегеніміз не
Марганец (химиялық белгі — mn, лат. Manganum) - Атом нөмірі 25, Д. И. Менделеевтің химиялық элементтерінің периодтық жүйесінің төртінші кезеңінің 17-ші тобының (ескірген классификациясы бойынша — жетінші топтың жанама кіші тобы, VIIB) химиялық элементі.
Қарапайым зат марганец-бұл қатты, бірақ сонымен бірге күміс-ақ түсті сынғыш өтпелі металл. Түсті металдарға жатады.

Жер қыртысының құрамы барлық атомдар санының 0,03% құрайды, ол темірден кейінгі екінші ең көп таралған металл.
Элемент ауыр металдарға жатады-атомдық массасы 40-тан асады. Ауада ол пассивацияланады-ол оттегімен одан әрі реакцияға жол бермейтін тығыз оксид пленкасымен жабылған.
Қыздырылған кезде марганец көптеген қарапайым заттармен, қышқылдармен және негіздермен әрекеттесіп, әртүрлі тотығу дәрежесімен қосылыстар түзеді: -1, -6, +2, +3, +4, +7. Металл өтпелі болып табылады, сондықтан ол тотықсыздану және тотығу қасиеттерін бірдей оңай көрсетеді. Металдармен, мысалы, темірмен, реакциясыз қатты ерітінділер түзеді.
Марганец-өмірлік маңызды микроэлементтердің бірі. Сонымен қатар, бұл өсімдіктер мен жануарларға да қатысты. Элемент фотосинтезге қатысады, тыныс алу процесінде бірқатар ферменттерді белсендіреді, бұлшықет метаболизмінің ажырамас қатысушысы және т.б. Адамдар үшін марганецтің тәуліктік дозасы 2-9 мг құрайды. элементтің жетіспеушілігі де, артық болуы да бірдей қауіпті.
Металл темірге қарағанда ауыр және қиын, бірақ оның жоғары сынғыштығына байланысты оның таза түрінде практикалық қолдану жоқ. Бірақ оның қорытпалары мен қосылыстары халық шаруашылығында өте маңызды. Ол қара және түсті металлургияда, тыңайтқыштар өндірісінде, электротехникада, жұқа органикалық синтезде және т.б. қолданылады.
Марганец өзінің кіші тобындағы металдардан өте ерекшеленеді. Технетий-жасанды түрде алынған радиоактивті элемент. Рений шашыраңқы және сирек элементтерге жатады. Борийді тек жасанды жолмен алуға болады және табиғатта болмайды.
Алынуы:
Пиролюзитті кальцийлеу кезінде түзілетін mn2o3 оксидін тотықсыздандыра отырып, алюминотермиялық әдіспен:
4MnO2 ⟶ 2Mn2O3 + O2
Mn2O3 + 2Al ⟶ 2Mn + Al2O3
Құрамында темір бар марганец оксиді кендерін Кокс арқылы азайту. Осылайша, металлургияда ферромарганец әдетте алынады ( 80% Mn).
Таза металл марганец электролиз арқылы алынады.
2.2 Марганецтін табиғатта таралуы
Марганец-жер бетіндегі таралуы бойынша 14-ші элемент, ал темірден кейін — жер қыртысында кездесетін екінші ауыр металл (жер қыртысының атомдарының жалпы санының 0,03%). Марганецтің массалық үлесі қышқылдан (600 г/т) негізгі жыныстарға (2,2 кг/т) артады. Оның көптеген кендерінде темірмен бірге жүреді, бірақ марганецтің тәуелсіз кен орындары да бар. Чиатурск кен орнында (Кутаиси ауданы) марганец кендерінің 40% - ы шоғырланған. Тау жыныстарында шашыраған Марганец сумен жуылады және Дүниежүзілік мұхитқа тасымалданады. Сонымен қатар, оның теңіз суындағы құрамы шамалы (10-7-10-6%), ал мұхиттың терең жерлерінде оның концентрациясы суда еритін оттегінің тотығуына байланысты 0,3% - ға дейін көтеріліп, суда ерімейтін марганец оксидін түзеді, ол гидратталған түрінде (MnO2 * xH2O·және мұхиттың төменгі қабаттарына түсіп, темір-марганец түйіндерін құрайды. марганец мөлшері 45% - ға жететін күн (сондай-ақ оларда мыс, никель, кобальт қоспалары бар). Мұндай ерекшеліктер болашақта өнеркәсіп үшін марганецтің көзі бола алады.
Ресейде бұл өте тапшы шикізат, кен орындары белгілі: Кемерово облысындағы" Усинское", Свердловск облысындағы "түн ортасы", Краснояр өлкесіндегі "Порожинское", Еврей автономиялық аймағындағы "Южно-Хинганское", "Рогачево-Тайнинская" алаңы және жаңа жердегі "Солтүстік-Тайнинское" өрісі.
2.3 Марганецтін физика химиялық қасиеттері
Физикалық қасиеттері
Марганец күмістей ақ түсті, морт, ауыр металл. Марганец электрохимиялық кернеу қатарында алюминий мен мырыштың арасынан орын алады. Бұл жағдайда оның химиялық акивтігінің жоғары екенін көрсетеді. Марганец қалыпты жағдайда тығыз оксидтер қабатымен қапталады, ал бұл қабат металды ары қарай тотығудан сақтайды.
Электронның шығу жұмысы: 4,1 эВ
Жылу кеңейту коэффициенті: 0,000022 K-1 (0 °C кезінде)
Электрөткізгіштігі: 0,00695⋅106 ОМ−1·см−1
Жылу өткізгіштік: 0,0782 Вт / (см·K)
Атомизация энтальпиясы: 25 °C температурада 280,3 кДж / моль
Балқу энтальпиясы: 14,64 кДж / моль
Булану энтальпиясы: 219,7 кДж / моль
Қаттылық:
Бринелл шкаласы бойынша: Мн/м2
мох шкаласы бойынша: 4
Бу қысымы: 1244 ° C температурада 121 Па
Молярлық көлемі: 7,35 см3 / моль
Марганецтің тән тотығу күйлері: 0, +2, +3, +4, +6, +7 (тотығу дәрежесі +1, + 5 төмен).
Ауада тотығу кезінде ол пассивті болады. Ұнтақты марганец оттегіде күйіп кетеді:
Mn + O2 ⟶ MnO2
Mn + 2H2O →∘t Mn(OH)2 + H2↑
Бұл жағдайда пайда болған марганец гидроксиді қабаты реакцияны баяулатады.
Марганец сутекті сіңіреді, температураның жоғарылауымен оның марганецтегі ерігіштігі артады. 1200 °C-тан жоғары температурада азотпен әрекеттесіп, құрамы әр түрлі нитридтер түзеді.
Көміртек балқытылған марганецпен әрекеттесіп, mn3c карбидтерін және басқаларын құрайды. Ол сонымен қатар силицидтер, боридтер, фосфидтер түзеді.
Тұз және күкірт қышқылдарымен теңдеу арқылы әрекеттеседі
Mn + 2H+ ⟶ Mn2+ + H2↑
Сілтілі ерітіндіде марганец тұрақты.
Марганец қыздырғанда оттегімен, күкіртпен, галогендермен, азотпен, көміртегімен әрекеттеседі, ал сумен ондан сутекті ығыстырады:
Mn0 + 2H+ OH = Mn2+(OH)2H20
Тұз қышқылымен және сұйытылған күкірт қышқылымен марганец қуатты түрде әрекеттесіп олардан сутегін ығыстырады:
Mn0 + H2SO4 = MnSO4 + H20
Марганец электрохимиялық кернеу қатарында өзінен кейін орналасқан металдарды олардың тұздарынан ыңыстырады:
Mn0 + CuSO4 = MnSO4 + Cu0
Марганец концентрлі күкірт қышқылымен және азот қышқылымен әрекеттесіп тотығады:
Mn0 + 2H2SO4 = MnSO4 +SO2 + H2O
3Mn + 8HNO3 = 3Mn (NO3)2 + 2NO + 4H2O
Марганец минералдары
пиролюзит MnO2 * xH2O, ең көп таралған минерал (құрамында 63,2% марганец бар);
манганит(қоңыр марганец кені) MnO (OH) (марганецтің 62,5%);
браунит 3mn2o3 * MnSiO3 (69,5% марганец);
гаусманит (MnIIMn2III)O4;
родохрозит (марганец шпаты, таңқурай шпаты) MnCO3 (марганецтің 47,8%);
псиломелан mMnO * MnO2 * nH2O (45-60% марганец);
күлгін Mn3 + [PO4], (марганецтің 36,65%).
2.4Марганец қосылыстары
Ең тұрақты оксидтер мен гидроксидтер +2, +3, +4 және +7 тотығу күйі бар марганец қосылыстары болып табылады. Бұл қатарда тотығу күйінің жоғарылауымен оксидтер мен гидроксидтердің қышқылдық қасиеттері және олардың тотығу қасиеттері артады
Марганец (II) оксиді (МпО) — суда ерімейтін сұр-сары кристалды зат. Жартылай өткізгіш. Марганец (II) оксиді-сонымен қатар оған сәйкес келетін гидроксиді (MP (oh)2) негізгі қасиеттерге ие, мысалы қышқылдармен әрекеттеседі:

Марганец оксиді (II) сутегі мен белсенді металдармен қызған кезде марганец қалпына келеді:
 Марганец оксиді (II) гидроксиді мен марганец нитратының ыдырауы арқылы алынады: Марганец оксиді (II) гидроксиді мен марганец нитратының ыдырауы арқылы алынады:

Марганец гидроксиді (II)Мп(oh) 2 — бозғылт қызғылт кристалды зат. Ол негізгі және әлсіз тотықсыздану қасиеттеріне ие: ол ауа оттегімен және басқа тотықтырғыштармен марганец қышқылына немесе оның манганат тұздарына тотығады:
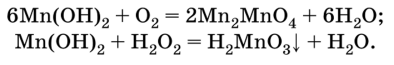
Марганец (II) гидроксиді марганец (II)тұздарының ерітінділеріне сілтілердің әсерінен алынады:
М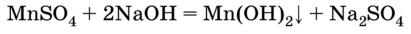 арганец тұздары (II) — суда жақсы еритін бозғылт қызғылт, кристалды заттар. Олар күшті тотықсыздандырғыштардың қасиеттерін көрсетеді, ал марганец тотықтырғыштың күші мен ортаның рН-на байланысты +4, +6, +7 тотығу күйіне дейін тотығуы мүмкін. арганец тұздары (II) — суда жақсы еритін бозғылт қызғылт, кристалды заттар. Олар күшті тотықсыздандырғыштардың қасиеттерін көрсетеді, ал марганец тотықтырғыштың күші мен ортаның рН-на байланысты +4, +6, +7 тотығу күйіне дейін тотығуы мүмкін.

Марганец оксиді (IV) немесе марганец диоксиді (Mp02) — суда ерімейтін қоңыр-қара зат. Оның гидроксиді (МП (ОН)4) сияқты амфотериялық қасиеттерін де көрсетеді:
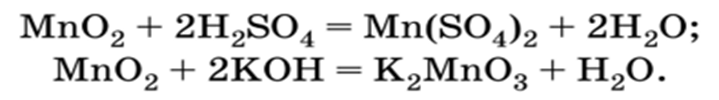
2.5 Марганец қосылыстарының қолдану аясы
Марганец сульфаты (MnS04) катализатор ретінде тоқыма өнеркәсібіндегі бояғыштардың құрамдас бөлігі ретінде марганецтің басқа қосылыстарын синтездеу үшін қолданылады.
Марганец нитраты(Mn (N03)2) — оксидті катализаторларды алу үшін микротыңайтқыштардың құрамдас бөлігі ретінде және лак-бояу материалдарының (сиккативтер заттары) кебуін тездететін заттар ретінде қолданылады.
Марганец карбонаты (Mps03) — бояғыш ретінде қолданылады (марганец ақ), сиккативтер мен айналы шойын алу үшін.
Марганец (IV) оксиді марганец пен оның қосылыстарын алу үшін, қоңыр бояудың (умбраның) құрамдас бөлігі ретінде, құрғақ химиялық ток көздерінде, әйнек өндірісінде ағартқыш ретінде, сондай-ақ Органикалық химиядағы тотықтырғыш ретінде қолданылады.
ІІІ.Қорытынды
Марганец-биогендік элемент, жануарлар мен өсімдік жасушаларында химиялық процестердің қалыпты жүруі үшін қажет он металдың бірі. Ересек адамның денесінде 12 мг марганец бар. Организмде марганец ақуыздар, нуклеин қышқылдары және кейбір аминқышқылдары бар кешендер түзеді. Марганец кейбір ферменттердің құрамына кіреді, мысалы аргиназа және холинестераза. Магний сияқты марганец жасуша энергиясы мен тіршілігін қамтамасыз ететін аде - нозинтрифосфор қышқылының (АТФ) гидролизін белсендіреді. Марганец иондары нуклеин қышқылдарының нуклеотидтерге ыдырауын жүзеге асыратын нуклеаза ферменттерін белсендіреді.
VI.Пайдалнылған әдебиеттер
1.https://studref.com/563938/matematika_himiya_fizik/soedineniya_margantsa?ysclid=l8cjfgeqcr786186290
2.https://ru.wikipedia.org/wiki/%D0%9C%D0%B0%D1%80%D0%B3%D0%B0%D0%BD%D0%B5%D1%86
3.https://chem.ru/marganec.html?ysclid=l8aemnpple592626032#%D0%A0%D0%B0%D1%81%D0%BF%D1%80%D0%BE%D1%81%D1%82%D1%80%D0%B0%D0%BD%D1%91%D0%BD%D0%BD%D0%BE%D1%81%D1%82%D1%8C_%D0%B2_%D0%BF%D1%80%D0%B8%D1%80%D0%BE%D0%B4%D0%B5 |
|
|
 Скачать 388.08 Kb.
Скачать 388.08 Kb.