Болезнь Альцгееймера. Болезнь Альцгеймера
 Скачать 0.88 Mb. Скачать 0.88 Mb.
|
Биохимия болезни Альцгеймера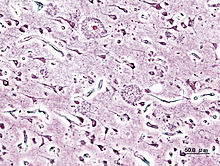 Гистопатологический образец участкакоры головного мозга с сенильными бляшками. Импрегнация серебром. [править]Нейропатология Болезнь характеризуется потерей нейронов и синаптических связей в коре головного мозга и определённых субкортикальных областях. Гибель клеток приводит к выраженной атрофии поражённых участков, в том числе к дегенерации височных и теменной долей, участков фронтальной коры и поясной извилины.[61] Как амилоидные бляшки, так и нейрофибриллярные клубки хорошо заметны под микроскопом при посмертном анализе образцов мозга больных.[10] Бляшки представляют собой плотные, в большинстве случаев нерастворимые отложения бета-амилоида и клеточного материала внутри и снаружи нейронов. Внутри нервных клеток они растут, образуя нерастворимые закрученные сплетения волокон, часто называемые клубками. У многих пожилых людей в мозге образуется некоторое количество бляшек и клубков, однако при болезни Альцгеймера их больше в определённых участках мозга, таких как височные доли.[73] [править]Биохимия 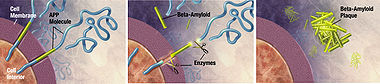 Ферменты разрезают предшественник бета-амилоида на участки, один из которых играет ключевую роль в формировании сенильных бляшек при болезни Альцгеймера. Установлено, что болезнь Альцгеймера является протеинопатией — заболеванием, связанным с накоплением в тканях мозга ненормально свёрнутых белков — бета-амилоида и тау-белка.[74] Бляшки образуются из малых пептидов длиной в 39-43аминокислоты, именуемых бета-амилоидом (тж. A-beta, Aβ). Бета-амилоид является фрагментом более крупного белка-предшественника — APP. Этот трансмембранный белок играет важную роль в росте нейрона, его выживании и восстановлении после повреждений.[75][76] При болезни Альцгеймера по неизвестным пока причинам APP подвергается протеолизу — разделяется на пептиды под воздействием ферментов.[77] Бета-амилоидные нити, образованные одним из пептидов, слипаются в межклеточном пространстве в плотные образования, известные как сенильные бляшки.[10][78]  При болезни Альцгеймера изменения в структуре тау-белка приводят к дезинтеграции микротрубочек в клетках мозга. Более специфически, болезнь Альцгеймера относят также к таупатиям — болезням, связанным с ненормальной агрегацией тау-белка. Каждый нейрон содержит цитоскелет, отчасти составленный из микротрубочек, которые действуют подобно рельсам, направляя питательные вещества и другие молекулы из центра на периферию клетки, к окончанию аксона, и обратно. Тау-белок, наряду с несколькими другими белками, ассоциирован с микротрубочками, в частности, после фосфорилирования он их стабилизирует. При болезни Альцгеймера тау-белок подвергается избыточному фосфорилированию, из-за чего нити белка начинают связываться друг с другом, слипаться в нейрофибриллярные клубки и разрушать транспортную систему нейрона.[79] [править]Патологический механизм Неизвестно, как именно нарушение синтеза и последующее скопление бета-амилоидных пептидов вызывает патологические отклонения при болезни Альцгеймера.[80] Амилоидная гипотеза традиционно указывала на скопление бета-амилоида как на основное событие, запускающее процесс нейрональной дегенерации. Считается, что отложения нарушают гомеостаз ионов кальция в клетке и провоцируют апоптоз.[81]Известно, что местом скопления Aβ в нейронах пациентов являются митохондрии, также этот пептид ингибирует работу некоторых ферментов и влияет на использование глюкозы.[82] Воспалительные процессы и цитокины могут играть роль в патофизиологии. Поскольку воспаление является признаком повреждения тканей при любом заболевании, при болезни Альцгеймера оно может играть вторичную роль по отношению к основной патологии либо представлять собой маркер иммунной реакции.[83] [править]Генетика Известны три гена, мутации которых в основном позволяют объяснить происхождение редкой ранней формы, однако распространенная форма болезни Альцгеймера пока не укладывается в рамки исключительно генетической модели. Наиболее выраженным генетическим фактором риска на данный момент считается APOE, но вариации этого гена ассоциированы лишь с некоторыми случаями болезни.[84] Менее 10 % случаев болезни в возрасте до 60 лет связаны с аутосомно-доминантными (семейными) мутациями, которые в общем массиве составляют менее 0.01 %.[84][85][86] Мутации обнаружены в генах APP, пресенилина 1 и пресенилина 2,[84] большинство из них усиливают синтез малого белка Abeta42, основного компонента сенильных бляшек.[87] В роду большинства больных не отмечается предрасположенности к заболеванию, однако гены могут отчасти обуславливать риск. Самый известный генетический фактор риска — наследуемая аллель E4 гена APOE, с которой может быть связано до половины случаев поздней спорадической болезни Альцгеймера.[88] Генетики сходятся в мнении о том, что многие другие гены могут в какой-то степени способствовать либо препятствовать развитию поздней болезни Альцгеймера.[84] Всего на ассоциацию с этим распространенным типом болезни проверено более 400 генов.[84] Один из недавних примеров — вариация гена RELN, связанная с повышенной заболеваемостью у женщин.[89] [править]Диагностика 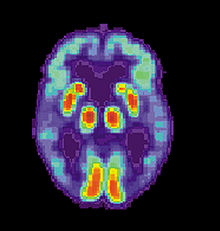 PET-сканирование мозга при болезни Альцгеймера демонстрирует угасание активности в височных долях. Клинический диагноз болезни Альцгеймера обычно основан на истории пациента (анамнезе жизни), истории его родственников и клинических наблюдений (наследственном анамнезе), при этом учитываются характерные неврологические и нейропсихологические признаки и исключаются альтернативные диагнозы.[90][91] Для того, чтобы отличить болезнь от других патологий и разновидностей деменции, могут быть использованы сложные методы медицинской визуализации — компьютерная томография, Магнитно-резонансная томография, фотонно эмиссионная компьютерная томография или Позитронно-эмиссионная томография.[92] Для более точной оценки состояния проводится тестирование интеллектуальных функций, в том числе памяти.[4] Медицинские организации вырабатывают диагностические критерии с целью облегчить диагностику практикующему врачу и стандартизировать процесс постановки диагноза. Иногда диагноз подтверждается либо устанавливается посмертно при гистологическом анализе тканей мозга.[93] [править]Диагностические критерии Национальный институт неврологических и коммуникативных расстройств и инсульта (NINDS) и Ассоциация болезни Альцгеймера составили наиболее часто используемый набор критериев для диагностики болезни Альцгеймера.[94] Согласно критериям, для постановки клинического диагноза возможной болезни Альцгеймера требуется подтвердить наличие когнитивных нарушений и предположительного синдрома деменции в ходе нейропсихологического тестирования. Для окончательного подтверждения диагноза необходим гистопатологический анализ тканеймозга, и в ходе сверки прижизненных диагнозов по критериям с посмертным анализом были отмечены хорошая статистическая надёжность и проверяемость.[95] Чаще всего нарушения при болезни Альцгеймера затрагивают восемь доменов: память, языковые навыки, способность воспринимать окружающее, конструктивные способности, ориентирование в пространстве, времени и собственной личности, навыки решения проблем, функционирования, самообеспечения. Эти домены эквивалентны критериям NINCDS-ADRDA, перечисленным в DSM-IV-TR.[96][97] [править]Методы диагностики  В диагностике болезни Альцгеймера может помочь нейропсихологическоескрининг-тестирование, при котором пациенты копируют фигуры, запоминают слова, читают, выполняют арифметические действия. 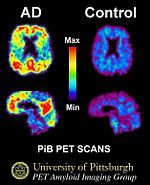 ПЭТ-сканирование: При болезни Альцгеймера, введённый в организмПиттсбургский состав Bскапливается в мозге, закрепляясь за отложения бета-амилоида (слева). Справа - мозг пожилого человека без признаков болезни Альцгеймера. Нейропсихологические тесты, например, MMSE, широко применяются для оценки когнитивных нарушений, которые должны присутствовать при заболевании. Для получения надёжных результатов требуются более развёрнутые наборы тестов, особенно на ранних стадиях болезни.[98][99] В начале болезни неврологический осмотр обычно не показывает ничего необычного, за исключением явных когнитивных отклонений, которые могут напоминать обычную деменцию. Ввиду этого, для дифференциальной диагностики болезни Альцгеймера и других заболеваний важно расширенное неврологическое исследование.[4] Беседа с членами семьи также используется при оценке хода болезни, поскольку родственники могут предоставить важную информацию об уровне повседневной активности человека и о постепенном снижении его мыслительных способностей.[100] Так как сам пациент обычно не замечает нарушений, точка зрения ухаживащих за ним людей особенно важна.[101] В то же время во многих случаях ранние симптомы деменции остаются незамеченными в семье и врач получает от родственников неточную информацию.[102] Дополнительные тесты обогащают картину информацией о некоторых аспектах болезни либо позволяют исключить другие диагнозы. Анализ крови может выявить альтернативные причины деменции,[4] которые изредка даже поддаются терапии, обращающей симптомы вспять.[103] Также применяются психологические тесты для выявления депрессии, которая может как сопутствовать болезни Альцгеймера, так и являться причиной когнитивного снижения.[104][105] Аппаратура SPECT- и PET-визуализации при её доступности может быть использована для подтверждения диагноза совместно с другими методами оценки, включающими анализ ментального статуса.[106] У людей, уже страдающих от деменции, SPECT, по некоторым данным, позволяет более эффективно дифференцировать болезнь Альцгеймера от других причин, по сравнению со стандартным тестированием и рассмотрением анамнеза.[107]Возможность наблюдать отложения бета-амилоида в мозге живых людей появилась благодаря созданию в Питтсбургском университете Питтсбургского состава B (PiB), связывающегося с амилоидными отложениями при введении в организм. Короткоживущий радиоактивный изотоп углерод-11 в соединении позволяет определять распределение этого вещества в организме и получать картину амилоидных отложений в мозге больного с помощьюПЭТ-сканера.[108] Показано также, что объективным маркером болезни может быть содержание бета-амилоида либо тау-белка в спинномозговой жидкости.[109] Эти два новых метода вызвали предложения о разработке новых диагностических критериев.[4][94] [править]Профилактика заболевания  Интеллектуальная активность, в том числе увлечение игрой в шахматы, и регулярное общение коррелируют со сниженным риском развития болезни Альцгеймера, по данным эпидемиологических исследований, однако причинно-следственная связь пока не доказана. Международные исследования, призванные оценить, насколько та или иная мера способна замедлить или предотвратить наступление болезни, нередко дают противоречивые результаты. К настоящему времени нет твердых свидетельств превентивного действия любого из рассматривавшихся факторов.[110]Вместе с тем, эпидемиологические исследования говорят о том, что некоторые поддающиеся коррекции факторы — диета, риск сердечно-сосудистых заболеваний, прием лекарств, мыслительная активность и другие — ассоциированы с вероятностью развития болезни. Однако реальные доказательства их способности предупредить болезнь могут быть получены лишь в ходе дополнительного изучения, в которое будут входить клинические исследования.[111] Ингредиенты средиземноморской диеты, в том числе фрукты и овощи, хлеб, пшеница и другие крупяные культуры, оливковое масло, рыба и красное вино, возможно, способны по отдельности либо в совокупности снижать риск и смягчать течение болезни Альцгеймера.[112] Приём некоторых витаминов, в их числе B12, B3, C и фолиевая кислота, в ходе некоторых исследований был связан со сниженным риском развития болезни,[113] однако другие работы говорят об отсутствии значимого воздействия на начало и течение болезни и о вероятности побочных эффектов.[114] Куркумин, содержащийся враспространённой специи, при исследовании на мышах показал некоторую способность предотвращать определённые патологические изменения в мозге.[115] Факторы риска сердечно-сосудистых заболеваний, такие как высокий уровень холестерина и гипертензия, диабет, курение, ассоциированы с повышенным риском и более тяжелым течением болезни Альцгеймера,[116][117] но средства, снижающие холестерин (статины) не показали эффективности в её предотвращении либо улучшении состояния больных.[118][119] Долговременное применение нестероидных противовоспалительных средств ассоциировано со сниженной вероятностью развития болезни у некоторых людей.[120] Другие лекарства, например, гормонозаместительная терапия у женщин, более не считаются эффективными в предотвращении деменции.[121][122]Систематический обзор гинкго билоба, проведённый в 2007 году, говорит о непоследовательном и неубедительном характере представленных свидетельств воздействия препарата на когнитивные нарушения,[123] а еще одно исследование говорит об отсутствии действия на заболеваемость.[124] Интеллектуальные занятия, такие как чтение, настольные игры, разгадывание кроссвордов, игра на музыкальных инструментах, регулярное общение, возможно, способны замедлить наступление болезни либо смягчить её развитие.[125][126] Владение двумя языками ассоциировано с более поздним началом болезни Альцгеймера.[127] Некоторые исследования говорят о повышенном риске развития болезни Альцгеймера у тех людей, чья работа связана с воздействием магнитных полей,[128][129] попаданием в организм металлов, особенно алюминия,[130][131] или использованием растворителей.[132] Некоторые из этих публикаций подверглись критике за низкое качество работы,[133] к тому же в других исследованиях не обнаружено связи факторов внешней среды с развитием болезни Альцгеймера.[134][135][136][137] [править]Терапия и уход От болезни Альцгеймера невозможно излечиться; доступные методы терапии способны в небольшой степени повлиять на симптомы, но по своей сути являются паллиативнымимерами. Из всего комплекса мер можно выделить фармакологические, психосоциальные и меры по уходу за больным. [править]Фармакотерапия  Трёхмерная структура донепезила,ингибитора ацетилхолинэстеразы, используемого для симптоматической терапии.  Молекулярная структура мемантина, средства, одобренного к применению при болезни Альцгеймера. Регулирующими агентствами, такими как FDA и EMEA, в настоящее время одобрены четыре препарата для терапии когнитивных нарушений при болезни Альцгеймера — три ингибитора холинэстеразы и мемантин, NMDA-антагонист. При этом нет таких лекарств, среди действий которых было бы указано замедление либо остановка развития болезни Альцгеймера. Известным признаком болезни Альцгеймера является снижение активности холинергических нейронов.[138] Ингибиторы холинэстеразы снижают скорость разрушения ацетилхолина (ACh), повышая его концентрацию в мозге и компенсируя потерю ACh, вызванную потерей холинергических нейронов.[139] По состоянию на 2008 год, врачами использовались такие ACh-ингибиторы как донепезил,[140] галантамин,[141] и ривастигмин (в форме таблеток[142] и пластыря[143]) Есть свидетельства эффективности этих препаратов на начальной и умеренной стадиях,[144] а также некоторые основания к их применению на поздней стадии. Только донепезил одобрен к применению при наступлении тяжелой деменции.[145]Использование этих препаратов при мягком когнитивном нарушении не замедлило наступления болезни Альцгеймера.[146] Среди побочных действий препаратов самыми распространёнными являются чувство тошноты и рвота, связанные с избытком холинергической активности, они возникают у 1-10 % пациентов и могут быть слабо- либо умеренновыраженными. Реже встречаются спазмы мышц, брадикардия, снижение аппетита, потеря веса, увеличение кислотности желудочного сока.[147] Возбудительный нейротрансмиттер глутамат играет важную роль в работе нервной системы, но его избыток ведет к чрезмерной активацииглутаматных рецепторов и может вызывать гибель клеток. Этот процесс, называемый эксайтотоксичностью, отмечается не только при болезни Альцгеймера, но и при других состояниях, например, при болезни Паркинсона и рассеянном склерозе.[148] Препарат под названиемМемантин,[149] изначально применявшийся при лечении гриппа, ингибирует активацию глутаматных NMDA-рецепторов.[148] Показана умеренная эффективность мемантина при болезни Альцгеймера умеренной и сильной тяжести, но неизвестно, как он действует на ранней стадии.[150]Редко отмечаются слабовыраженные побочные эффекты, среди них — галлюцинации, замешательство, головокружение, головная боль и утомление.[151] В комбинации с донепезилом мемантин демонстрирует «статистически значимую, но клинически едва заметную эффективность» в действии на когнитивные показатели.[152] У пациентов, чьё поведение представляет проблему, антипсихотики могут в умеренной степени снизить агрессию и воздействовать на психоз. В то же время эти препараты вызывают серьёзные побочные эффекты, в частности, цереброваскулярные осложнения, двигательные нарушения и снижение когнитивных способностей, что исключает их повседневное использование.[153][154] При длительном назначении антипсихотиков при болезни Альцгеймера отмечается повышенная смертность.[154] [править] |
