Фармхимия_Задание_16_Бахриддинова_Дилноза_Ф_310А. C5H11N02s m в. 149,21 Описание
 Скачать 0.73 Mb. Скачать 0.73 Mb.
|
|
Анализ алифатических аминокислот. Метионин, глютаминовая кислота и глицин.8   Метионин Methioninum d,l-альфа-Амино-гамма-метилтиомасляная кислота 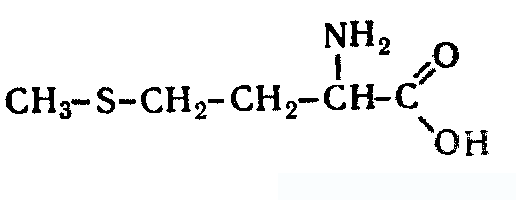 C5H11N02S M. в. 149,21 Описание. Белый кристаллический порошок с характерным запахом и слегка сладковатым вкусом. Растворимость. Трудно растворим в воде, практически нерастворим в органических растворителях, легко растворим в разведенных минеральных кислотах, растворах едких щелочей и аммиака, растворим в растворе карбоната натрия. Подлинность. 0,05 г препарата растворяют в 1 мл воды при нагревании, прибавляют 5-6 капель раствора нингидрина; появляется сине-фиолетовое окрашивание. 0,05 г препарата нагревают в пробирке с 5-6 каплями 30% раствора едкого натра до получения сплава. Пробирку закрывают кусочком фильтровальной бумаги, которую смачивают 1-2 каплями свежеприготовленного 5 % раствора нитропруссида натрия; на фильтровальной бумаге появляется красно-фиолетовое окрашивание. К охлажденному сплаву добавляют 5 мл воды и подкисляют разведенной серной кислотой; появляется запах сероводорода и меркаптана. Прозрачность и цветность раствора. Растворы 0,5 г препарата в 20 мг роды при 25° и 0,5 г препарата в 5 мл разведенной соляной кислоты должны быть прозрачными и бесцветными. Хлориды. 0,8 г препарата растворяют в 40 мл воды при 25° в течение 5 минут. 10 мл полученного раствора должны выдерживать испытание на хлориды (не более 0,01 % в препарате). Сульфаты. 10 мл того же раствора должны выдерживать испытание на сульфаты (не более 0,05% в препарате). Соли аммония. 0,2 г препарата нагревают до кипения с 3 мл раствора едкого натра Влажная красная лакмусовая бумага не должна синеть в парах кипящей жидкости. Цианиды. К 0,5 г препарата прибавляют 10 мл воды, 5 капель раствора сульфата закисного железа, 2 капли раствора хлорида окисного железа, 1 мл раствора едкого натра и слегка нагревают. После подкис-ления соляной кислотой смесь не должна окрашиваться в синий цвет. Потеря в весе при высушивании. Около 0.5 г препарата (точная навеска) сушат при 100-105° до постоянного веса. Потеря в весе не должна превышать 0,5% Сульфатная зола и тяжелые металлы. Сульфатная зола из 0,5 г препарата не должна превышать 0,1% и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в препарате). Мышьяк. 0,5 г препарата не должны давать реакции на мышьяк. Количественное определение. 1. Около 0,1 г препарата (точная навеска) помешают в колбу Кьельдаля емкостью 200 мл и далее поступают, как указано в статье «Определение азота в органических соединениях». После просветления раствора сжигание продолжают в течение 4-41/2 часов. Содержание общего азота в препарате должно быть не менее 9,2% и не более 9.5% 2. Около 0,3 г препарата (точная навеска) помещают в коническую колбу емкостью 250 мл, растворяют в 100 мл воды, прибавляют 5 г фосфата калия двузамешенного, 2 г фосфата калия однозамешенного, 2 г йодида калия и взбалтывают до полного растворения. Затем прибавляют точно 50 мл 0,1 н. раствора йода, закрывают колбу, хорошо перемешивают и оставляют на 30 минут Избыток йода оттитровывают 0,1 н. раствором тиосульфата натрия, прибавляя в конце титрования раствор крахмала. Параллельно проводят контрольный опыт. 1 мл 0,1 н. раствора йода соответствует 0,007461 г C5H11N02S, которого в пересчете на сухое вещество должно быть не менее 98,5%. Хранение. В хорошо укупоренных банках оранжевого стекла, в защищенном от света месте. Глицин, таблетки Таbulettae Glycini Настоящая фармакопейная статья распространяется на лекарственный препарат глицин, таблетки (таблетки, таблетки подъязычные, таблетки защёчные). Препарат должен соответствовать требованиям ОФС «Таблетки» и ниже приведенным требованиям. Cодержит не менее 90,0 % и не более 110,0 % от заявленного количества глицина C2H5NO2. Описание. Таблетки белого цвета, допускается наличие мраморности. Подлинность. 1. Качественная реакция. 50 мг порошка растёртых таблеток растворяют в 50 мл воды. К 10 мл полученного раствора прибавляют 0,2 мл раствора нингидрина в ацетоне и нагревают; должно появиться синевато-фиолетовое окрашивание. 2. Тонкослойная хроматография. Основная зона адсорбции на хроматограмме испытуемого раствора, полученной в испытании "Родственные примеси", по положению должна соответствовать основной зоне адсорбции на хроматограмме раствора сравнения. Однородность массы В соответствии с ОФС «Однородность массы дозированных лекарственных форм». Распадаемость. От 10 до 30 мин (ОФС «Распадаемость таблеток и капсул»). Родственные примеси. Определение проводят методом ТСХ. Пластинка.ТСХ пластинка со слоем силикагеля. Подвижная фаза (ПФ). Уксусная кислота – вода – бутанол 25:25:50. Испытуемый раствор. Навеску порошка растёртых таблеток, содержащую 0,1 г глицина, помещают в мерную колбу вместимостью 100 мл, прибавляют 50 мл воды, взбалтывают в течение 15 мин, доводят объём раствора водой до метки и фильтруют. Раствор сравнения А. 0,1 г стандартного образца глицинапомещают в мерную колбу вместимостью 100 мл, растворяют в воде и доводят объём раствора водой до метки. Раствор сравнения Б. 1,0 мл раствора сравнения А помещают в мерную колбу вместимостью 200 мл и доводят объём раствора водой до метки. На линию старта пластинки наносят по 5 мкл испытуемого раствора (5 мкг), раствора сравнения А (5 мкг) и раствора сравнения Б (0,025 мкг). Пластинку с нанесенными пробами высушивают на воздухе в течение 5 мин, помещают в камеру с ПФ и хроматографируют восходящим способом. Когда фронт ПФ пройдет около 80–90 % длины пластинки от линии старта, её вынимают из камеры, сушат до удаления следов растворителей, выдерживают в сушильном шкафу при температуре 80 °С в течение 30 мин. Охлаждённую до комнатной температуры пластинку опрыскивают 0,2 % раствором нингидрина и выдерживают в сушильном шкафу при температуре 100–105 °С в течение 15 мин. Хроматографическая система считается пригодной, если на хроматограмме раствора сравнения Б чётко видна зона адсорбции основного вещества. Зона адсорбции любой примеси на хроматограмме испытуемого раствора по совокупности величины и интенсивности поглощения не должна превышать зону адсорбции на хроматограмме раствора сравнения Б. Суммарное содержание примесей не должно превышать 2 %. Микробиологическая чистота. В соответствии с ОФС «Микробиологическая чистота». Количественное определение. Определение проводят методом титриметрии. Точную навеску порошка растертых таблеток, содержащую около 70 мг глицина, помещают в коническую колбу вместимостью 100 мл, прибавляют 25 мл безводной уксусной кислоты и нагревают на водяной бане с обратным холодильником до растворения. После охлаждения до комнатной температуры полученный раствор титруют 0,1 М раствором хлорной кислоты до перехода окраски в зелёную (индикатор – 0,1 мл 0,5 % раствора кристаллического фиолетового) или потенциометрически с использованием стеклянного электрода в качестве индикаторного. Параллельно проводят контрольный опыт. 1 мл 0,1 М раствора хлорной кислоты соответствует 7,507 мг глицина C2H5NO2. Хранение. В плотно закрытой упаковке, в защищенном от света месте. Методы количественного определения Выделяют несколько методов количественного определения: М 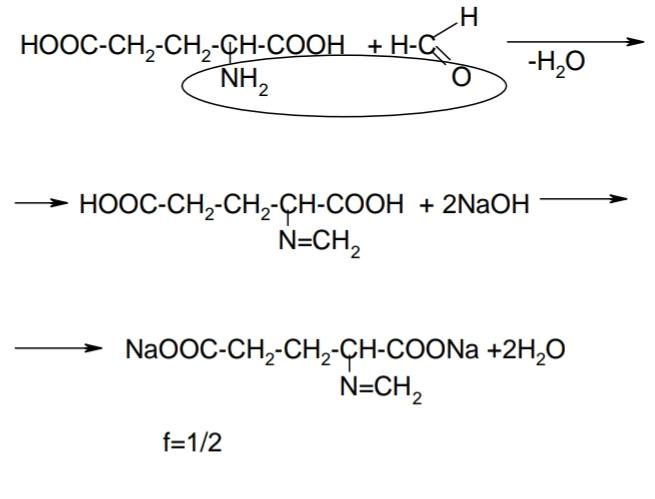 етод алкалиметрический по Серенсену, способ прямого титрования, индикатор фенолфталеин. Способ заключается в образовании Шиффова производного по аминогруппе кислоты с формальдегидом и последующим титрованием щелочью обеих карбоксильных групп. Аминокислоты в водных растворах ведут себя как биполярные ионы. В связи с этим, непосредственное титрование аминокислот раствором NаОН затруднено. Для количественного определения аминокислот применяется так называемое формольное титрование. Образовавшееся производное имеет сильно кислый характер и дает четкую точку эквивалентности по фенолфталеину. Алкалиметрический метод прямого титрования щелочью в присутствии индикаторов бромтимолового синего или нейтрального красного (до оранжевого окрашивания). В этом случае оттитровывается только одна карбоксильная группа: 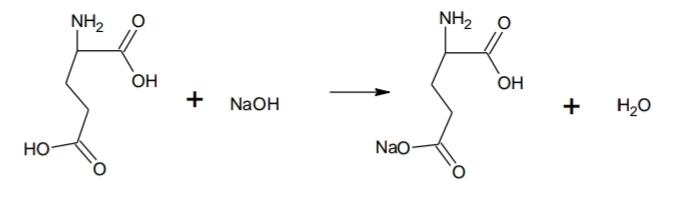 Метод Кьельдаля. Классический метод Кьельдаля. Метод основан на предварительной минерализации азотсодержащего органического соединения до гидросульфата аммония. Определение выполняют с помощью прибора. 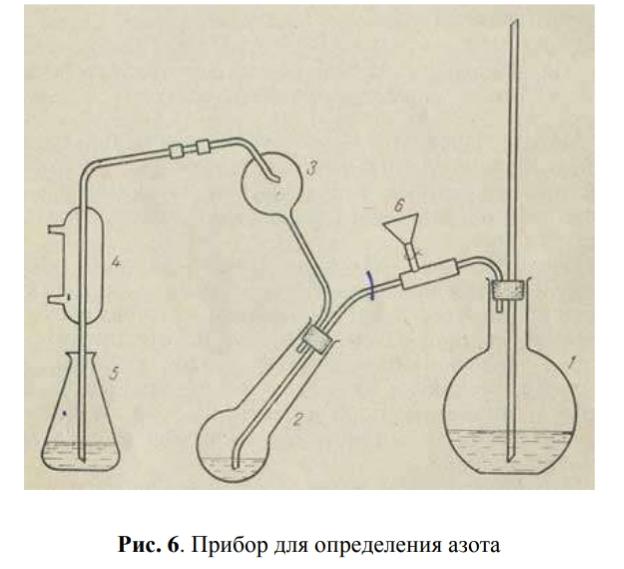 Прибор для определения азота состоит из: ▪︎парообразователя с предохранительной трубкой – 1 ▪︎сменных грушевидных колб с длинным горлом – 2 ▪︎воронки для ввода щелочи – 6 ▪︎брызгоуловителя – 3 ▪︎прямого холодильника – 4 ▪︎сменных конических колб – приемников - 5 Определение состоит из нескольких стадий: 1)Минерализация (нагревание с концентрированной серной кислотой): 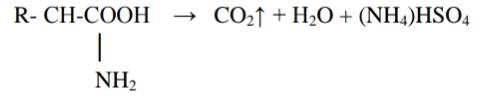 2) Разложение (NH4)HSO4 гидроксидом натрия и отгонка образующегося аммиака в приемник: 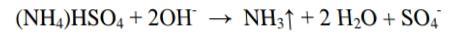 3) Взаимодействие NH3 в приемнике с борной кислотой с образованием тетрагидроксибората аммония: 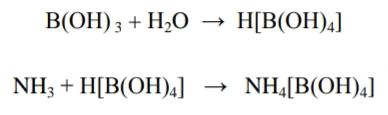 4 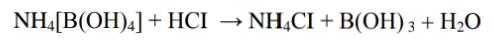 ) Титрование отгона 0,1 М раствором хлористоводородной кислоты: Параллельно проводят контрольный опыт (без анализируемого вещества) для повышения точности результатов титрования. Индикатор метиловый оранжевый. Микрометод Кьельдаля. Все операции проводят аналогично классическому методу, но используют аппарат для автоматического определения азота. Видоизменённый метод Кьельдаля. Количественное определение проводится после щелочного гидролиза по количеству образовавшегося аммиака. Катализатор - К2SO4 + CuSO4∙5H2O. Метод неводного титрования. Кислоты γ–аминомасляная, аминокапроновая, дисульфирам определяют количественно методом неводного титрования. Титруют раствором хлорной кислоты в среде ледяной уксусной кислоты (индикатор кристаллический фиолетовый): 1)Растворение хлорной кислоты в ледяной уксусной кислоте: 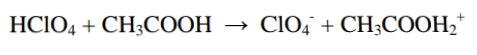 2) Растворениу основания (R3N - кислоты γ–аминомасляная и аминокапроновая) в ледяной уксусной кислоте: 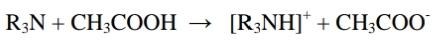 3 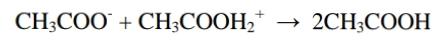 ) Взаимодействие ацетоний- и ацетат-ионов: 4 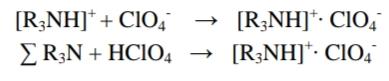 ) Взаимодействие протонированного амина с хлорат-ионом: Кислотно-основное титрование в смешанных растворителях. Данным методом определяют кислоту аминокапроновую. Данный препарат титруют 0,1 М раствором гидроксида натрия в водно-ацетоновой среде (5:25) с индикатором тимолфталеином. Метионин определяют в водно-спиртовой среде (10:20) с тем же индикатором и титрантом. Для определения тетацина кальция используют 0,05М раствор нитрата свинца в присутствии гексаметилентетрамина и разведенной хлористоводородной кислоты, которые выполняют роль буферного раствора. Индикатором служит ксиленоловый оранжевый. Иодатометрический метод используется для определения каптоприла. Т 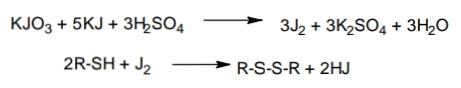 очную навеску каптоприла (около 0,3 г) растворяют в 100 мл воды в колбе с притертой пробкой, добавляют 10 мл 3,6М серной кислоты и 1,0 г иодида калия, 2 мл раствора крахмала. Титруют 0,1М раствором иодида калия до появления голубой окраски, не исчезающей в течение 30 сек. Определение основано на окислении сульфгидрильной группы йодом: Йодометрический метод используется преимущественно для определения серосодержащих аминокислот. Цистеин и ацетилцистеин титруют в кислой среде 0,1 М раствором йода. Определение основано на окислении сульфгидрильных групп: 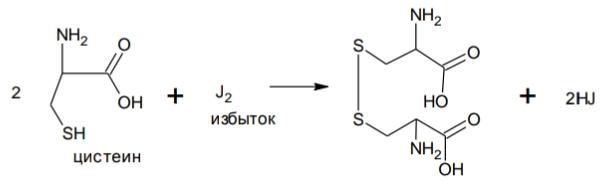 Затем избыток йода оттитровывают стандартным раствором натрия тиосульфата: 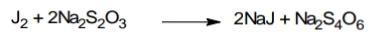 М 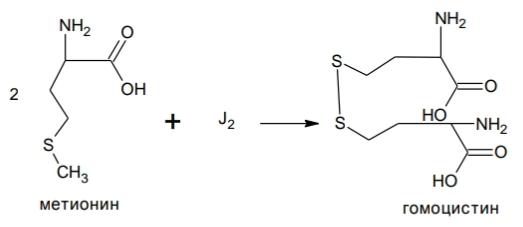 етионин предварительно растворяют в смеси растворов монокалийфосфата и дикалийфосфата (одно и двузамещенного фосфата калия) в присутствии йодида калия, а затем окисляют 0,1 М раствором йода по схеме: Й 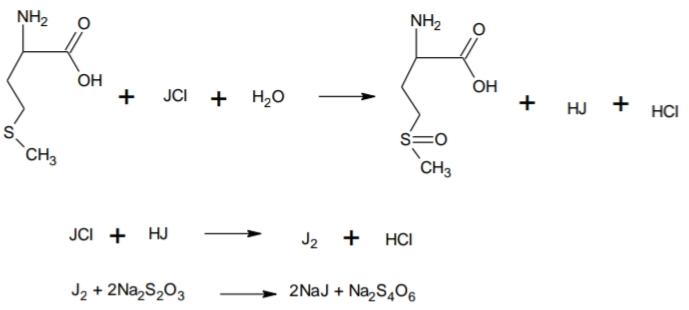 одохлорметрический метод. При йодхлорометрическом титровании метионин окисляется до соответствующего сульфоксида: Комплексонометрия используется для количественного определениядисульфирама, вариант обратной комплексонометрии. Дисульфирам предварительно восстанавливают смесью, состоящей из 10%-ного раствора сульфита натрия и 5%-ного раствора аммиака. Продукт восстановления взаимодействует с 0,1 М раствором сульфита никеля (в течение 1 часа). Образовавшееся соединение никеля извлекают хлороформом и титруют избыток сульфата никеля 0,05 М раствором трилона Б (индикатор мурексид). Фотоколориметрия. Для количественного определения аминокислот используется реакция с ионами меди (ІІ), сопровождающаяся образованием хелатных комплексов. Выделяющиеся при этом ионы водорода нейтрализуют фосфатным или боратным буфером, избыток ионов меди удаляют в виде осадка малорастворимой соли или гидроксида. Затем устанавливают количество меди в образовавшемся комплексе с аминокислотой с помощью фотоколориметрического определения. Спектрофотометрический метод. Метионин и кислоту глутаминовуюидентифицируют с помощью ИК-спектров по совпадению полос поглощения в области 4000-400 см -1 с прилагаемыми к ФС рисунками спектров. УФ-спектрпоглощения цистеина имеет максимум поглощения при 236 нм, а ацетилцистеина – при 233 нм (растворитель 0,1 М раствор гидроксида натрия). Удельные показатели поглощения соответственно равны 690 и 355.Дисульфирам идентифицируют по совпадению полос поглощения ИК-спектраиспытуемого раствора и прилагаемого к ФС рисунка спектра в области 1600-400 см-1. В УФ-области раствор дискльфирама имеет максимум поглощения при 260 нм (растворитель 0,1 М раствор гидроксида натрия). o Количественное определение каптоприла в таблетках выполняют методом УФ-спектрофотометрии при длине волны 212 нм (растворитель – 0,1 М раствор хлористоводородной кислоты). |
