otchet_po_analitu_9 коненый варик. Цель работы определить содержание в растворе катионов меди (II) методом йодометрии. Описание метода анализа
 Скачать 25.4 Kb. Скачать 25.4 Kb.
|
|
Цель работы: определить содержание в растворе катионов меди (II) методом йодометрии. Описание метода анализа: Титрование основано на измерении объёма раствора с известной концентрацией, который необходимо добавить к пробе известного объёма (аликвоте) для протекания аналитической реакции в соответствии со стехиометрическим уравнением. Добавляемый реагент называют титрантом, а его раствор с заданной концентрацией – титрованным раствором. Йодометрические методы основаны на применении стандартного раствора тиосульфата натрия для титрования йода, выделившегося при взаимодействии определяемого окислителя с избытком иодида калия (при титровании по замещению) или оставшегося в избытке при медленном взаимодействии определяемого восстановителя с фиксированным объемом стандартного раствора иода (в случае обратного титрования). Сущность работы: Определение основано на восстановлении меди (II) до меди (I) йодидом калия и последующем титровании образовавшегося в эквивалентном количестве йода раствором тиосульфата натрия: 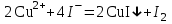 ; ;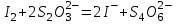 . .Точку эквивалентности определяют по обесцвечиванию крахмала. Выполнение работы: 1. В конические колбы для титрования мерной пипеткой отобрали аликвоты объёмом 10 мл. 2. Добавили 10-15 капель серной кислоты. 3. Разбавили дистиллированной водой до 20-30 мл. 4. Шпателем добавили избыток сухого йодида калия. 5. Поместили колбы на 5 минут в темное место для восстановления меди (II) и образования эквивалентного количества йода. 6. Залили в бюретку тиосульфат натрия, выпустили из носика бюретки воздух и довели уровень раствора до отметки «0». 7. К пробе добавили 5-6 капель крахмала, который служит индикатором на йод. 8. Титровали пробу раствором тиосульфата натрия до исчезновения окраски крахмала. 9. Долили бюретку до нуля и повторили титрование со второй аликвотой. 10. Записали эквивалентные объемы. Результаты эксперимента: Номер пробы: 66. Объем аликвоты Va: 10 мл. Концентрация тиосульфата натрия C(Na2S2O3): 0,1 экв/л. Объем тиосульфата натрия, расходованный на титрование: V1(Na2S2O3) = 5,1 мл; V2(Na2S2O3) = 5,0 мл; Vср(Na2S2O3)2 = 5,05 мл. Обработка результатов эксперимента: 1. Вычислить нормальную концентрацию меди (II) в растворе: 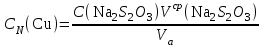 = = 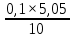 = 0,0505 экв/л. = 0,0505 экв/л.2. Выразить содержание меди (II) в растворе в г/л: 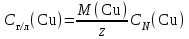 = = 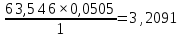 г/л. г/л.Вывод: в данной работе был проведен анализ пробы №66. Методом йодометрии мы определили, что 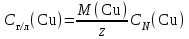 = = 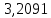 г/л. г/л. |
