лр. ЛР_2_Опред-е_амилолитич._активности_солода. Определение амилолитической активности солода для студентов специальности 5В070100 Биотехнология
 Скачать 34.82 Kb. Скачать 34.82 Kb.
|
 Министерство образования и науки Республики Казахстан Торайгыров университет Кафедра «Биотехнология» Лабораторное занятие №2 Тема: Определение амилолитической активности солода для студентов специальности 5В070100 – Биотехнология Павлодар Цель занятия: освоить методику определения активности ферментов зернового сырья. Реактивы и оборудование: 1 М раствор NаОН, 1,0 М раствор йода, 1 М раствор серной кислоты, 0,1 М раствор тиосульфата натрия, 2 % буферный раствор крахмала, ацетатный буферный раствор рН 4,3. Мерный цилиндр вместимостью 500 см³, стеклянный стакан вместимостью 500 см³, мерная колба вместимостью 200 см³, пипетки вместимостью 100, 50, 10, 5 см³, коническая колба вместимостью 250 см³, водяная баня, электрическая плита, воронка, фильтровальная бумага. Для анализа необходимо 20 г солода или 40 г ячменя. Техника определения Для определения амилолитической активности используется водная вытяжка ячменя, свежепроросшего или сухого солода. При исследовании ячменя используют навеску ячменной муки в 40 г, при исследовании сухого солода -20 г, а при исследовании свежепроросшего солода, особенно в последние сутки проращивания – 10 г. Свежепроросший солод отделяют от ростков, измельчают на мясорубке, в ступке или лабораторной мельнице. Навеску муки (10-40 г) помещают в стеклянный стакан вместимостью 500 см³, добавляют 450 см³ дистиллированной воды, проводят экстракцию в течение 1 часа на водяной бане при температуре 40ºС при периодическом помешивании и стеклянной палочкой содержимого стакана. Стакан охлаждают под струей холодной воды и доводят на технических весах до массы 520 г. Содержимое стакана перемешивают и фильтруют через складчатый бумажный фильтр. Первые порции фильтрата возвращают на фильтр. В мерную колбу вместимостью 200 см³ пипеткой отмеривают 100 см³ 2 % раствора крахмала и выдерживают колбу на водяной бане при температуре 20 ºС в течение 20 минут. Затем в колбу добавляют 5 см³ солодовой вытяжки, содержимое колбы перемешивают и выдерживают на водяной бане при температуре 20 ºС в течение 30 минут для гидролиза крахмала, после чего процесс гидролиза останавливают добавлением 3 см³ 1 М раствора NаОН. Колбу доводят дистиллированной водой до метки и перемешивают. Отмеривают 50 см³ осахаренного раствора крахмала в коническую колбу вместимостью 250 см³. Далее в колбе вносят 25 см³ 0,1 М раствора йода, 3 см³ 1 М раствора NаОН, перемешивают, выдерживают в темном месте 5 минут при комнатной температуре. Затем в раствор добавляют 4,5 см³ 1 М раствора серной кислоты, перемешивают и оттитровывают избыток йода 0,1 М раствором тиосульфата натрия до обесцвечивания раствора. Индикатором служит содержащийся в растворе неосахаренный крахмал, придающий раствору синий цвет. Количество йода, пошедшего на окисление мальтозы, должно находиться в пределах 5-15 см³. Если в реакции связывается более 15 см³ йода, то опыт повторяют с вытяжкой, приготовленной из 10 г солода, если же количество связанного йода менее 5 см³, то опыт повторяют с вытяжкой, приготовленной из 40 г солода. В проведенном определении общее количество йода расходуется не только на окисление образовавшейся мальтозы, но и связывается веществами солодовой вытяжки и крахмала. Поэтому определяют и в расчетах учитывают следующие поправки. Поправка на солодовую вытяжку. В коническую колбу вместимостью 250 см³ отмеривают 12,5 см³ вытяжки, добавляют 37,5 см³ дистиллированной воды. Общий объем должен составлять, как и в основном опыте 50 см³. Затем в колбу добавляют 25 см³ 0,1 М раствора йода, 3 см³ 1 М раствора NаОН, перемешивают, выдерживают в темном месте 5 минут. Затем в раствор добавляют 4,5 см³ 1 М раствора серной кислоты, перемешивают и оттитровывают 0,1 М раствором тиосульфата натрия до обесцвечивания раствора. Так как в основном опыте 50 см³ реакционной смеси содержат 1,25 см³ солодовой вытяжки, то при расчетах берут десятую часть найденной величины. Поправка на раствор крахмала. В коническую колбу вместимостью 250 см³ отмеривают 25 см³ буферного раствора крахмала, добавляют 10 см³ 0,1 М раствора йода и 3 см³ 1 М раствора NаОН, перемешивают и выдерживают в темном месте 5 минут. Затем раствор подкисляют добавлением 4,5 см³ 1 М раствора серной кислоты и оттитровывают 0,1 М раствором тиосульфата натрия до обесцвечивания раствора. Расчет амилолитической активности проводят по формуле : АС = (а - ( 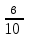 + с)) ·К·17,1, (1) + с)) ·К·17,1, (1)где: а - количество 0,1 М раствора йода, связанного в основном опыте, см³; в - количество 0,1 М раствора йода, связанного с солодовой вытяжкой, см³; с - количество 0,1 М раствора йода, связанного с раствором крахмала, см³; К- коэффициент разбавления солодовой вытяжки в опыте (при использовании 10 г солода К=4, при 20 г К=2, при 40 г К=1); 17,1 - число мг мальтозы, эквивалентное 1 см³ 0,1 М раствору йода. Количество 0,1 М раствора йода, связанного в основном опыте рассчитывают по формуле 2: А = 25 – d , (2) где: d - количество 0,1 М тиосульфата натрия, пошедшего на титрование в основном опыте. Количество 0,1 М раствора йода, связанного с солодовой вытяжкой рассчитывают по формуле 3: В = 25 – е , (3) где: е - количество 0,1 М раствора тиосульфата натрия, пошедшее на титрование солодовой вытяжки. Количество 0,1 М раствора йода, связанного с раствором крахмала рассчитывают по формуле 4: С = 10 – f , (4) где: f- количество 0,1 М раствора тиосульфата натрия, пошедшего на титрование раствора крахмала. Анализ результатов работы Результаты сводят в таблице 1 и делают вывод о содержании ферментов в исследуемых объектах. Таблица 1 - Содержание ферментов в исследуемых объектах
Контрольные вопросы Приведите классификацию ферментов. Какие гидролитические ферменты используются в бродильных производствах. По каким признакам характеризуется ферментный препарат. Какими методами определяется активность амилолитических ферментов. Какую роль выполняют амилолитические ферменты солода. Какие факторы влияют на активность амилолитических ферментов. |
