РГР Аналитика. Чувашский государственный университет имени И. Н. Ульянова ( фгбоу впо чгу им. И. Н. Ульянова)
 Скачать 32.12 Kb. Скачать 32.12 Kb.
|
|
Министерство Образования Российской Федерации Федеральное государственное бюджетное образовательное учреждение Высшего профессионального образования «Чувашский государственный университет имени И.Н. Ульянова» ( ФГБОУ ВПО «ЧГУ им. И.Н.Ульянова») Расчетно-графическая работа По дисциплине « Аналитическая химия и Физико-химические методы анализа» Вариант 9 Выполнил студент группы: Х-42-19 Тарасова Елена Анатольевна Проверил: Турусова Елена Васильевна Чебоксары – 2020 Вариант 9 Сколько надо взять раствора едкого кали плотности 1,350 г/мл, чтобы приготовить 4 л 0,5 М раствора? Сколько надо взять пятиводного тиосульфата натрия, чтобы получить 4 л раствора, каждый мл которого соответствовал бы 0,01 г меди? Навеска гематита массой 1,0000 г растворена в кислотах и полученный раствор разбавлен в мерной колбе до 250 мл. На титрование Fе(II) из 50,00 мл этого раствора затрачивается 20,60 мл раствора КМnO4 с концентрацией 0,1217 моль/л (f = 1/5). Сколько процентов железа содержится в гематите? Какой объем электролита лужения, содержащего 60,00 г/л SnSО4, следует взять для определения олова, чтобы на титрование затрачивалось 20,00 мл раствора иода с концентрацией 0,15 моль/л (f = 1/2) и F = 0,9314? Сколько процентов хлора содержится в нашатыре, если на навеску его, 0,1525 г, затрачивается при титровании хлорида 40,50 мл 0,05 М раствора AgNO3 с F = 1,2780? Какова должна быть навеска угля, содержащего около 1% серы, для анализа на содержание серы в виде BaSO4? Сколько г сульфата аммония нужно добавить к 250 мл воды, чтобы при промывании осадка сульфата бария потеря за счет растворения не превышала 0,001 мг? Рассчитать процентное содержание соли Мора в техническом образце, если навеска его 0,5612 г. В результате анализа было получено 0,1012 г окиси железа (III). Какова должна быть навеска сплава, содержащего 9,5% алюминия, чтобы в результате анализа получилось 0,1496 г окиси алюминия? В гидрате сульфата закисного железа, если навеска его 0,3614 г. При анализе получено 0,1038 г окиси железа. Вычислите число частиц воды. 1. Сколько надо взять раствора едкого кали плотности 1,350 г/мл, чтобы приготовить 4 л 0,5 М раствора? Табличное значение KOH: 1,350 г/мл = 31,72% 4 л = 4000 мл 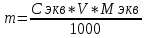 = = 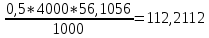 г г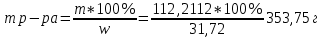 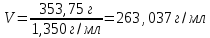 Ответ: 263,037 г/мл Сколько надо взять пятиводного тиосульфата натрия, чтобы получить 4 л раствора, каждый мл которого соответствовал бы 0,01 г меди? 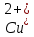 +2 +2 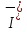 = =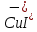 + +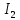 f=1 f=1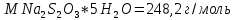 2 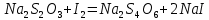 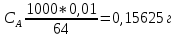 m=0, 15625*4*248, 2=155,125 г Ответ: 155, 125 г Навеска гематита массой 1,0000 г растворена в кислотах и полученный раствор разбавлен в мерной колбе до 250 мл. На титрование Fе(II) из 50,00 мл этого раствора затрачивается 20,60 мл раствора КМnO4 с концентрацией 0,1217 моль/л (f = 1/5). Сколько процентов железа содержится в гематите? 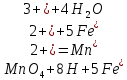 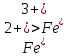 f = 1 f = 1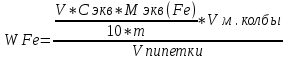 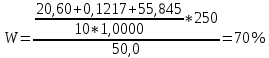 Ответ: 70% Какой объем электролита лужения, содержащего 60,00 г/л SnSО4, следует взять для определения олова, чтобы на титрование затрачивалось 20,00 мл раствора йода с концентрацией 0,15 моль/л (f = 1/2) и F = 0,9314? 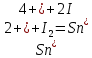 f = 2 V Sn f = 2 V Sn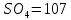 Cэкв=0, 15 моль/л * 0, 9314= 0, 13971 моль/л C 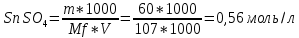 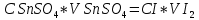 0, 56*V=0, 13971*20 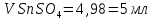 Ответ: 5 мл Сколько процентов хлора содержится в нашатыре, если на навеску его, 0,1525 г, затрачивается при титровании хлорида 40,50 мл 0,05 М раствора AgNO3 с F = 1,2780? 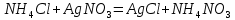 Cэкв=1, 2780*0, 05=0, 0639 моль/л 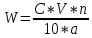 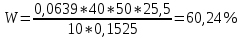 Ответ: 60,24% Какова должна быть навеска угля, содержащего около 1% серы, для анализа на содержание серы в виде BaSO4? W=1% 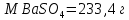 /моль /моль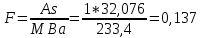 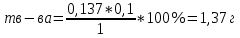 Ответ: 1,37 г Сколько г сульфата аммония нужно добавить к 250 мл воды, чтобы при промывании осадка сульфата бария потеря за счет растворения не превышала 0,001 мг? 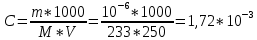 Ks=1, 1* 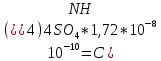 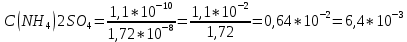 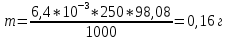 Ответ: 0,16 г Рассчитать процентное содержание соли Мора в техническом образце, если навеска его 0,5612 г. В результате анализа было получено 0,1012 г окиси железа (III). 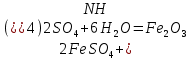 f=2 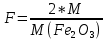 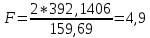 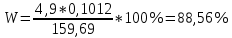 Ответ: 88,56% Какова должна быть навеска сплава, содержащего 9,5% алюминия, чтобы в результате анализа получилось 0,1496 г окиси алюминия? 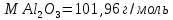 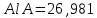 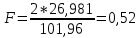 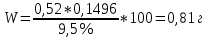 Ответ: 0,81 г В гидрате сульфата закисного железа, если навеска его 0,3614 г. При анализе получено 0,1038 г окиси железа. Вычислите число частиц воды. 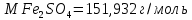 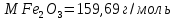 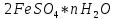 = =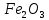 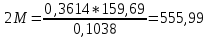 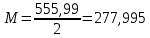 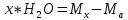 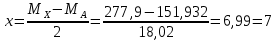 n=7 Ответ: n=7 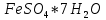 |
