ЗАДАНИЕ 4
Химическое равновесие
1. Приведите выражение для стандартной (термодинамической) константы равновесия 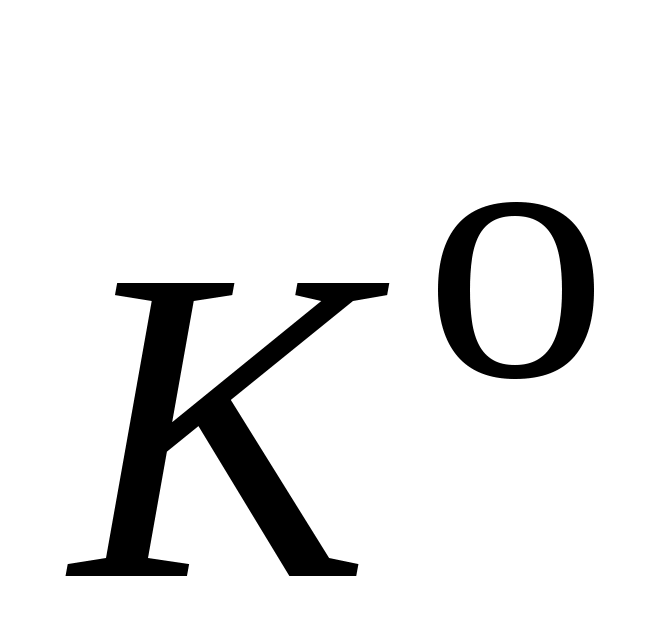 и эмпирических констант равновесия и эмпирических констант равновесия 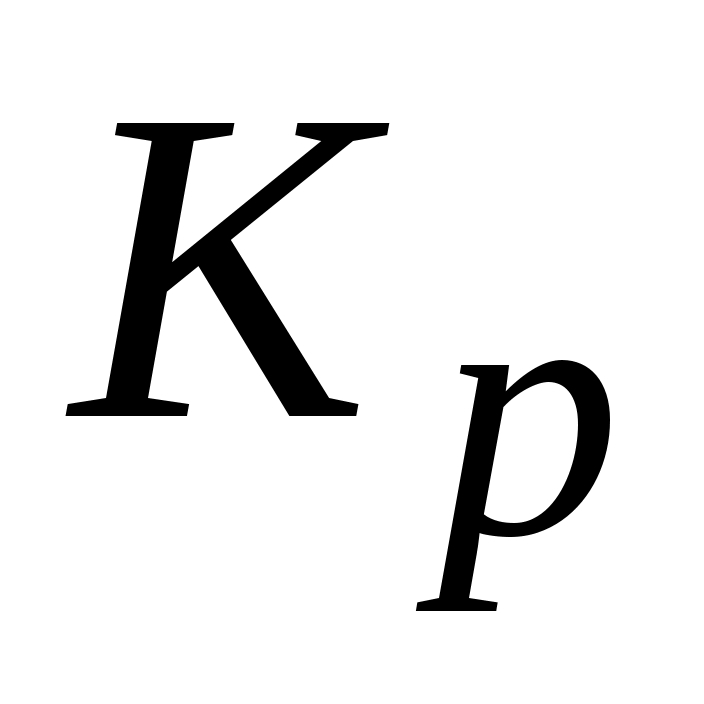 и и 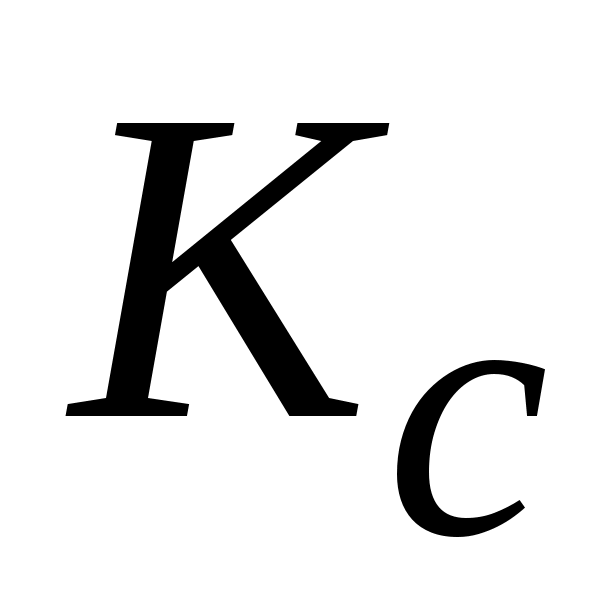 для реакции А (см. задание 1) при некоторой температуре Т. Все вещества, участвующие в химической реакции А, находятся в идеальном газообразном состоянии. для реакции А (см. задание 1) при некоторой температуре Т. Все вещества, участвующие в химической реакции А, находятся в идеальном газообразном состоянии.
Уравнение химической реакции А в общем виде:
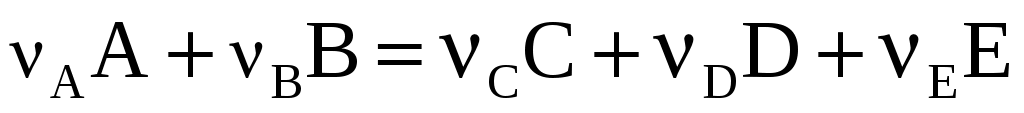
2. Выразите константу равновесия 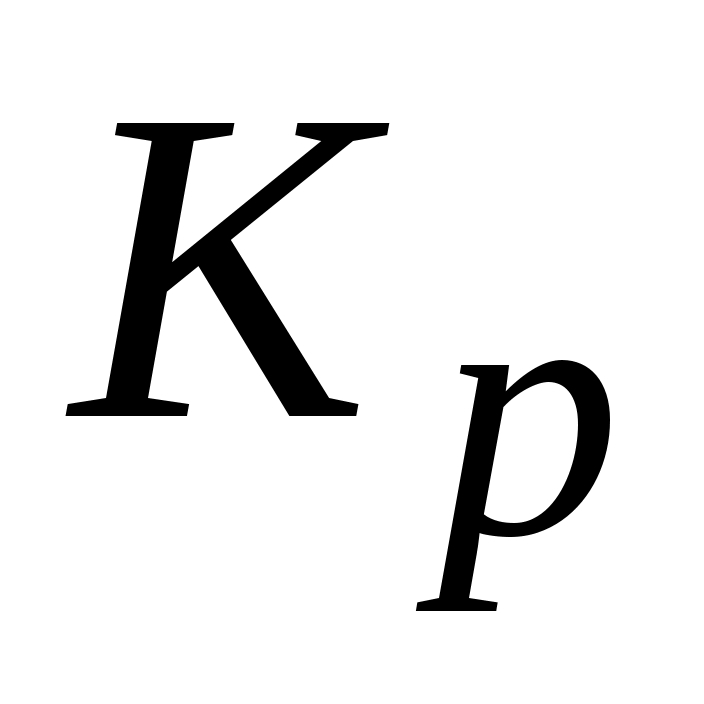 через равновесное количество молей продукта реакции С (вещество, стоящее в химическом уравнении первым с правой стороны от знака равенства), равное х, при температуре Т и общем давлении в системе через равновесное количество молей продукта реакции С (вещество, стоящее в химическом уравнении первым с правой стороны от знака равенства), равное х, при температуре Т и общем давлении в системе 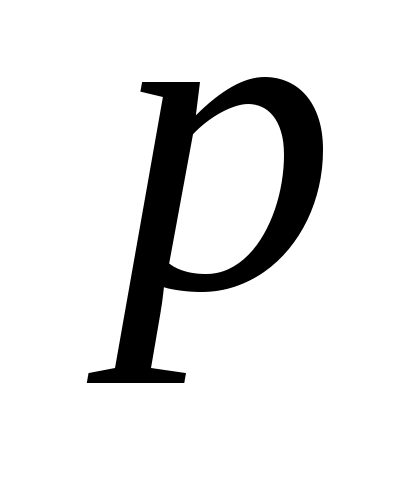 : :
а) исходные вещества взяты в стехиометрических количествах,
б) начальные количества исходных реагирующих веществ: 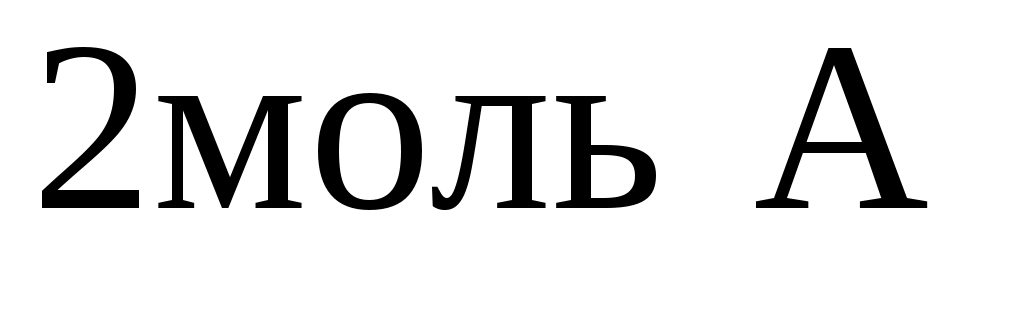 и и 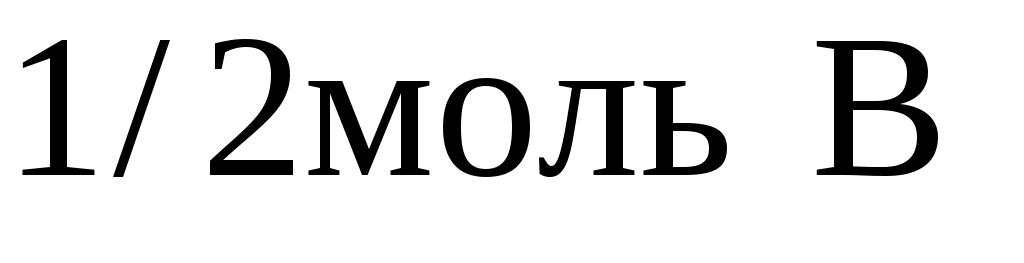 . .
Все вещества, участвующие в химической реакции А, находятся в идеальном газообразном состоянии.
3. Проанализируйте каким образом влияет на равновесный выход продукта реакции С увеличение общего давления в системе?
4. Как скажется на равновесном выходе продукта реакции С разбавление реакционной смеси инертным газом, т.е. газом, не участвующим в химическом взаимодействии, при постоянных 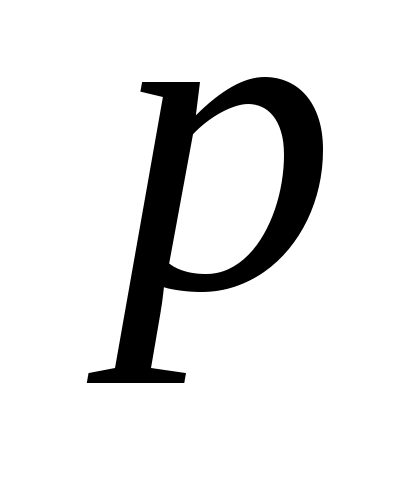 и и 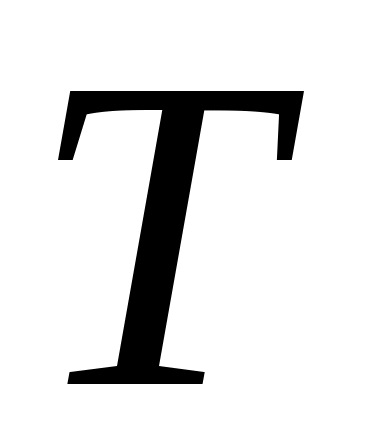 ? ?
5. Запишите выражение для константы равновесия реакции А в случае, когда реагенты – реальные газы (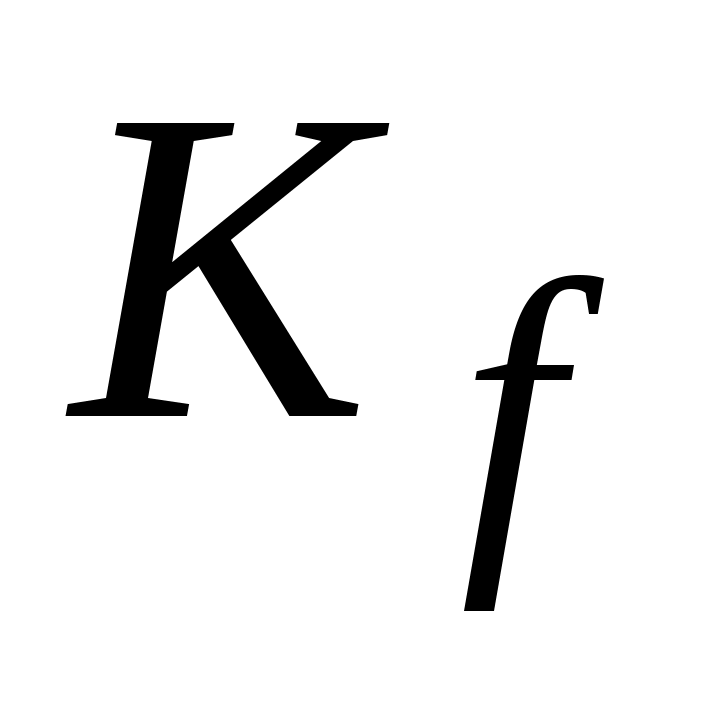 ). ).
6. Запишите уравнение, связывающее стандартное химическое сродство 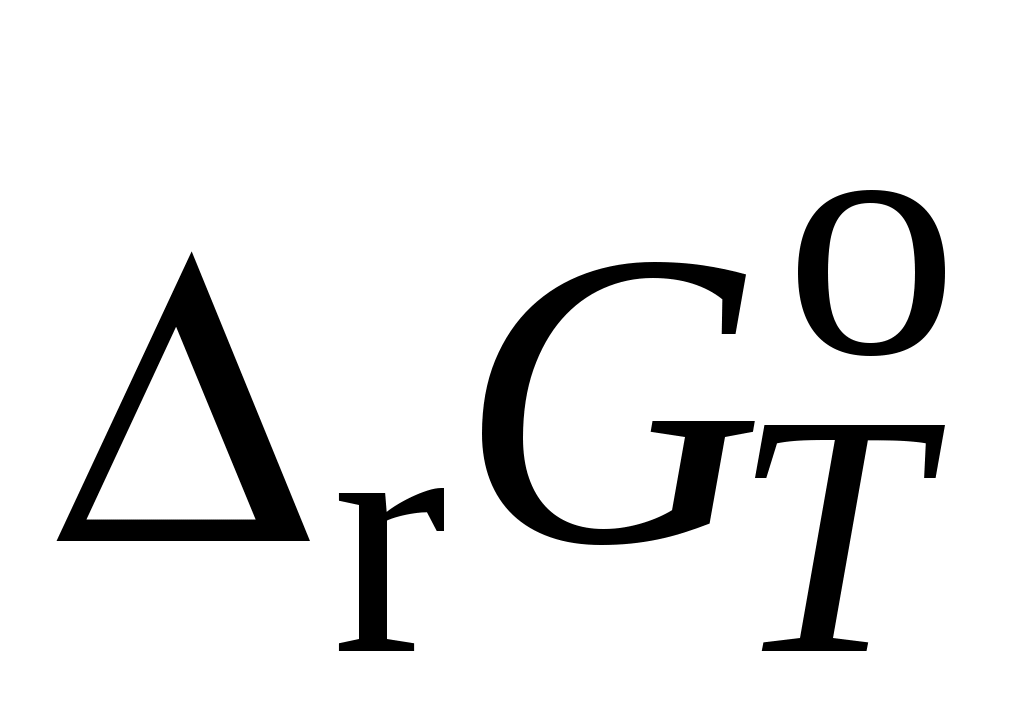 со стандартной константой равновесия. Рассчитайте стандартную константу равновесия со стандартной константой равновесия. Рассчитайте стандартную константу равновесия 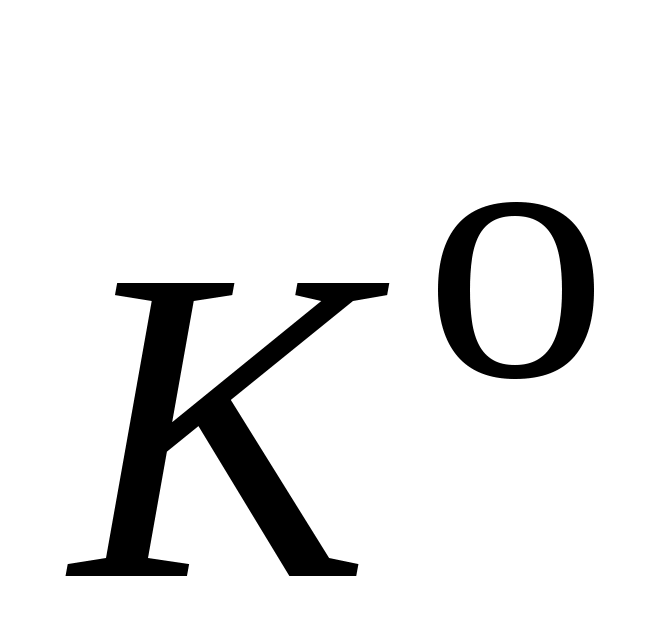 реакции А (реагенты – идеальные газы) при реакции А (реагенты – идеальные газы) при 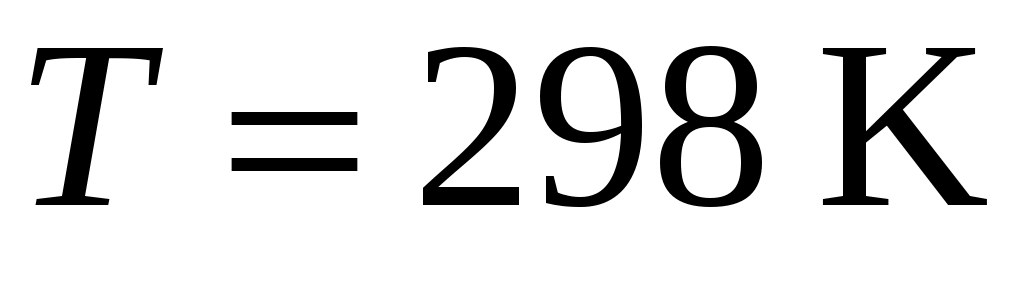 на основании значения на основании значения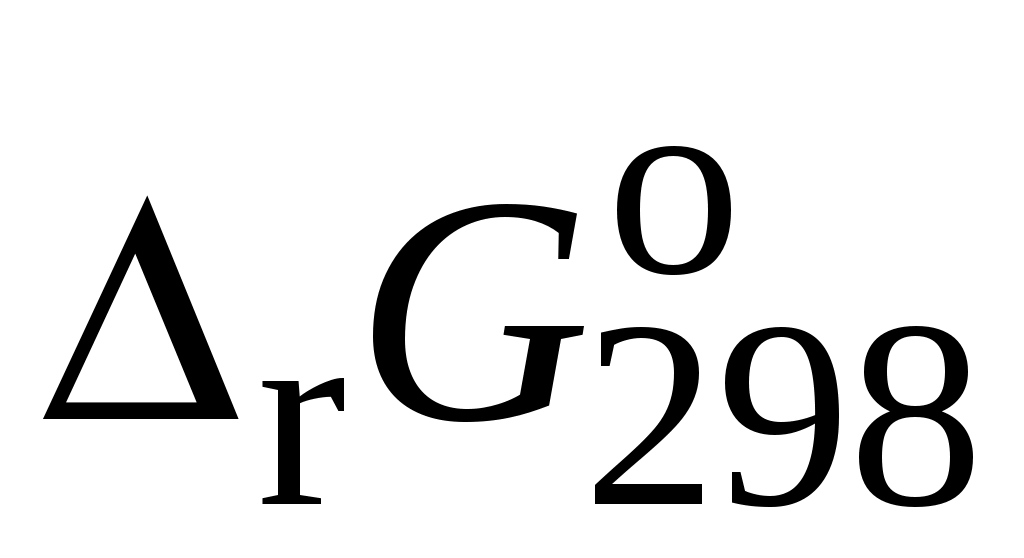 , рассчитанной в задании 2 (п. 18). , рассчитанной в задании 2 (п. 18).
7. Приведите уравнение изотермы Вант-Гоффа для химической реакции А. Определите 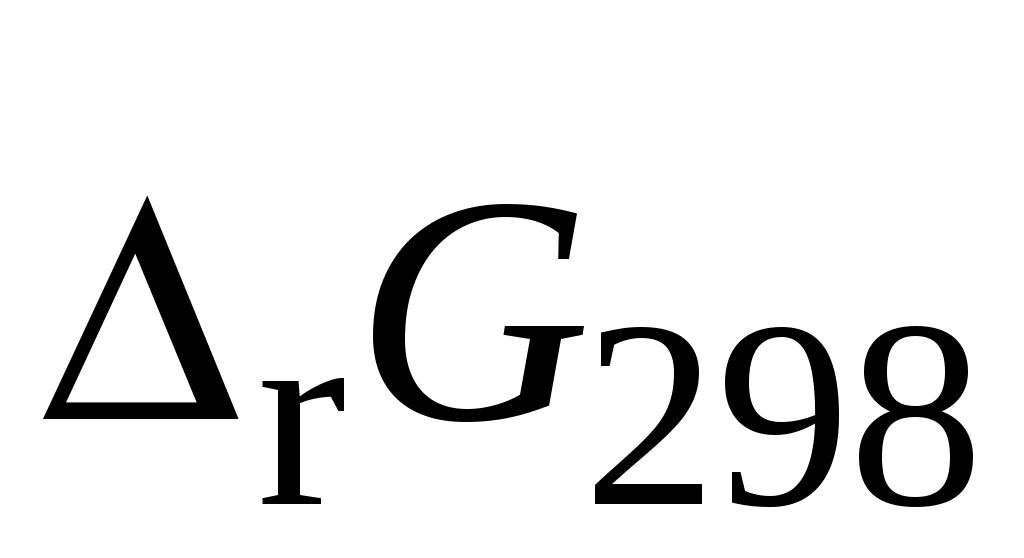 (химическое сродство, кДж) для реакции А (все реагенты – идеальные газы), если в начальный момент реакции парциальные давления реагирующих веществ A, B, C, D и E соответственно составляют рВ, рС, рD, рE и рF (табл. 4). Сделайте вывод о направлении протекания реакции А при заданных начальных условиях. (химическое сродство, кДж) для реакции А (все реагенты – идеальные газы), если в начальный момент реакции парциальные давления реагирующих веществ A, B, C, D и E соответственно составляют рВ, рС, рD, рE и рF (табл. 4). Сделайте вывод о направлении протекания реакции А при заданных начальных условиях.
8. Приведите уравнение изотермы Вант-Гоффа для случая достижения состояния равновесия.
9. Рассчитайте 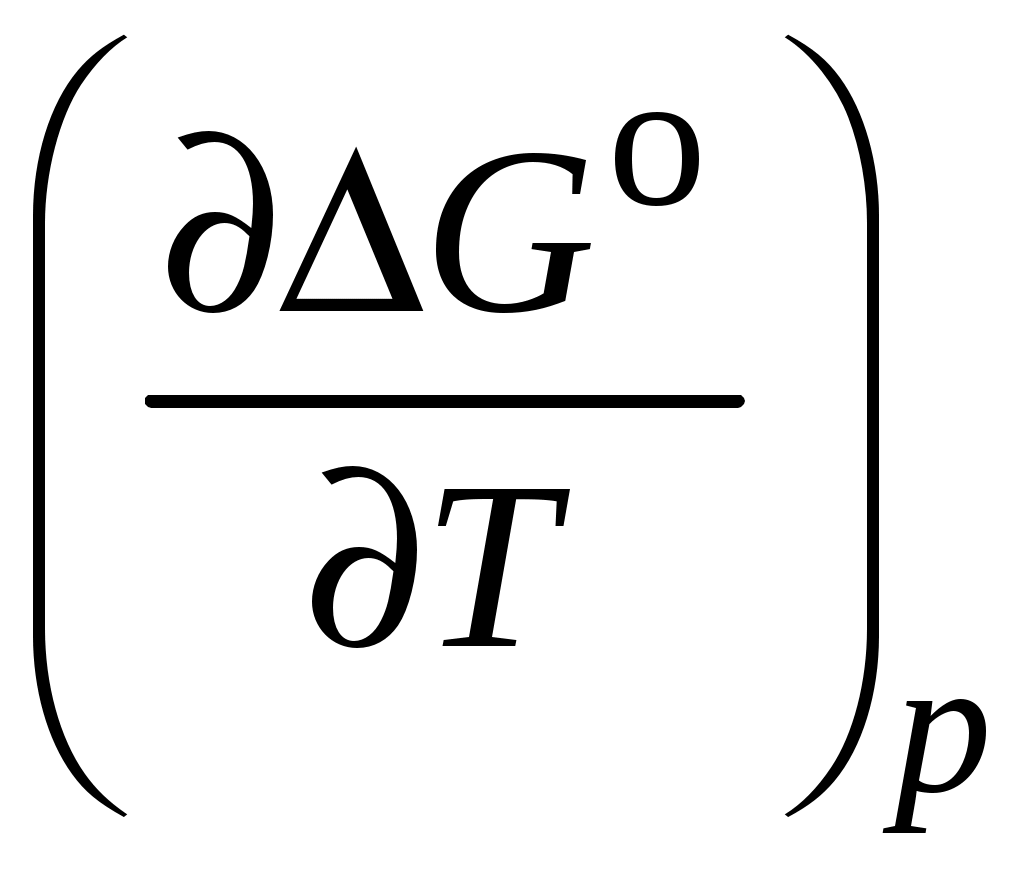 реакции А при реакции А при 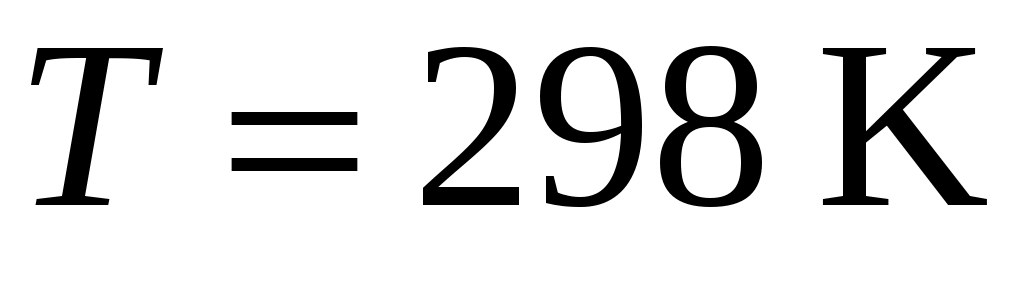 в в 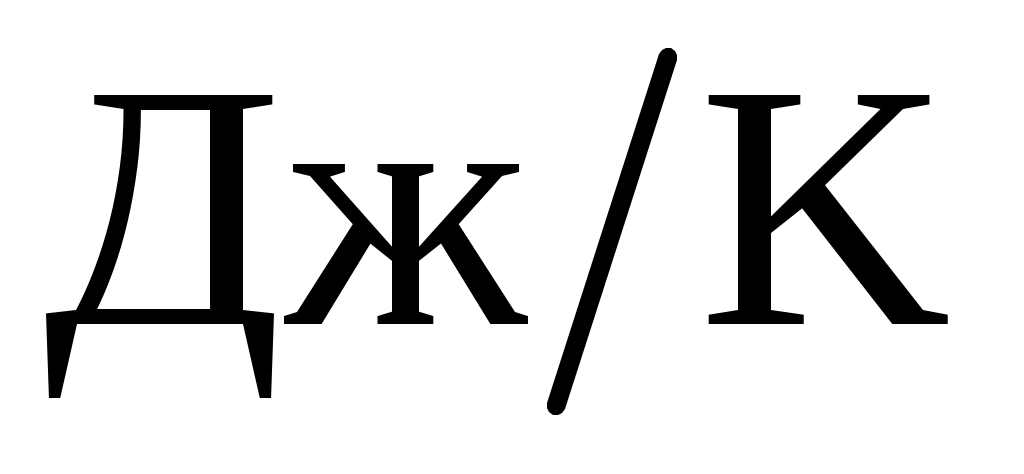 и сделайте вывод о влиянии температуры на энергию Гиббса реакции. и сделайте вывод о влиянии температуры на энергию Гиббса реакции.
10. Напишите уравнение зависимости константы равновесия химической реакции 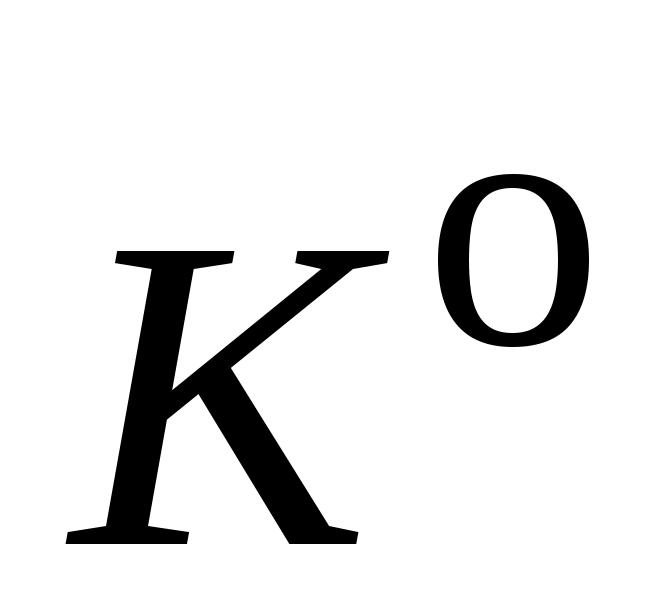 от температуры в дифференциальном виде и проведите его анализ. от температуры в дифференциальном виде и проведите его анализ.
11. Зависимость константы равновесия реакции А от температуры выражается уравнением: 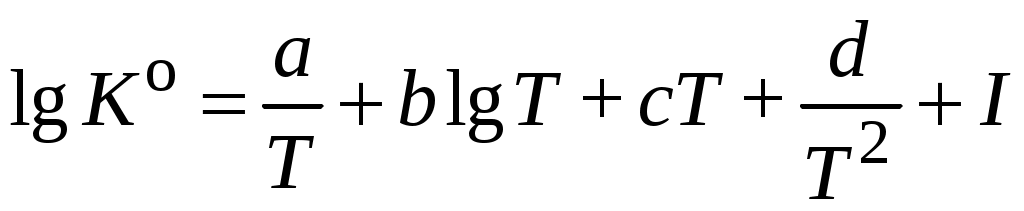 . Коэффициенты a, b, c, d и I приведены в табл. 5. Запишите уравнения . Коэффициенты a, b, c, d и I приведены в табл. 5. Запишите уравнения 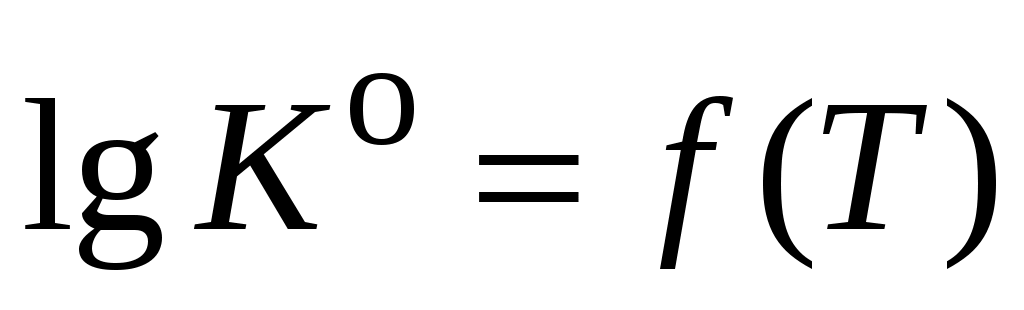 и и 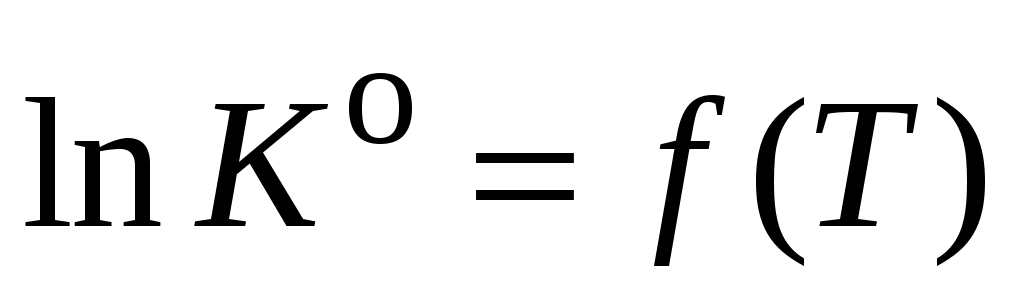 для Вашей реакции, подставив в них численные значения указанных коэффициентов. для Вашей реакции, подставив в них численные значения указанных коэффициентов.
12. Используя аналитическую зависимость 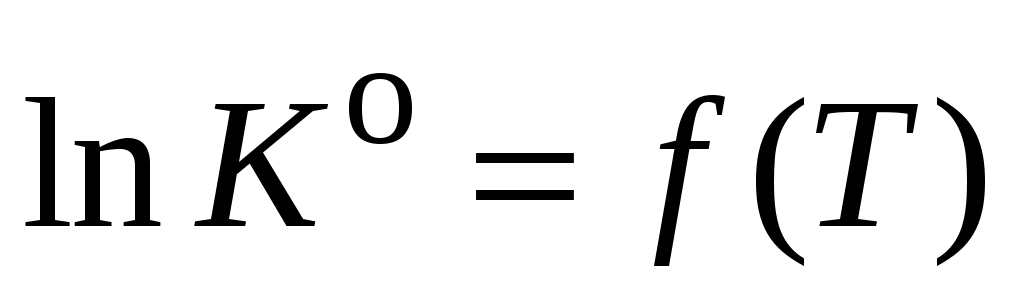 найдите производную найдите производную 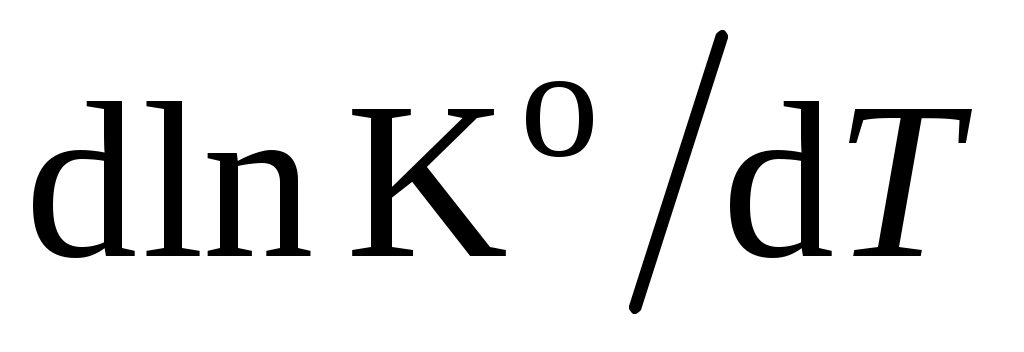 и рассчитайте величину истинного теплового эффекта реакции А при температуре Т (табл. 5) и рассчитайте величину истинного теплового эффекта реакции А при температуре Т (табл. 5)
13. Рассчитайте стандартную константу равновесия 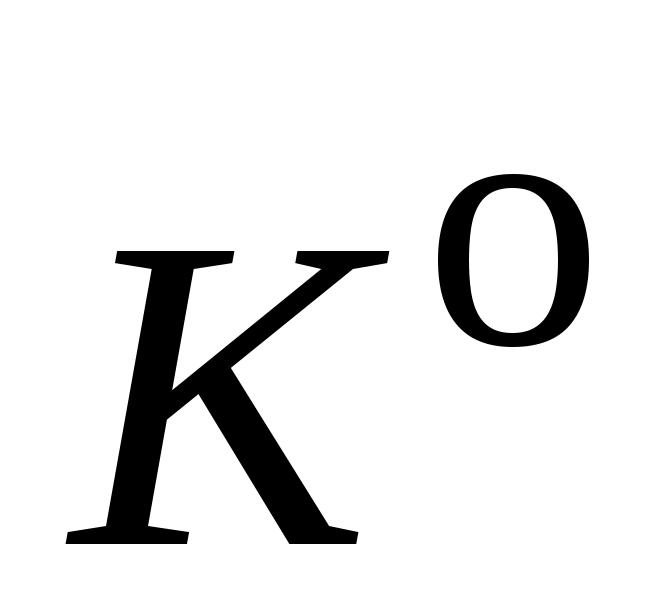 химической реакции А при температуре 298 K и 5–6 температурах в диапазоне от химической реакции А при температуре 298 K и 5–6 температурах в диапазоне от 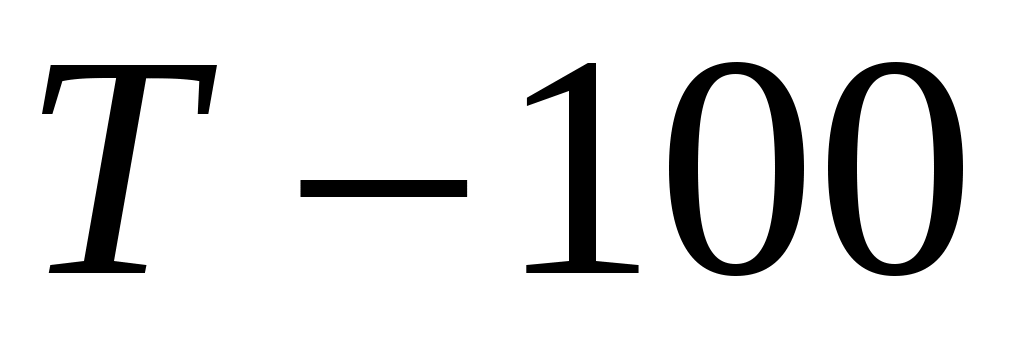 до до 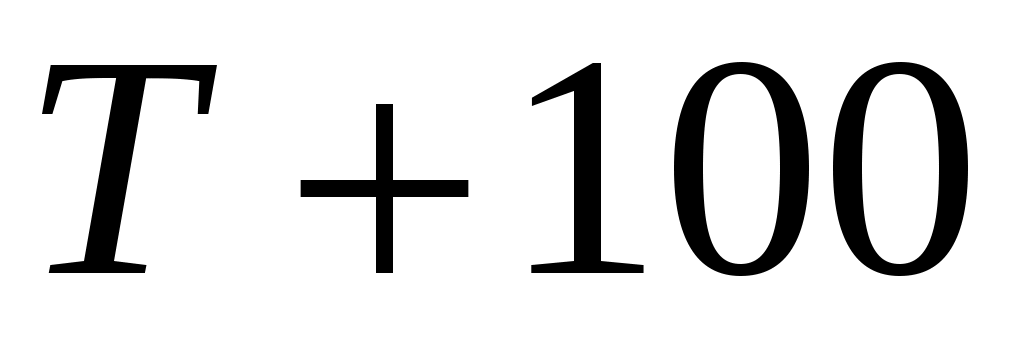 . .
14. На основании рассчитанных значений константы равновесия (п. 13) постройте график зависимости 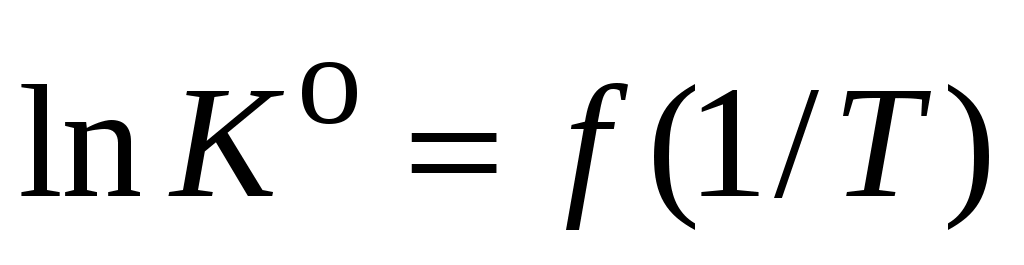 . .
15. По графику 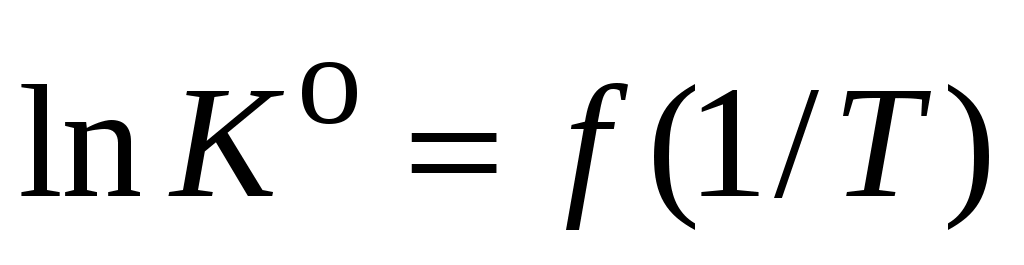 , который в небольшом температурном интервале представляет собой прямую линию, определите производную , который в небольшом температурном интервале представляет собой прямую линию, определите производную 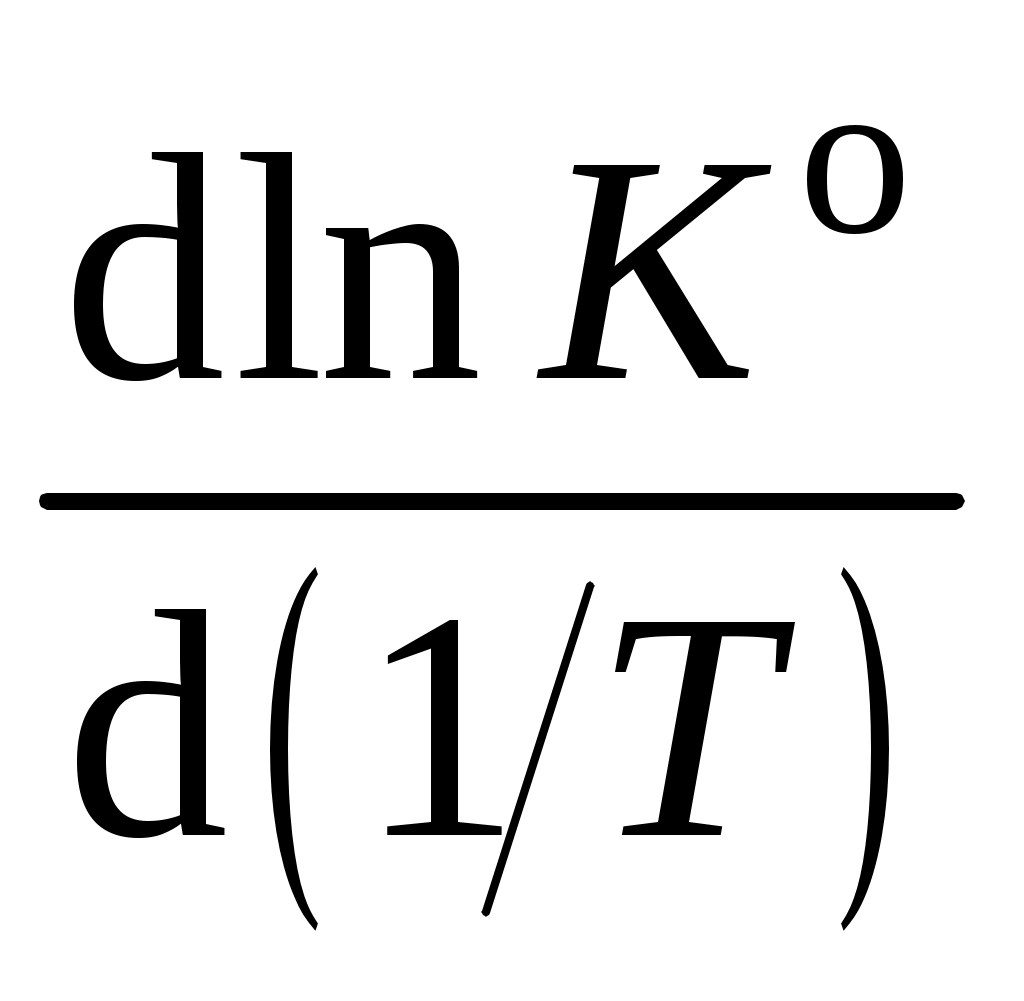 , равную тангенсу угла наклона прямой, и рассчитайте средний тепловой эффект реакции А. , равную тангенсу угла наклона прямой, и рассчитайте средний тепловой эффект реакции А.
16. На основании значений 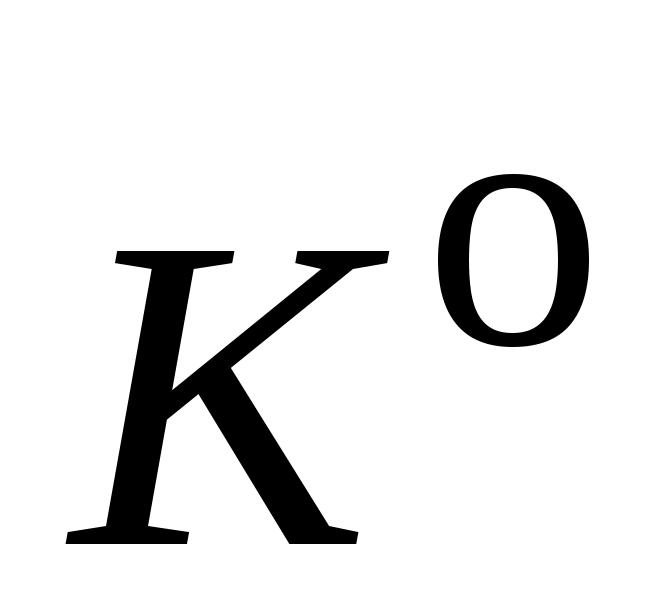 , рассчитанных в п. 13, постройте график зависимости , рассчитанных в п. 13, постройте график зависимости 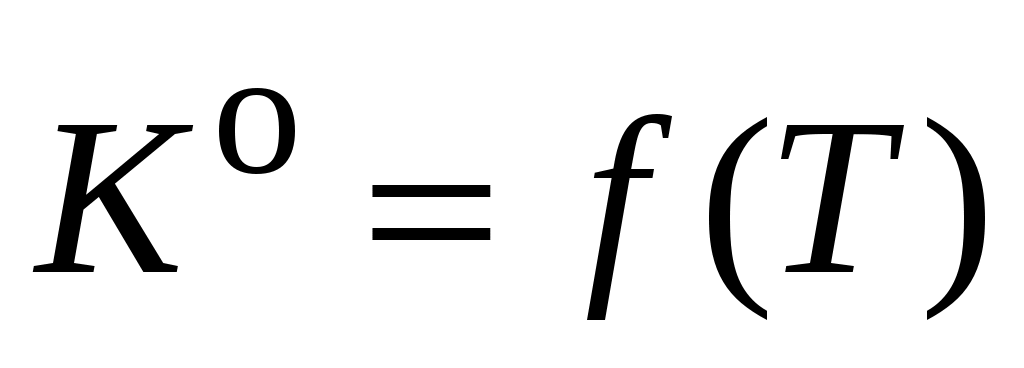 в диапазоне температур от в диапазоне температур от 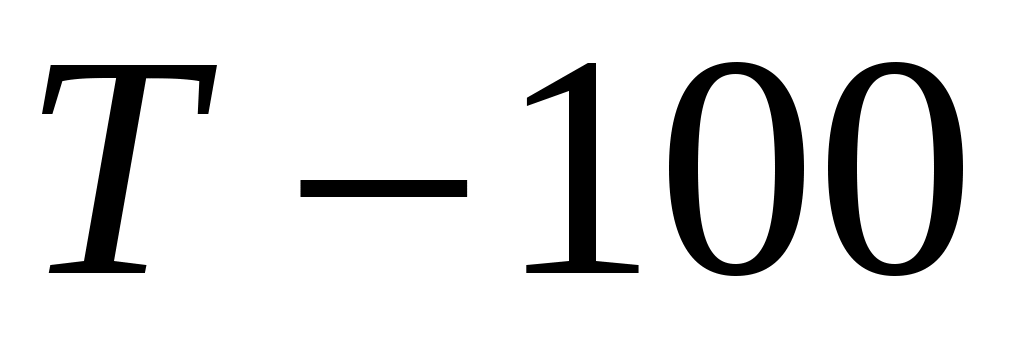 до до 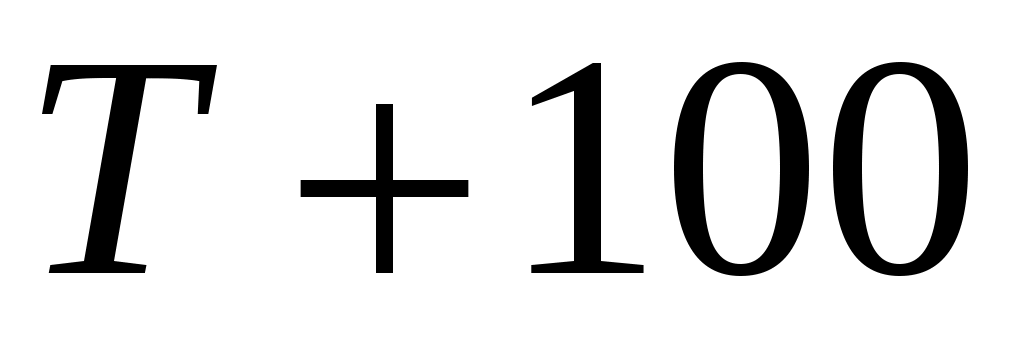 . .
17. Используя графическую зависимость 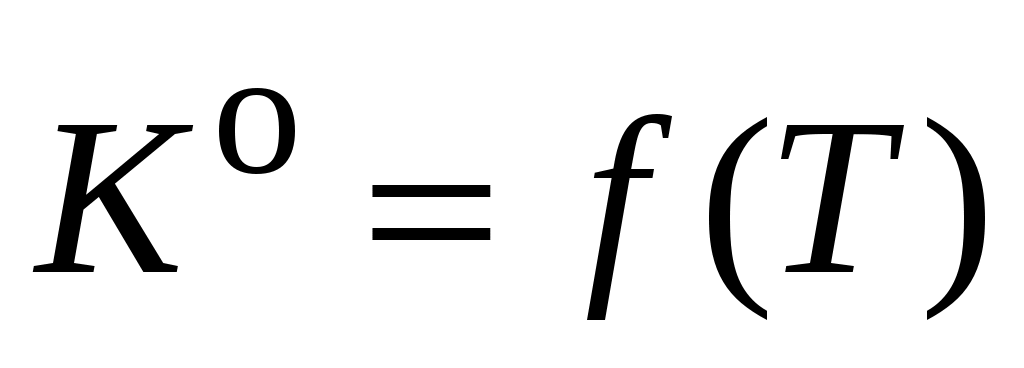 , определите значение истинного теплового эффекта реакции А при температуре T, предварительно определив производную , определите значение истинного теплового эффекта реакции А при температуре T, предварительно определив производную 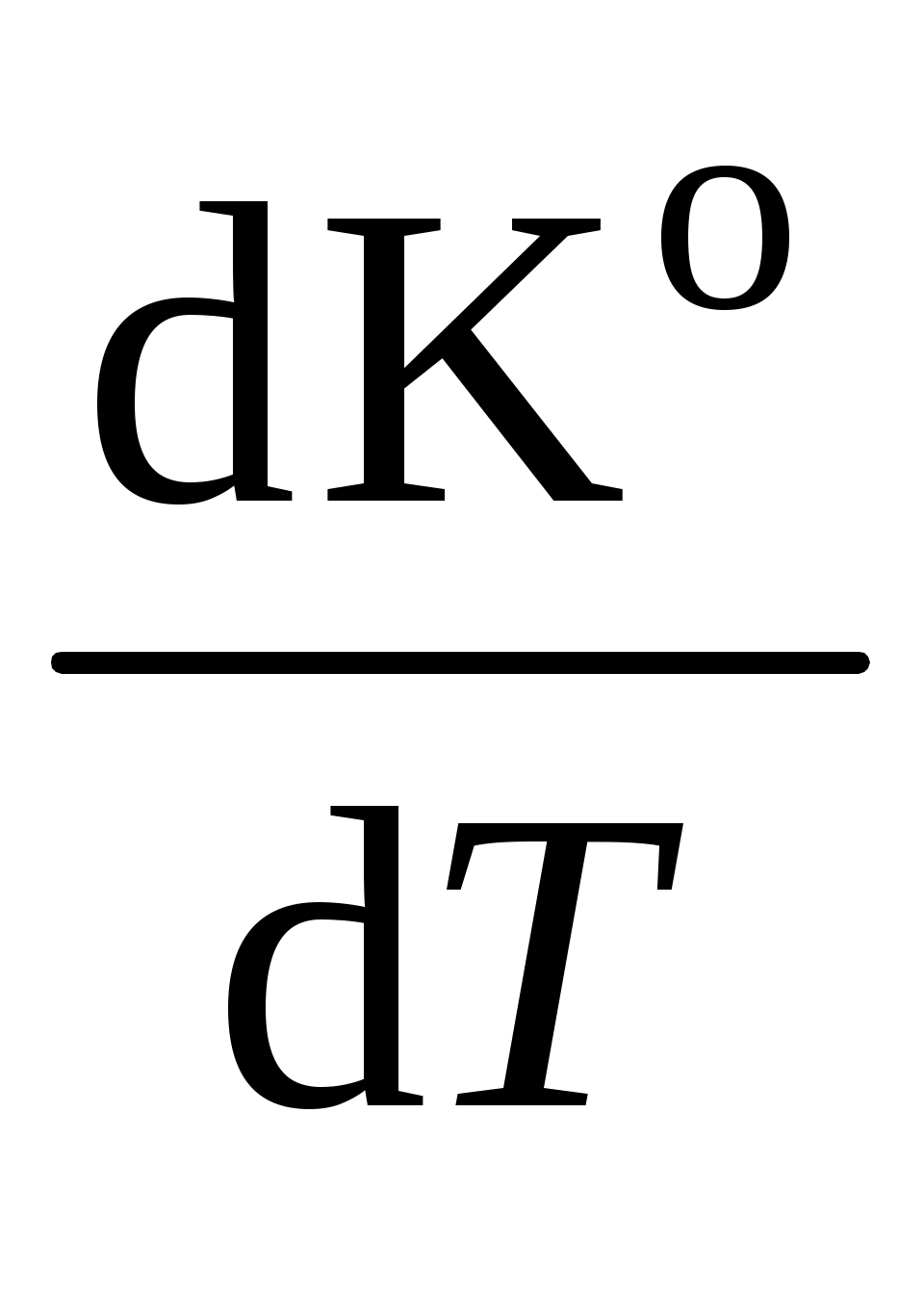 как тангенс угла наклона касательной к кривой зависимости константы равновесия как тангенс угла наклона касательной к кривой зависимости константы равновесия 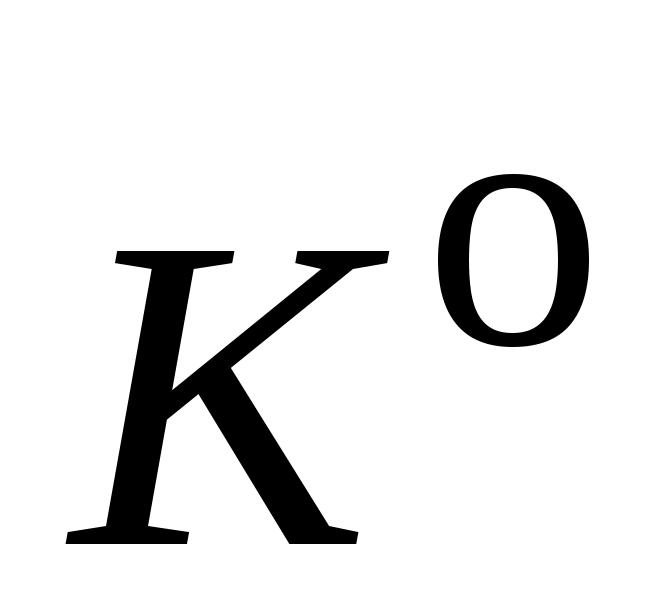 от температуры. от температуры.
Если Вы затрудняетесь выполнить это задание, то обратитесь к литературе [ 9], с. 258-283, примеры 1, 6, 7, 13, 16, 17 (задачи с решениями)
Таблица 4
№
варианта
|
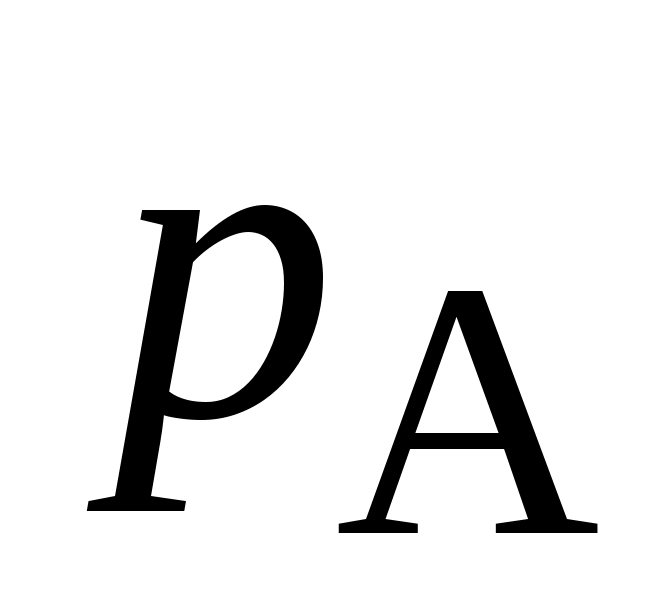 , атм , атм
|
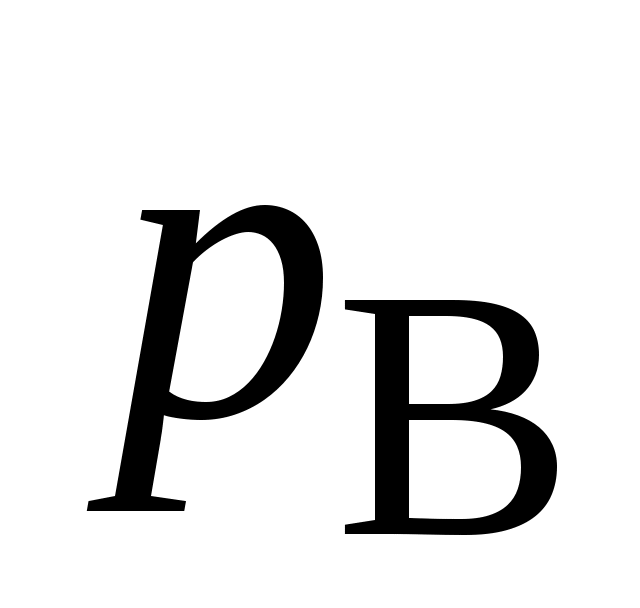 , атм , атм
|
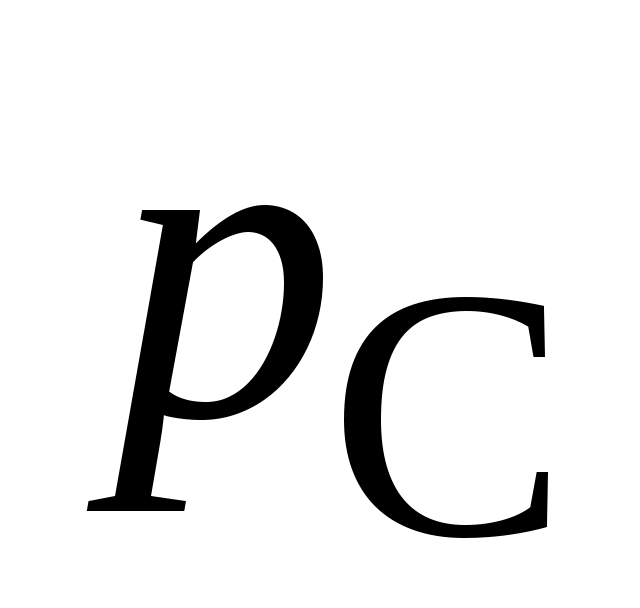 , атм , атм
|
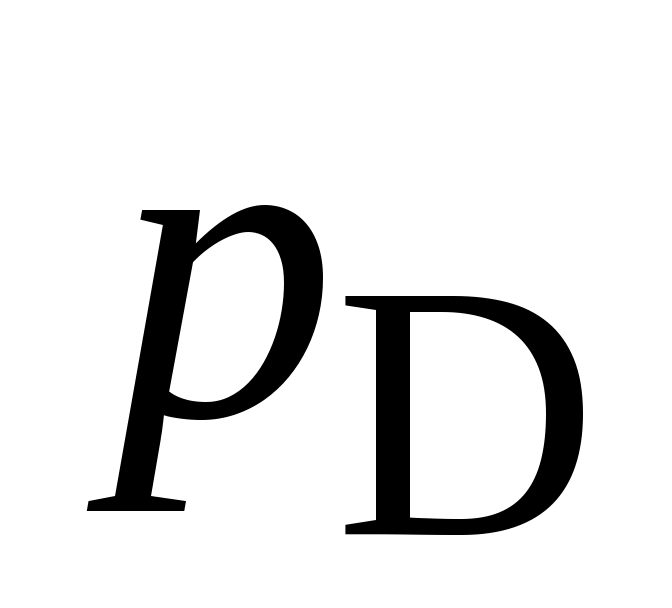 , атм , атм
|
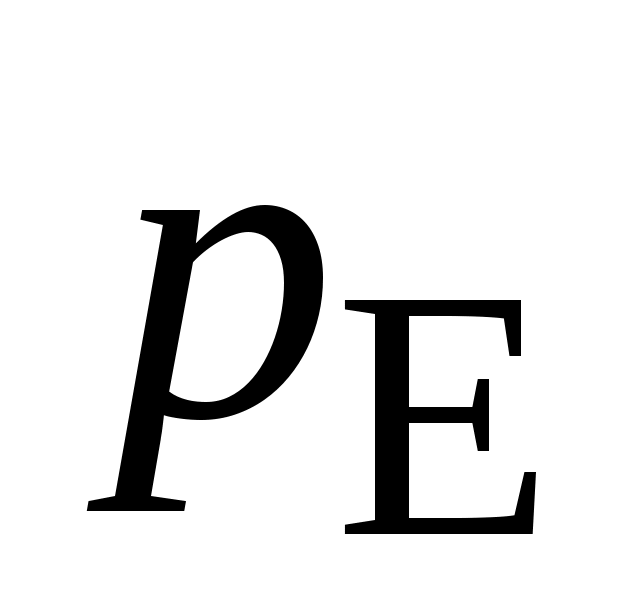 , атм , атм
|
1
|
0,20
|
0,01
|
0,01
|
-
|
-
|
2
|
1,00
|
-
|
0,10
|
0,10
|
-
|
3
|
0,40
|
0,20
|
0,10
|
0,30
|
-
|
4
|
0,10
|
0,20
|
0,10
|
0,40
|
-
|
5
|
0,08
|
0,01
|
2,00
|
0,50
|
-
|
6
|
0,01
|
0,02
|
2,00
|
-
|
-
|
7
|
0,04
|
1,5
|
4,00
|
-
|
-
|
8
|
0,02
|
0,03
|
2,00
|
-
|
-
|
9
|
0,70
|
1,60
|
1,00
|
0,40
|
0,50
|
10
|
0,10
|
0,02
|
3,00
|
0,70
|
-
|
11
|
0,50
|
-
|
0,50
|
0,50
|
0,50
|
12
|
1,00
|
2,00
|
0,20
|
-
|
-
|
13
|
1,00
|
2,00
|
0,20
|
-
|
-
|
14
|
1,00
|
2,00
|
0,20
|
-
|
-
|
15
|
1,00
|
2,00
|
0,20
|
-
|
-
|
16
|
1,00
|
2,00
|
0,20
|
0,60
|
-
|
17
|
1,00
|
2,00
|
0,20
|
3,00
|
-
|
18
|
1,00
|
2,00
|
0,20
|
1,50
|
-
|
19
|
1,00
|
2,00
|
0,20
|
0,70
|
-
|
20
|
1,00
|
2,00
|
0,20
|
-
|
-
|
Таблица 5
№
варианта
|

|
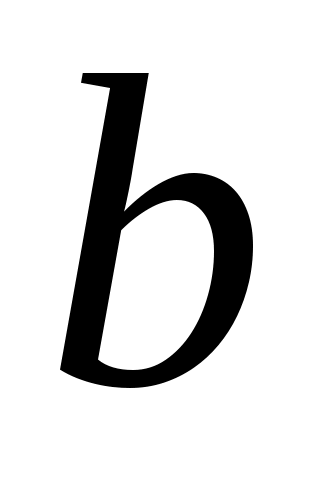
|
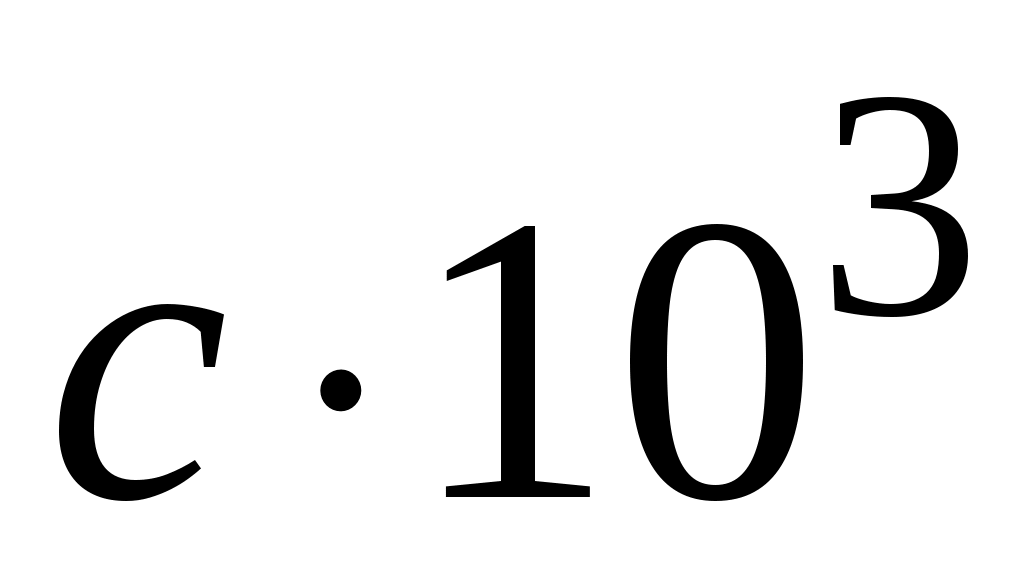
|
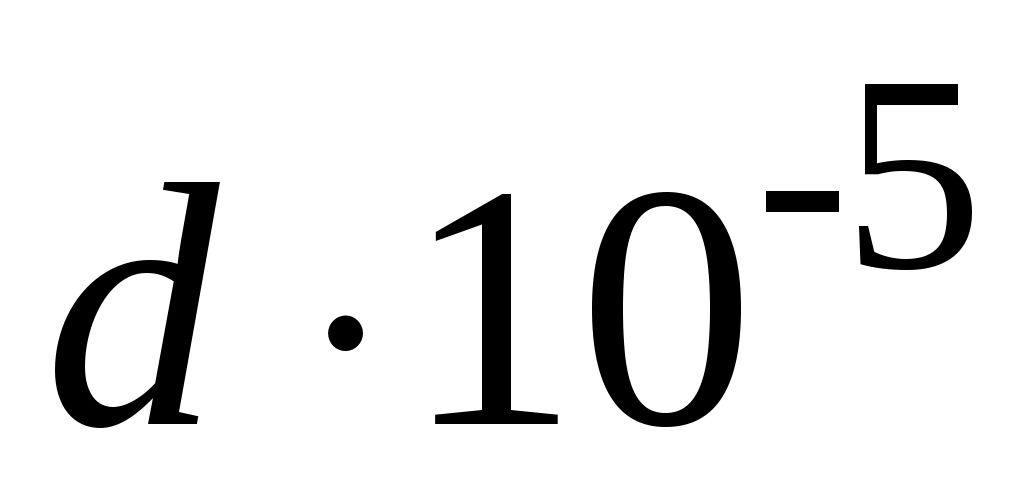
|
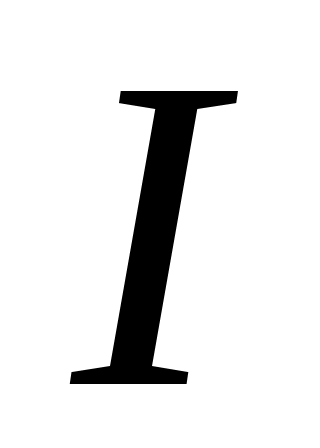
|
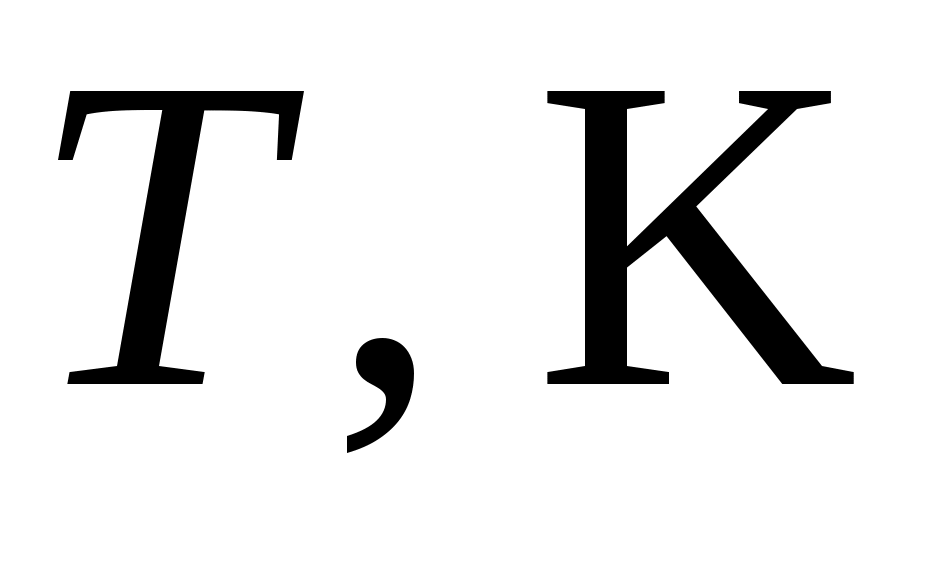
|
1
|
10050
|
-11,614
|
4,752
|
-0,002
|
11,601
|
500
|
2
|
-6365
|
2,961
|
-0,766
|
-
|
-2,344
|
400
|
3
|
-6020
|
0,423
|
-0,025
|
0,147
|
5,672
|
700
|
4
|
-47500
|
-1,750
|
-
|
-
|
-13,706
|
1000
|
5
|
9874
|
-7,140
|
1,880
|
-
|
-1,371
|
1000
|
6
|
29791
|
-
|
0,169
|
0,324
|
-9,495
|
800
|
7
|
3886
|
-8,142
|
2,470
|
-0,014
|
10,826
|
500
|
8
|
5835
|
0,206
|
0,190
|
-0,150
|
-8,032
|
400
|
9
|
17637
|
2,611
|
1,356
|
0,223
|
-3,794
|
500
|
10
|
11088
|
3,113
|
-2,852
|
-
|
-1,483
|
600
|
11
|
-4141
|
8,826
|
-2,912
|
0,030
|
-11,191
|
500
|
12
|
4189
|
-6,028
|
0,964
|
0,126
|
6,491
|
700
|
13
|
9590
|
-9,919
|
2,285
|
-
|
-6,452
|
400
|
14
|
2250
|
-1,750
|
0,455
|
-
|
-7,206
|
500
|
15
|
2049
|
-3,648
|
1,880
|
-0,009
|
2,94
|
400
|
16
|
-66250
|
-1,750
|
-
|
-
|
-10,206
|
700
|
17
|
7674
|
-6,230
|
0,906
|
-
|
-1,291
|
800
|
18
|
1522
|
5,420
|
2,290
|
-
|
-2,810
|
500
|
19
|
2485
|
1,565
|
-0,066
|
0,207
|
-6,946
|
700
|
20
|
10373
|
1,222
|
-
|
-
|
18,806
|
700
|
|
 Скачать 1.19 Mb.
Скачать 1.19 Mb.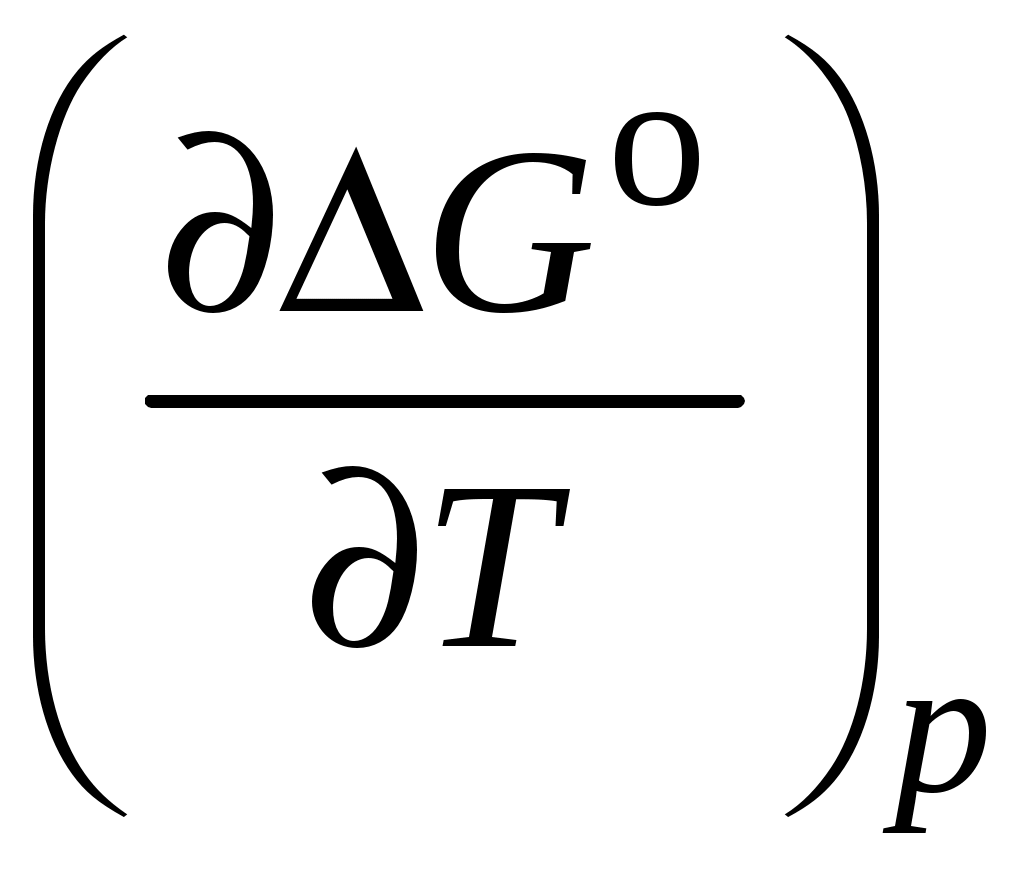 реакции А при
реакции А при 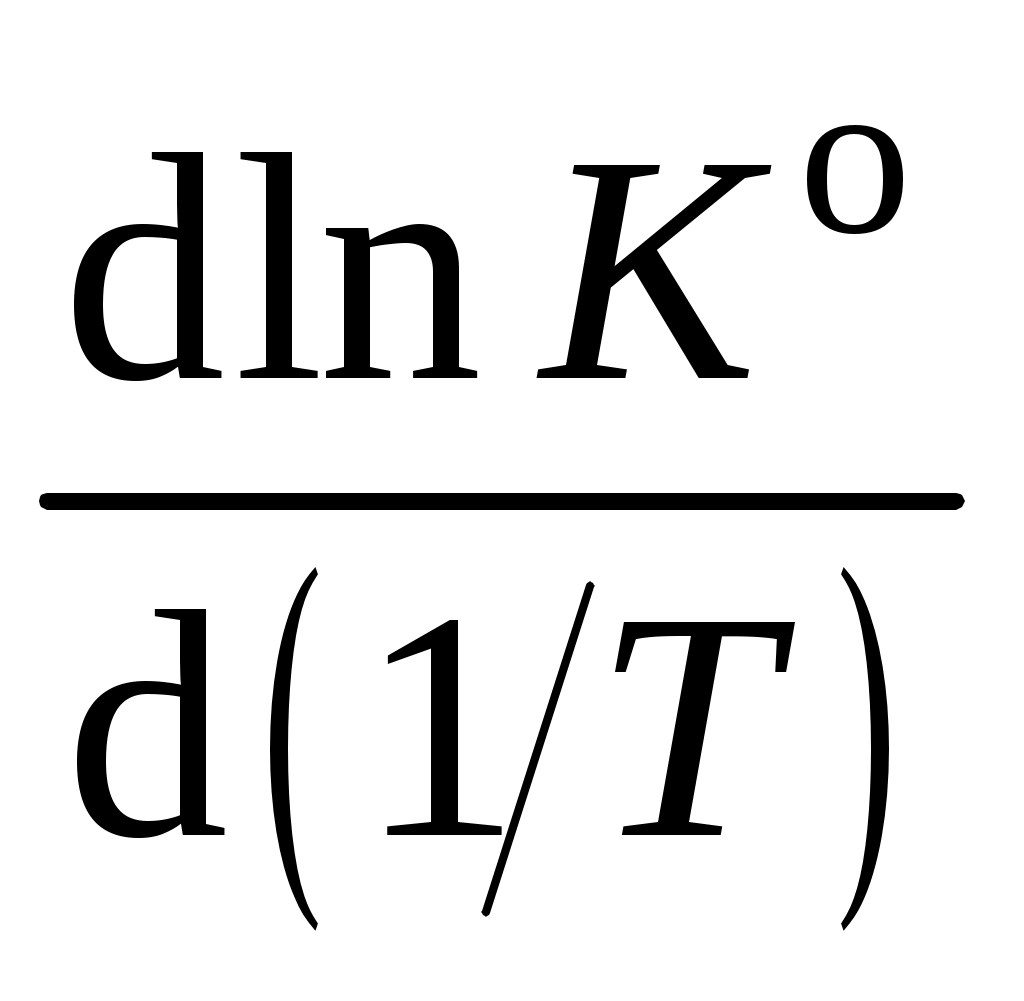 , равную тангенсу угла наклона прямой, и рассчитайте средний тепловой эффект реакции А.
, равную тангенсу угла наклона прямой, и рассчитайте средний тепловой эффект реакции А.