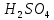лаба. Электрохимическая коррозия с водородной деполяризацией
 Скачать 53.49 Kb. Скачать 53.49 Kb.
|
|
Министерство науки и высшего образования Российской Федерации федеральное государственное бюджетное образовательное учреждение высшего образования «САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ПРОМЫШЛЕННЫХ ТЕХНОЛОГИЙ И ДИЗАЙНА» ВЫСШАЯ ШКОЛА ТЕХНОЛОГИИ И ЭНЕРГЕТИКИ Институт энергетики и автоматизации Кафедра неорганической химии ЛАБОРАТОРНАЯ РАБОТА №3по дисциплине «Защита от коррозии ОФО» на тему: Электрохимическая коррозия с водородной деполяризацией
Санкт-Петербург 2021 Цель работы: 1. Изучить теоретические основы электрохимической коррозии с водородной деполяризацией; 2. Определить скорость коррозии металлов или сплавов по потере массы и по объему выделившегося водорода, сопоставить результаты; 3. Приобрести практические навыки проведения электрохимической коррозии с водородной деполяризацией. Реагенты и оборудование: В данной лабораторной работе используется 5% раствор H2SO4 , 5% раствор H2SO4, содержащий 0,002 моль/л CuSO4 и 0,005 моль/л CuSO4, дистиллированная вода для очистки образцов металла и стаканов с кислотами. Оборудование необходимое для изучения скорости коррозии волюмометрическим методом: бюретка, полипропиленовый стакан, штатив для закрепления бюретки, пинцет для извлечения образцов металла, форвакуумный насос, фильтровальная бумага для просушки образцов, термометр, секундомер, штангенциркуль. Результаты эксперимента и расчётная работа:
Скорость коррозии, выраженная в виде объёмного показателя: 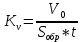 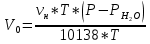 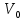 – объём выделившегося газа, см3; – объём выделившегося газа, см3; 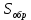 – поверхность образца, см2; – поверхность образца, см2; 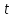 – продолжительность коррозии, ч; – продолжительность коррозии, ч; 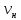 – объём выделившегося газа, см3, при температуре T и давлении P; – объём выделившегося газа, см3, при температуре T и давлении P; 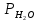 – давление насыщенного водяного пара, Па, при температуре T; 101385 – нормальное давление, Па. – давление насыщенного водяного пара, Па, при температуре T; 101385 – нормальное давление, Па.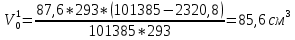 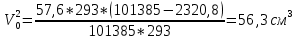 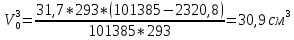 Площади образцов: 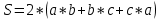 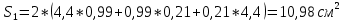 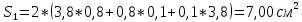 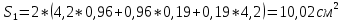 Скорость коррозии, выраженная в виде объёмного показателя: 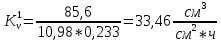 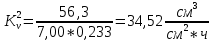 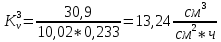 Весовой показатель скорости коррозии: 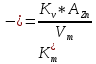 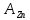 – атомная массы цинка; – атомная массы цинка; 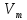 – мольный объём газа при нормальных условиях, составляющий – мольный объём газа при нормальных условиях, составляющий 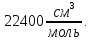 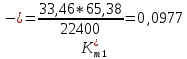 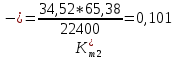 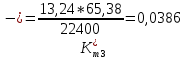 Весовой показатель, рассчитанный по изменению массы образца: 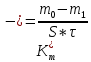 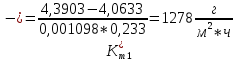 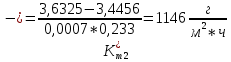 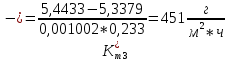 Объём выделившегося газа №1: 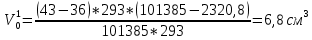 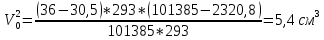 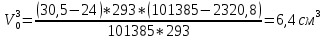 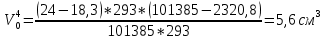 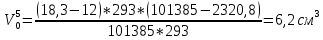 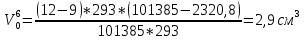 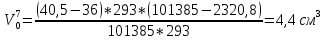 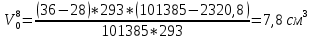 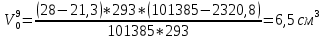 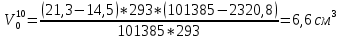 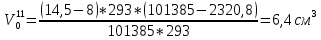 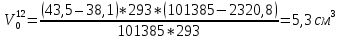 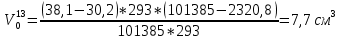 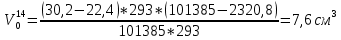 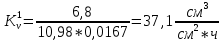 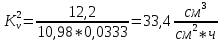 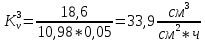 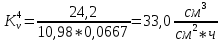 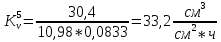 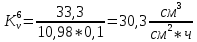 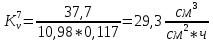 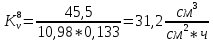 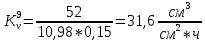 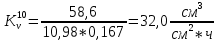 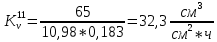 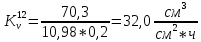 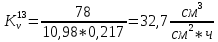 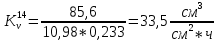 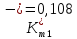 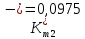 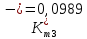 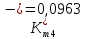 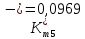 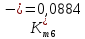 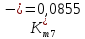 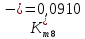 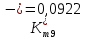 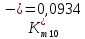 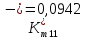 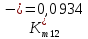 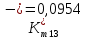 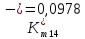 Объём выделившегося газа №2: 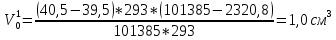 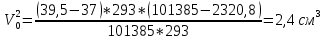 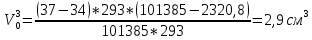 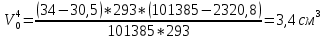 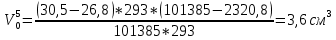 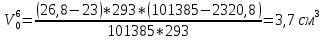 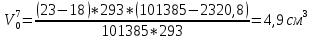 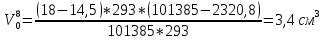 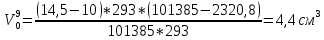 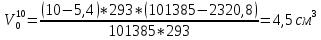 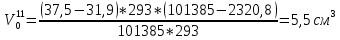 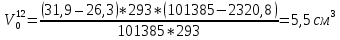 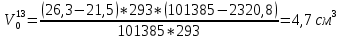 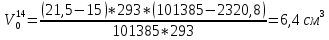 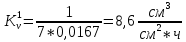 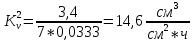 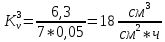 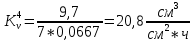 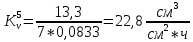 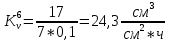 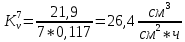 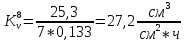 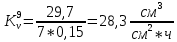 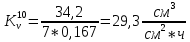 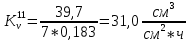 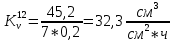 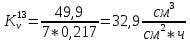 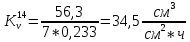 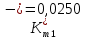 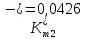 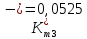 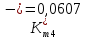 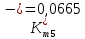 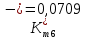 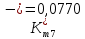 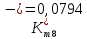 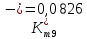 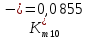 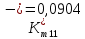 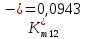 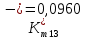 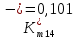 Объём выделившегося газа №3: 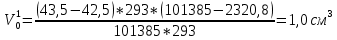 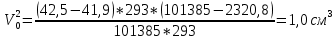 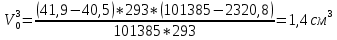 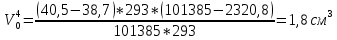 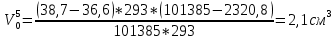 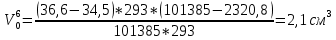 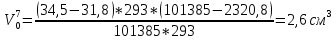 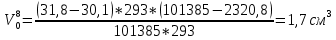 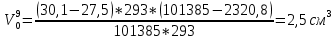 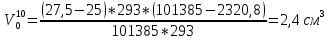 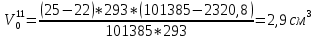 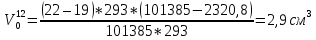 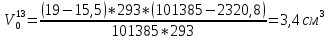 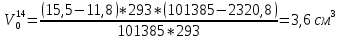 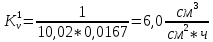 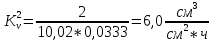 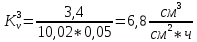 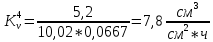 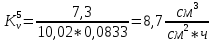 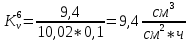 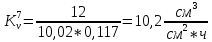 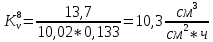 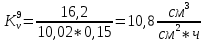 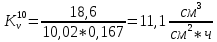 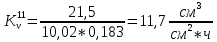 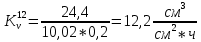 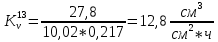 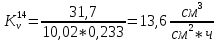 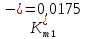 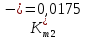 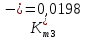 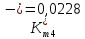 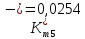 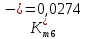 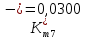 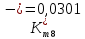 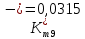 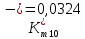 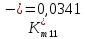 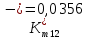 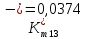 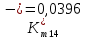 ЭДС цементации металлов-примесей: 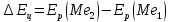 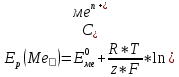 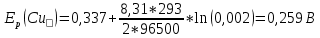 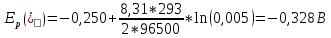 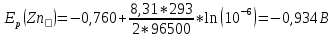 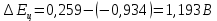 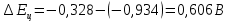
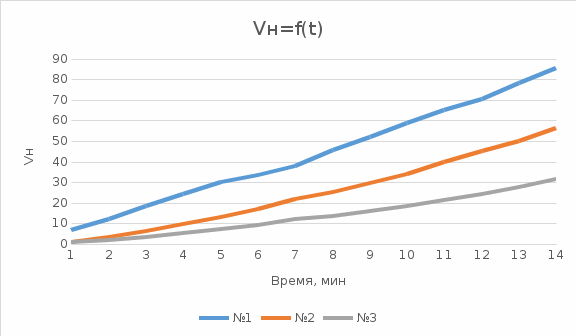 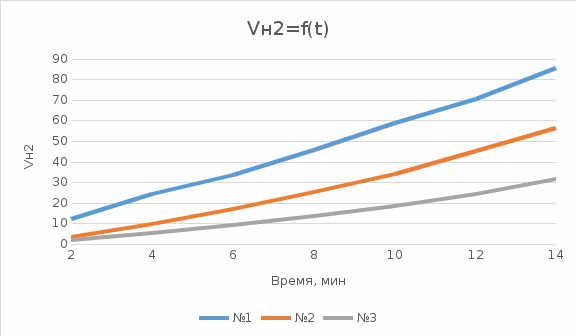 Вывод: в ходе данной лабораторной работы были изучены теоретические основы электрохимической коррозии с водородной деполяризацией. Приобретены практические навыки проведения электрохимической коррозии с водородной деполяризацией. Скорость коррозии в чистой соляной кислоте наибольшая, затем следует соляная кислота с добавлением 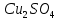 и соляная кислота с добавлением и соляная кислота с добавлением 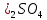 . По полученным экспериментальным данным был построен график зависимости объёма выделившегося водорода от времени. График показывает, что с увеличением интервала времени объём выделившегося водорода возрастает. . По полученным экспериментальным данным был построен график зависимости объёма выделившегося водорода от времени. График показывает, что с увеличением интервала времени объём выделившегося водорода возрастает. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||