ФОРМИРОВАНИЕ СЛОЕВ ОКСИДА КРЕМНИЯ В АТМОСФЕРЕ СУХОГО КИСЛОРОДА НА КРЕМНИИ. Формирование слоев оксида кремния в атмосфере сухого кислорода на кремнии
 Скачать 227.18 Kb. Скачать 227.18 Kb.
|
|
МИНОБРНАУКИ РОССИИ Санкт-Петербургский государственный электротехнический университет «ЛЭТИ» им. В.И. Ульянова (Ленина) Кафедра ФЭТ отчет по лабораторной работе №3 по дисциплине «Компьютерные технологии» Тема: Формирование слоев оксида кремния в атмосфере сухого кислорода на кремнии
Санкт-Петербург 2022 Цели работы: приобретение навыков моделирования процесса выращивания оксида кремния в сухом кислороде на подложке из кремния. Моделирование осуществляется в специализированном пакете Synopsys Sentaurus TCAD модулем Sentaurus Process. Общие теоретические положения Пленка оксида кремния служит в качестве маски при ионной имплантации или диффузии легирующей примеси в кремний, для пассивирования поверхности структур, для изоляции приборов друг от друга, выступает в роли одного из основных компонентов в структурах металл–оксид–полупроводник (МОП-структурах), и обеспечивает электрическую изоляцию в системах многослойной металлизации. Для создания надежных высококачественных полупроводниковых приборов ИС требуется не только понимать основной механизм окисления, но и обладать возможностью формировать высококачественный окисел контролируемым и воспроизводимым образом. Кроме того, нужно знать зависимость электрических свойств окисла от технологических параметров процесса окисления, для того чтобы гарантировать надежность полупроводниковых приборов ИС. Под окислением полупроводников понимают процесс их взаимодействия с окисляющими агентами: кислородом, водой, озоном и т. д. При определенных условиях скорость процесса окисления по мере роста концентрации окислителя уменьшается. Это явление часто называют пассивностью и связывают с образованием тонкой диэлектрической пленки, препятствующей переносу окислителя к реакционной поверхности раздела. В 1958 г. К. Вагнер ввел понятие об активном и пассивном окислении, имея в виду в первом случае процессы, не связанные с образованием оксидных пленок на поверхности исходного материала. Пассивное окисление отсутствует, когда выделяющиеся продукты реакции удаляются со скоростями, большими скорости их образования. В настоящее время процессы активного и пассивного окисления полупроводников широко используются в технологии производства современных полупроводниковых приборов при проведении операций химического или газового травления, эпитаксии, термического окисления и диффузии. При этом основное внимание технологов и разработчиков сосредоточено на процессах пассивного окисления, что объясняется первостепенной ролью пленок термически выращенной двуокиси кремния. Растворимость кислорода в кремнии довольно высока, поэтому процессы диффузии частиц окислителя в поверхностный слой подложки следует отнести к числу основных факторов, влияющих на кинетику окисления кремниевых пластин и структуру окисных пленок. Окисление материалов можно свести к трем основным стадиям: Адсорбция окислителя на поверхности материала. Диффузия частиц окислителя или окисляемого материала через пленку окисла. 3.Химическая реакция между окислителем и материалом. При окислении либо атомы окислителя (кислорода) должны проникать внутрь материала через пленку окисла, либо частицы материала должны пере мещаться к наружному слою пленки, либо эти два процесса будут происходить одновременно. Исходя из этого, видно, что в металлах данный процесс будет протекать только в том случае, когда 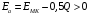 , где , где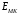 – энергия взаимодействия металла с кислородом, – энергия взаимодействия металла с кислородом, 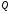 – теплота сублимации (энергия перехода атомов вещества из твердого тела в газ). – теплота сублимации (энергия перехода атомов вещества из твердого тела в газ). По величине  можно судить о возможности протекания процесса окисления. У благородных металлов можно судить о возможности протекания процесса окисления. У благородных металлов 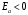 и окисление невозможно, а у неблагородных металлов и окисление невозможно, а у неблагородных металлов  и процесс окисления весьма интенсивен. и процесс окисления весьма интенсивен.В тех случаях, когда на границе раздела фаз необходимо получить низкую плотность поверхностных состояний, предпочте отдается методу термического окисления. Однако в связи с тем, что маскирующий окисел впоследствии чаще всего удаляют, условие получения минимальной плотности поверхностных состояний не играет роли при выборе метода формирования маскирующего слоя для процессов диффузии легирующей примеси в кремний. Очевидно, что при необходимости формирования окисной пленки на поверхности металлического слоя (а это характерно для процессов формирования многослойной металлизации) пригодными оказываются только методы газофазного осаждения. Опишем химическую реакцию окисления кремния: 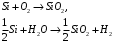 (1) (1) Процесс проводят при температуре 900…1200 °С либо в сухом кислороде по реакции (3.1), либо в увлажненном кислороде с использованием реакций (3.1), (3.2). На практике нередко применяют комбинированное окисление: сначала в сухом кислороде формируют совершенную границу раздела при толщине оксида до 0,1 мкм, а затем в увлажненном кислороде увеличивают толщину слоя до 0,4…0,8 мкм. Согласно данным радиоизотопного анализа окисляющий агент (O2 или 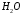 ) диффундирует через растущий слой оксида, т. е. процесс окисления про исходит на внутренней границе раздела SiO2 –Si. Так как молярный объем диоксида кремния больше, чем кремния, то примерно половина образовавшегося слоя SiO2 замещает по толщине окисленный кремний, а другая половина растет наружу. ) диффундирует через растущий слой оксида, т. е. процесс окисления про исходит на внутренней границе раздела SiO2 –Si. Так как молярный объем диоксида кремния больше, чем кремния, то примерно половина образовавшегося слоя SiO2 замещает по толщине окисленный кремний, а другая половина растет наружу.Процесс сухого окисления. Кремниевые пластины, подвергаемые окислению, сначала очищаются с помощью детергента и водного раствора, растворителей с ксилолом, изопропиловым спиртом или других веществ. Очищенные пластины высушиваются и загружаются в кварцевый держатель для пластин, который называется лодочкой. Затем они помещаются в кварцевую трубу или ячейку диффузионной печи с операторского конца (загрузочный конец). Через входной конец трубы (источник) подается высокочистый кислород или смесь кислорода и азота. Поток «сухого» кислорода контролируется в кварцевой трубе, он обеспечивает избыток кислорода для выращивания оксида кремния на поверхности кремниевой пластины. Обработка результатов эксперимента Моделирование в Synopsys Sentaurus TCAD.  Рисунок 1 – Код программы Synopsys Sentaurus TCAD 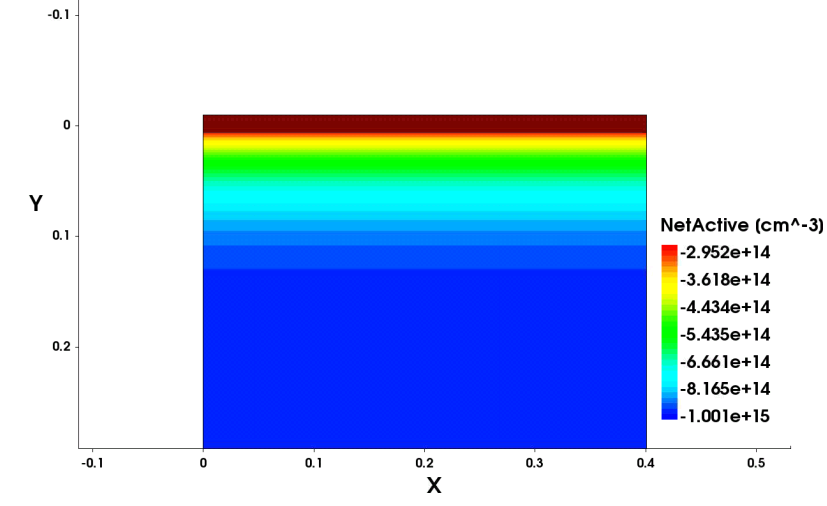 Рисунок 2 – Пример полученной структуры SiO2 на Si, для ориентации 100, времени выращивания 50 минут и температуры 900 ℃ При получении результатов, приведенных на рисунках 1 и 2, были выбраны фиксированные параметры: температура 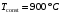 , время , время 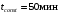 и ориентация и ориентация 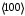 . .Формулы и постоянные для теоретического расчета  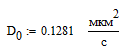 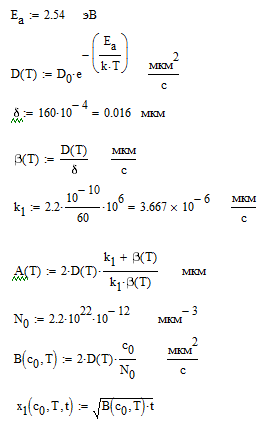  Сравнение теоретических и моделированных результатов 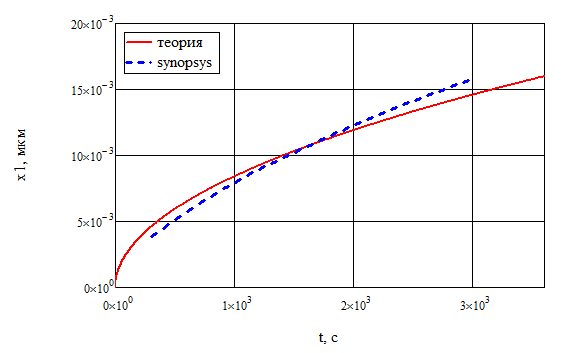 Рисунок 3 – Зависимость толщины выращенного оксида от времени при температуре 900 ℃ и кристаллографическом направлении 100 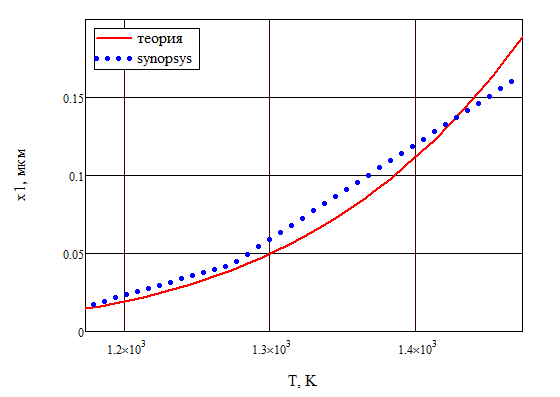 Рисунок 4 – Зависимость толщины выращенного оксида от температуры при кристаллографическом направлении 100 и времени 50 мин. Представлены графики зависимостей толщины диоксида кремния 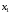 от времени от времени 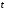 и температуры и температуры 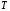 на рисунках 3 и 4 соответственно. на рисунках 3 и 4 соответственно. Рисунок 5 – Зависимость толщины выращенного оксида от времени проведения эпитаксии для различных кристаллографических направлений Выводы: В ходе выполнения лабораторной работы №3 был сформирован слой оксида кремния в атмосфере сухого кислорода в программном пакете Synopsys Sentaurus TCAD. Получили зависимости толщины оксидного слоя от времени, температуры и различных кристаллографических направлений. На рисунке 3 указана зависимость толщины оксидного слоя от времени его роста. Её вид обуславливается тем, что на начальном этапе графика у нас толщина оксидного слоя пропорциональная константа соответствует формуле h(t)≈Cл*t, где Сл – константа линейного роста. Сама константа линейного роста пропорциональная парциальному давлению окислителя в газовой фазе и коэффициенту растворимости молекул окислителя. Процесс окисления на начальном этапе протекает в кинетической области. Скорость роста линейно возрастёт при увеличении парциального давления окислителя в газовой фазе. На начальном этапе при слое с малой толщиной диффузия молекул через тонкий слой протекает достаточно быстро. На втором этапе у нас начинается параболический рост. Константа параболического роста также зависит от парциального давления. Теперь процесс у нас протекает в диффузионной области. Он управляется только диффузионным массопереносом. Через толстый слой окисла будет переносится гораздо меньше молекул, чем при обычной химической реакции. Но всё также константа параболического роста имеет вид p01/2. На рисунке 4 указана зависимость толщины оксидного слоя от температуры. Вид зависимости обуславливается тем, что на первом этапе у нас виден линей рост в кинетической области. Он обуславливается тем, что у нас идёт конкуренция двух температурных зависимостей для константы роста и коэффициента растворимости. Величина коэффициента растворимости при увеличении температуры уменьшается, но при всём этом произведение этих зависимостей растёт из-за доминирующего вклада закона Аррениуса. Поэтому при увеличении температуры у нас будет увеличиваться и константа линейного роста, которая прямопропроциональна этим двум температурным зависимостям. В диффузионной области же у нас параболический рост определяет коэффициент газопроницаемости. Энергия активации процесса диффузии теперь превосходит теплоту молекулярного растворения из-за чего вклад коэффициента газопроницаемости для коэффициента диффузии преобладает над температурной зависимостью коэффициента растворимости. Поэтому при увеличении температуры будет увеличиваться и константа параболического роста, которая прямопропорциональна коэффициенту газопроницаемости. На рисунке 5 приведена зависимость толщины пленки оксида от времени проведения эпитаксии для различных кристаллографических направлений при температуре 900 ℃. Как видно из рисунка, кристаллографическому направлению [111] соответствует наибольшая скорость роста. Кристалл при ориентации 111 имеет большую поверхностную энергию, что способствует большему выращиванию окислов. Соответственно кристаллы при 101 и 100 ориентациях имеют меньшую поверхностную энергию. СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ1. Александров, О. В. Модель термического окисления кремния на фронте объемной реакции / О. В. Александров, А. И. Дусь // Физика и техника полупроводников. – 2008. – Т. 42. – №. 11. – С. 1400. 2. Irene, E. A. Silicon Oxidation Studies: Some Aspects of the Initial Oxidation Regime / E. A. Irene // Journal of The Electrochemical Society. – 1978. – V. 125. – № 10. – P. 1708. |
